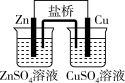
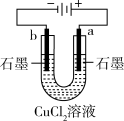
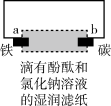
下列方程式书写正确的是
A.金属钠跟水反应: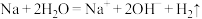 |
B.浓硝酸保存在棕色试剂瓶的原因: |
C.氢气燃烧热的热化学方程式: 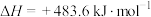 |
D.钢铁吸氧腐蚀的负极电极反应式: |
更新时间:2024-02-05 14:46:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某学生配制浓硫酸与浓硝酸的混合酸,当将浓硫酸较快地加入到浓硝酸中时,在容器口产生大量白雾,下列描述与这一现象无关的是
| A.浓硫酸具有强氧化性 | B.硝酸具有挥发性 |
| C.浓硫酸与水作用放出大量的热 | D.硝酸极易溶于水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作和现象所得结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向久置的浓硝酸中通入空气 | 溶液褪色 | 涉及化合反应 |
| B | 将某种盐溶液溶于水形成浓溶液,加入足量盐酸 | 产生白色沉淀 | 盐中可能含有Ag+或SiO |
| C | 控制相同条件,分别加热KClO3和KClO3与MnO2的混合物 | 产生等体积的气体,前者用时更长 | 催化剂能改变反应热 |
| D | 将Na2S加入含Hg2+的废水中 | 生成黑色难溶物 | 可用Na2S净化含Hg2+的废水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法中,正确的是( )
| A.可用铝制或铁制容器盛装稀硝酸 |
B.在 的盐酸中, 的盐酸中, 、 、 、 、 、 、 能大量共存 能大量共存 |
| C.56gFe与硝酸发生氧化还原反应时,转移的电子数一定是3mol |
| D.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定,见光易分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据化学实验现象得出的结论正确的是
| 选项 | 实验现象 | 结论 |
| A | 钠块放入水中,钠浮在水面上并熔化成银白色小球 | 钠的密度比水小且熔点较低 |
| B | 某溶液中滴加AgNO3溶液产生白色沉淀 | 原溶液中一定含有Cl- |
| C | 氯水滴到KBr溶液中,溶液变成橙黄色 | 氧化性:Cl2<Br2 |
| D | 分别加热等质量Na2CO3、NaHCO3固体,冷却后NaHCO3固体质量减少 | 热稳定性:Na2CO3<NaHCO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于钠和过氧化钠的性质与应用说法正确的是( )
| A.过氧化钠常用作呼吸面具中的供氧剂 |
| B.Na2O和Na2O2中氧的价态相同 |
| C.过氧化钠投入到水中会有大量氢气产生 |
| D.将一小块钠投入滴有石蕊试液的水中,反应后溶液变红 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验操作、现象和结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 碳酸钠或碳酸氯钠固体鉴别时,向盛有其中一种白色固体的烧杯中加入少量的水 | 固体结块变成晶体,并有放热的现象 | 该固体是Na2CO3 |
| B | 向澄清石灰水中加入NaHCO3溶液 | 产生白色沉淀 | 该沉淀为Ca(HCO3)2 |
| C | 将钠切割后投入滴有酚酞的水中 | 钠沉在水底,熔成小球,四处游动,溶液变红 | 钠与水反应生成了气体,并有碱生成 |
| D | 向某溶液中滴加NaOH溶液后加热,并用湿润的蓝色石蕊试纸进行检验 | 试纸变红 | 该溶液中有NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
A.已知C2H6的燃烧热为1090 kJ•mol-1,则表示C2H6燃烧的热化学方程式为:C2H6(g)+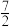 O2(g)=2CO2(g)+3H2O(g) ΔH=-1090 kJ•mol-1 O2(g)=2CO2(g)+3H2O(g) ΔH=-1090 kJ•mol-1 |
| B.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度即盐酸起始温度、NaOH溶液起始温度和反应后终止温度 |
| C.已知2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ•mol-1,则CO的燃烧热ΔH=-283 kJ |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ•mol-1,则稀醋酸与稀NaOH溶液反应生成1 mol H2O(l)时也放出57.3 kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A.已知反应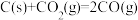 ,常温下不能自发进行,则该反应的 ,常温下不能自发进行,则该反应的 |
B.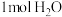 在不同状态时的熵值: 在不同状态时的熵值: |
C.已知 的燃烧热 的燃烧热 ,则 ,则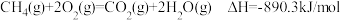 |
D. 、 、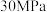 下,将 下,将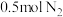 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成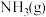 ,放热 ,放热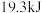 ,则其热化学方程式为 ,则其热化学方程式为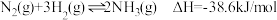 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知2CO(g)+O2(g)=2CO2(g) ΔH= -566 kJ•mol-1
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2O2(g) ΔH= -226 kJ•mol-1
下列表述正确的是
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2O2(g) ΔH= -226 kJ•mol-1
下列表述正确的是
| A.1molCO燃烧时放出的热量为283kJ•mol-1 |
| B.Na2O2(s)+CO(g)=Na2CO3(s)ΔH=-509kJ•mol-1 |
| C.Na2O2(s)与CO2(g)反应放出226kJ热量时电子转移数为2NA |
| D.Na2O2和Na2CO3中阴阳离子个数比不同 |
您最近一年使用:0次
【推荐1】下列说法正确的是
| A.蓄电池在放电过程中,负极质量减少,正极质量增加 |
| B.钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀 |
| C.钢铁在潮湿的环境中易发生吸氧腐蚀,其中负极电极反应式为Fe-3e-=Fe3+ |
| D.电解精炼铜时,若阳极质量减少64g,则转移到阴极的电子等于2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】钢铁发生两种电化学腐蚀时,下列分析正确的是( )
| A.它们的负极发生相同的反应 |
| B.它们的正极发生相同的反应 |
| C.酸性水膜条件下,正极吸收氧气 |
| D.负极都直接生成Fe3+ |
您最近一年使用:0次