三个密闭容器分别装有A.Na2O2和NaHCO3, B.Na2O2和NH4HCO3, C.Na2O2和Ca(HCO3)2,其中每种物质均为1mol。将它们加热至300℃,充分反应后排出气体。
(1)写出各容器中残余物质的化学式及物质的量。
A._____ ; B._____ ; C._____ 。
(2)如果分别加入相同浓度的足量盐酸与残留物完全反应,则消耗盐酸的体积由大到小的顺序是_____ 。
(3)如果分别将A、B、C中原物质加入水中完全反应后溶质分别是什么?现象如何?
A:_____ ; B:_____ ; C:_____ 。
(1)写出各容器中残余物质的化学式及物质的量。
A.
(2)如果分别加入相同浓度的足量盐酸与残留物完全反应,则消耗盐酸的体积由大到小的顺序是
(3)如果分别将A、B、C中原物质加入水中完全反应后溶质分别是什么?现象如何?
A:
更新时间:2024-02-12 17:55:37
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯与综合利用工艺如下:

(注:SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是___________ 。
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为___________ 。由气体Ⅱ中某物得到水玻璃的化学反应方程式为___________ 。
(3)步骤①为:搅拌、___________ 。所得溶液Ⅳ中的阴离子有___________ 。
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为___________ ,100kg初级石墨最多可能获得Ⅴ的质量为___________ kg。
(5)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注___________ 。


(注:SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为
(3)步骤①为:搅拌、
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为
(5)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组甲、乙两位同学为测定Na2CO3和NaCl混合物中Na2CO3的质量分数,分别进行实验。回答下列问题:
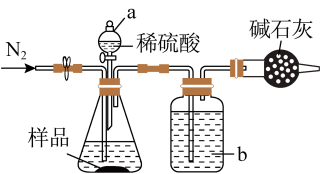
(1)甲同学用上图所示装置进行测定。称取一定质量的待测样品于锥形瓶中,反应前先打开弹簧夹,通入一段时间的N2,然后关闭弹簧夹,接上总质量为m g的干燥管,再打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗a的活塞,打开弹簧夹,再通入一段时间的N2,然后取下干燥管称得其质量为n g。
①洗气瓶b中盛放的液体是___________ (写名称)。
②第二次通入N2的目的是___________ 。
③甲同学设计的该实验装置中存在一不合理之处,会导致测定结果出现误差。如何改进?___________ 。
(2)乙同学用图中所示方法和步骤进行实验:
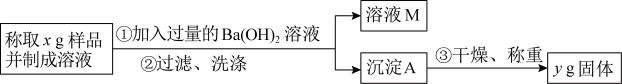
通过该方法测得样品中Na2CO3的质量分数为___________ 。(用含x和y的代数式表示)

(1)甲同学用上图所示装置进行测定。称取一定质量的待测样品于锥形瓶中,反应前先打开弹簧夹,通入一段时间的N2,然后关闭弹簧夹,接上总质量为m g的干燥管,再打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗a的活塞,打开弹簧夹,再通入一段时间的N2,然后取下干燥管称得其质量为n g。
①洗气瓶b中盛放的液体是
②第二次通入N2的目的是
③甲同学设计的该实验装置中存在一不合理之处,会导致测定结果出现误差。如何改进?
(2)乙同学用图中所示方法和步骤进行实验:
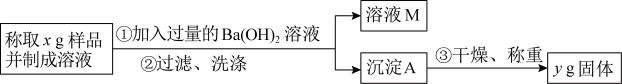
通过该方法测得样品中Na2CO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】加碘盐的推广让我国基本杜绝了“碘缺乏症”,我国在部分缺铁人群中又推广了“加铁盐”。某学习小组进行实验探究一种加铁盐(成分表中加铁成分为FeSO4,加碘成分为KIO3)的成分。
(1)配制溶液:准确称量10.00g该加铁盐,配制100mL加铁盐溶液。需要使用的玻璃仪器:烧杯、玻璃棒、____ 、____ 。
(2)离子检验:
①用洁净的铂丝蘸取溶液,灼烧铂丝,直接观察火焰呈黄色,甲同学认为含Na+,盐中未加KIO3,该加铁盐与宣传不符。“但乙同学进行实验,____ ,观察到火焰呈紫色,否定了甲同学的观点。
②另取适量溶液于试管中,先加入____ ,静置,用胶头滴管取上层清液于另一试管中,加足量稀硝酸和几滴____ 溶液,有白色沉淀,说明溶液中有Cl-。
(3)检验加铁成分:实验小组设计了以下实验,请完成表格。
(4)加铁盐国标是:含铁量为600-1000毫克每千克,含碘量不小于40毫克每千克。
定量测定:取20mL所配溶液,加入足量NaOH溶液,现象是____ ,充分反应后过滤,加热固体至质量不再变化,用分析天平称量剩余红色固体2.40mg,通过计算说明该加铁盐含铁量是否达标____ (请在答题卡写出计算过程)。
(1)配制溶液:准确称量10.00g该加铁盐,配制100mL加铁盐溶液。需要使用的玻璃仪器:烧杯、玻璃棒、
(2)离子检验:
①用洁净的铂丝蘸取溶液,灼烧铂丝,直接观察火焰呈黄色,甲同学认为含Na+,盐中未加KIO3,该加铁盐与宣传不符。“但乙同学进行实验,
②另取适量溶液于试管中,先加入
(3)检验加铁成分:实验小组设计了以下实验,请完成表格。
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取所配溶液,加入 | 无明显现象 | 溶液中存在Fe2+,且未变质 |
| 步骤2 | 继续向溶液中加入 |
定量测定:取20mL所配溶液,加入足量NaOH溶液,现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去氯化氢气体并探究CO2与过氧化钠(Na2O2)反应的实验,请回答下列问题:

(1)装置A的作用是___________ ;A中发生的反应是___________ (用离子反应方程式表示)。
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量反应后B中的固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含______ ,该小组同学继续进行探究。
(提出问题)反应后硬质玻璃管中固体的成分是什么?
(做出猜想)猜想一:Na2CO3,猜想二:Na2CO3和NaOH。
(3)(实验验证)小组同学取少量溶液M于试管中,向其中加入过量的___________ 溶液,
A.氯化钡 B.氢氧化钙 C.亚硫酸钡 D.氢氧化钡
若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想二成立。根据此猜想,写出产生白色沉淀的离子反应方程式:___________ 。
(4)(交流反思)小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,若看见有___________ 生成,也能得出同样的结论,你认为该同学的观点___________ (填“正确”或“错误”),理由是:___________ (用离子方程式表示)。
(5)研究发现过氧化钠具有较强的氧化性,二氧化硫具有较强的还原性,可以和SO2反应。写出该反应的化学方程式:___________ 。

(1)装置A的作用是
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量反应后B中的固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含
(提出问题)反应后硬质玻璃管中固体的成分是什么?
(做出猜想)猜想一:Na2CO3,猜想二:Na2CO3和NaOH。
(3)(实验验证)小组同学取少量溶液M于试管中,向其中加入过量的
A.氯化钡 B.氢氧化钙 C.亚硫酸钡 D.氢氧化钡
若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想二成立。根据此猜想,写出产生白色沉淀的离子反应方程式:
(4)(交流反思)小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,若看见有
(5)研究发现过氧化钠具有较强的氧化性,二氧化硫具有较强的还原性,可以和SO2反应。写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
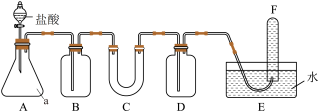
【推荐2】在呼吸面具和潜水艇中可用Na2O2做供氧剂。请选用适当的化学试剂和实验用品,用图中的实验装置进行实验,证明Na2O2可做供氧剂。___________ 。
(2)A是制取CO2的装置,写出A中发生反应的化学方程式___________ 。
(3)B中盛有饱和的NaHCO3溶液,加入该试剂是为了除去CO2中的HCl气体,反应的离子方程式是___________ 。
(4)用___________ 检验F中收集到的气体。
(2)A是制取CO2的装置,写出A中发生反应的化学方程式
(3)B中盛有饱和的NaHCO3溶液,加入该试剂是为了除去CO2中的HCl气体,反应的离子方程式是
(4)用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在实验室里为了研究钠的性质,做了如下实验:
(1)将一小块钠投入到FeCl3溶液中,发生反应的有关离子方程式为___________ 、___________ 。
(2)现用金属钠和空气制备纯度较高的Na2O2(不考虑空气中的N2参与反应),所用装置如图所示。

回答下列问题:
①上述装置Ⅳ中盛放的试剂是___________ ,为完成实验应将装置Ⅳ接在___________ (填字母)。
A.Ⅰ之前 B.Ⅰ和Ⅱ之间 C.Ⅱ和Ⅲ之间 D.Ⅲ之后
②若没有装置Ⅰ可能导致生成的Na2O2中含有杂质,用化学方程式表示该杂质的生成过程___________ 。
③装置Ⅲ的作用是___________ 。
④为制得更纯的Na2O2,应在通空气___________ 点燃酒精灯(填“前”或“后”)。
(3)海绵钛可与热的浓硝酸发生反应:Ti+8HNO3(浓) Ti(NO3)4+4NO2↑+4H2O。
Ti(NO3)4+4NO2↑+4H2O。
①用单线桥表示该反应电子转移的方向和数目___________ 。
②该反应过程中硝酸体现的性质是___________ 和___________ ;若要溶解12kg金属钛,实际参与反应的HNO3的质量为___________ kg。
(1)将一小块钠投入到FeCl3溶液中,发生反应的有关离子方程式为
(2)现用金属钠和空气制备纯度较高的Na2O2(不考虑空气中的N2参与反应),所用装置如图所示。

回答下列问题:
①上述装置Ⅳ中盛放的试剂是
A.Ⅰ之前 B.Ⅰ和Ⅱ之间 C.Ⅱ和Ⅲ之间 D.Ⅲ之后
②若没有装置Ⅰ可能导致生成的Na2O2中含有杂质,用化学方程式表示该杂质的生成过程
③装置Ⅲ的作用是
④为制得更纯的Na2O2,应在通空气
(3)海绵钛可与热的浓硝酸发生反应:Ti+8HNO3(浓)
 Ti(NO3)4+4NO2↑+4H2O。
Ti(NO3)4+4NO2↑+4H2O。①用单线桥表示该反应电子转移的方向和数目
②该反应过程中硝酸体现的性质是
您最近一年使用:0次



