氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)氯碱工业的反应原理为 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ 。
(2)为了防止食品变质而添加的抗氧化剂应具有___________ 性。(填“氧化”或“还原”)
(3)电子工业中常用 溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为
溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为___________ 。
(4) 可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应:
可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应: ,由此可知
,由此可知 的氧化性
的氧化性___________ (填“>”或“<”) 。该反应中氧化剂与还原剂的物质的量之比为
。该反应中氧化剂与还原剂的物质的量之比为___________ 。
(1)氯碱工业的反应原理为
 ,该反应中的氧化剂是
,该反应中的氧化剂是(2)为了防止食品变质而添加的抗氧化剂应具有
(3)电子工业中常用
 溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为
溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板,其反应的离子方程式为(4)
 可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应:
可用于制备铬矾、铬颜料等,也是制造火柴头的原料之一。已知反应: ,由此可知
,由此可知 的氧化性
的氧化性 。该反应中氧化剂与还原剂的物质的量之比为
。该反应中氧化剂与还原剂的物质的量之比为
更新时间:2024-02-19 08:10:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
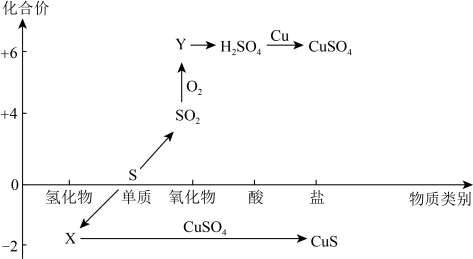
【推荐1】硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)X与 反应的化学方程式是
反应的化学方程式是___________ ,氧化剂是___________ (填化学式)。
(3)
___________ (填“是”、或“不是”)电解质,检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(2)X与
 反应的化学方程式是
反应的化学方程式是(3)

 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应是一类重要的反应,在工农业生产生活中都有广泛的用途。
(1)“维生素C可以将食物中的 转化为
转化为 ,说明维生素C具有
,说明维生素C具有___________ (填“氧化性”或“还原性”)。
(2)高铁酸钠( )是一种新型绿色消毒剂,其一种在碱性环境中制备原理如下:
)是一种新型绿色消毒剂,其一种在碱性环境中制备原理如下:

①请配平该方程式___________ ;(写出完整的方程式)
②该反应产物 中,Fe元素显
中,Fe元素显___________ 价;
(3)金属Cu可与硝酸反应, ;
;
①该反应中,硝酸体现了酸性和氧化性,其分子个数比例为___________ ;
②每生成1个NO分子,转移电子数为___________ 。
(1)“维生素C可以将食物中的
 转化为
转化为 ,说明维生素C具有
,说明维生素C具有(2)高铁酸钠(
 )是一种新型绿色消毒剂,其一种在碱性环境中制备原理如下:
)是一种新型绿色消毒剂,其一种在碱性环境中制备原理如下:
①请配平该方程式
②该反应产物
 中,Fe元素显
中,Fe元素显(3)金属Cu可与硝酸反应,
 ;
;①该反应中,硝酸体现了酸性和氧化性,其分子个数比例为
②每生成1个NO分子,转移电子数为
您最近一年使用:0次
【推荐3】氧化还原反应在生产生活中有很多实际应用。
I.高铁酸钾( )是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
)是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到 ,反应为:
,反应为: ,该反应的氧化产物是
,该反应的氧化产物是___________ ;每生成 转移电子数目为
转移电子数目为___________ 。
(2)湿法制备高铁酸钾( )的反应体系中有六种数粒:
)的反应体系中有六种数粒: 、
、 、
、 、
、 、
、 、
、 写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:
写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:___________ 。
(3)低温下,在高铁酸钠溶液中加入KOH至饱和也可制得高铁酸钾( )固体,请解释其原因
)固体,请解释其原因___________ 。
(4)高铁酸钾能用于处理饮用水的原因?___________ 、___________ 。
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(5)含氰废水中的 有剧毒。在微生物的作用下,
有剧毒。在微生物的作用下, 能被氧气氧化成
能被氧气氧化成 同时生成
同时生成 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(6)试分析 反应中,被
反应中,被 氧化的P的物质的量为
氧化的P的物质的量为___________ 。
I.高铁酸钾(
 )是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
)是一种新型绿色消毒剂,具有强氧化性,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。(1)干法制备高铁酸钾时,先制备得到
 ,反应为:
,反应为: ,该反应的氧化产物是
,该反应的氧化产物是 转移电子数目为
转移电子数目为(2)湿法制备高铁酸钾(
 )的反应体系中有六种数粒:
)的反应体系中有六种数粒: 、
、 、
、 、
、 、
、 、
、 写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:
写出并配平湿法制高铁酸钾的离子反应方程式并用单线桥表示出电子转移的方向和数目:(3)低温下,在高铁酸钠溶液中加入KOH至饱和也可制得高铁酸钾(
 )固体,请解释其原因
)固体,请解释其原因(4)高铁酸钾能用于处理饮用水的原因?
Ⅱ.对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(5)含氰废水中的
 有剧毒。在微生物的作用下,
有剧毒。在微生物的作用下, 能被氧气氧化成
能被氧气氧化成 同时生成
同时生成 ,该反应的离子方程式为
,该反应的离子方程式为(6)试分析
 反应中,被
反应中,被 氧化的P的物质的量为
氧化的P的物质的量为
您最近一年使用:0次
【推荐1】碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛。完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。写出该反应的化学方程式_____ 。
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是__________________________________ 。
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2 + Hg=Cu2HgI4(玫瑰红)+ 2Cu,产物Cu2HgI4中Cu元素显____ 价。当有1 molCu2I2参与反应时,转移电子____ mol。
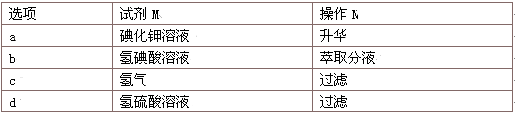
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是_____ (选填编号)
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。写出该反应的化学方程式
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2 + Hg=Cu2HgI4(玫瑰红)+ 2Cu,产物Cu2HgI4中Cu元素显
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.电解质溶液导电的能力的强弱主要由自由移动的离子的浓度的大小决定,离子浓度越大,导电能力越强,向一定体积的稀硫酸中逐滴加入氢氧化钡溶液,反应混合液的导电能力随时间变化的曲线如图所示。

(1)ac段发生的反应的离子方程式为:_________ 。
(2)下列说法正确的是_________。
Ⅱ. 是国际公认的高效安全杀菌消毒剂,工业制备
是国际公认的高效安全杀菌消毒剂,工业制备 的反应原理如下:
的反应原理如下:
(3)该反应中,氧化产物是_________ (填化学式),还原剂是_________ (填化学式),依据氧化还原反应规律判断,氧化性强弱为
_________  (填>、<或=)。
(填>、<或=)。
(4)亚氯酸钠 是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:
是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:

请将流程中反应①的离子方程式中所缺的物质补充完整并配平:_________ 。

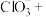

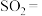


 _________
_________

(1)ac段发生的反应的离子方程式为:
(2)下列说法正确的是_________。
| A.b处溶液呈碱性,d处溶液呈酸性 |
B.c处主要成分是 和 和 |
| C.c时刻溶液的导电能力约为零,说明溶液中几乎没有自由移动的离子 |
| D.ce段溶液的导电能力不断增大,主要是由于过量的氢氧化钡电离出的离子导电 |
Ⅱ.
 是国际公认的高效安全杀菌消毒剂,工业制备
是国际公认的高效安全杀菌消毒剂,工业制备 的反应原理如下:
的反应原理如下:
(3)该反应中,氧化产物是

 (填>、<或=)。
(填>、<或=)。(4)亚氯酸钠
 是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:
是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如下:
请将流程中反应①的离子方程式中所缺的物质补充完整并配平:

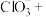

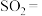


 _________
_________
您最近一年使用:0次
【推荐3】Ⅰ.高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,且无二次污染。
①K2FeO4在净水过程中可转化为Fe(OH)3胶体而吸附杂质,Fe(OH)3胶体粒子的直径大小范围是_______________ 。
②K2FeO4中Fe为+6价,具有强氧化性,盐酸中加入少量K2FeO4固体,产生黄绿色气体。该反应的化学方程式是________ 。
③K2FeO4是否具有还原性?__________ (填“有”或“没有”)。
Ⅱ.Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
① 用单线桥标出电子转移的方向和数目______ 。
② 此反应中氧化剂与还原剂的质量之比为________ 。
Ⅲ.已知常温下在溶液中可发生如下两个反应: ;
; 。由此可以确定
。由此可以确定 、
、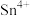 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是____________ 。
①K2FeO4在净水过程中可转化为Fe(OH)3胶体而吸附杂质,Fe(OH)3胶体粒子的直径大小范围是
②K2FeO4中Fe为+6价,具有强氧化性,盐酸中加入少量K2FeO4固体,产生黄绿色气体。该反应的化学方程式是
③K2FeO4是否具有还原性?
Ⅱ.Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
① 用单线桥标出电子转移的方向和数目
② 此反应中氧化剂与还原剂的质量之比为
Ⅲ.已知常温下在溶液中可发生如下两个反应:
 ;
; 。由此可以确定
。由此可以确定 、
、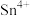 、
、 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】小组同学探究+3价铬元素和+6价铬元素的相互转化。
资料: (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (砖红色,难溶于水)
(砖红色,难溶于水)
实验Ⅰ:向 溶液中滴入
溶液中滴入 溶液,无明显变化,得到溶液a,取少量溶液a,加入
溶液,无明显变化,得到溶液a,取少量溶液a,加入 溶液,未观察到砖红色沉淀。
溶液,未观察到砖红色沉淀。
实验Ⅱ:向溶液a中加入 溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为
溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为 ,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的
,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的 约为3,再加入
约为3,再加入 溶液,有砖红色沉淀生成。
溶液,有砖红色沉淀生成。
(1)实验Ⅱ中加入稀硫酸的目的是___________ 。
(2)甲同学认为实验Ⅱ中溶液变黄生成 的原因是
的原因是 将+3价铬元素氧化为
将+3价铬元素氧化为 ,乙同学认为该说法不严谨。乙的理由是
,乙同学认为该说法不严谨。乙的理由是___________ 。
(3)对比实验Ⅰ和Ⅱ,小组同学研究碱性环境对+3价铬元素或 性质的影响。
性质的影响。
①提出假设:
假设a:碱性增强, 的氧化性增强
的氧化性增强
假设b:___________ 。
② 参与的电极反应式是
参与的电极反应式是___________ ,据此分析,假设a不成立。
实验Ⅲ:向实验Ⅱ中的黄色溶液中加入稀硫酸,溶液变为橙色,再加入 溶液,溶液最终变为绿色,有气泡生成。
溶液,溶液最终变为绿色,有气泡生成。
(4)实验Ⅲ中溶液由橙色变为绿色的离子方程式是___________ 。
(5)综上, 在+3价铬元素和+6价铬元素相互转化中的作用是
在+3价铬元素和+6价铬元素相互转化中的作用是___________ 。
资料:
 (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (砖红色,难溶于水)
(砖红色,难溶于水)实验Ⅰ:向
 溶液中滴入
溶液中滴入 溶液,无明显变化,得到溶液a,取少量溶液a,加入
溶液,无明显变化,得到溶液a,取少量溶液a,加入 溶液,未观察到砖红色沉淀。
溶液,未观察到砖红色沉淀。实验Ⅱ:向溶液a中加入
 溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为
溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为 ,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的
,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的 约为3,再加入
约为3,再加入 溶液,有砖红色沉淀生成。
溶液,有砖红色沉淀生成。(1)实验Ⅱ中加入稀硫酸的目的是
(2)甲同学认为实验Ⅱ中溶液变黄生成
 的原因是
的原因是 将+3价铬元素氧化为
将+3价铬元素氧化为 ,乙同学认为该说法不严谨。乙的理由是
,乙同学认为该说法不严谨。乙的理由是(3)对比实验Ⅰ和Ⅱ,小组同学研究碱性环境对+3价铬元素或
 性质的影响。
性质的影响。①提出假设:
假设a:碱性增强,
 的氧化性增强
的氧化性增强假设b:
②
 参与的电极反应式是
参与的电极反应式是实验Ⅲ:向实验Ⅱ中的黄色溶液中加入稀硫酸,溶液变为橙色,再加入
 溶液,溶液最终变为绿色,有气泡生成。
溶液,溶液最终变为绿色,有气泡生成。(4)实验Ⅲ中溶液由橙色变为绿色的离子方程式是
(5)综上,
 在+3价铬元素和+6价铬元素相互转化中的作用是
在+3价铬元素和+6价铬元素相互转化中的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据信息和要求书写相应的方程式。
(1)已知 为酸性氧化物,可与水反应生成磷酸(
为酸性氧化物,可与水反应生成磷酸(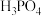 ),写出
),写出 与NaOH溶液反应的化学方程式:
与NaOH溶液反应的化学方程式:_______ 。
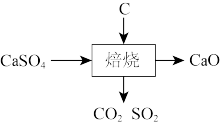
(2)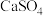 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:_______ 。
(3)以 为原料可在加热熔融条件下可以制取
为原料可在加热熔融条件下可以制取 。该反应中包含的所有物质为MnO2、
。该反应中包含的所有物质为MnO2、 、KCl、KOH、
、KCl、KOH、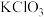 、
、 。写出该反应的化学方程式
。写出该反应的化学方程式_______ 。
(4)已知硫化亚铁(FeS)为难溶硫化物,在弱碱性溶液中,FeS与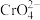 反应生成
反应生成 、
、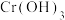 和单质S,其离子方程式为
和单质S,其离子方程式为_______ 。
(5)写出 溶液与过量
溶液与过量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(1)已知
 为酸性氧化物,可与水反应生成磷酸(
为酸性氧化物,可与水反应生成磷酸(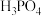 ),写出
),写出 与NaOH溶液反应的化学方程式:
与NaOH溶液反应的化学方程式:(2)
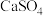 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
(3)以
 为原料可在加热熔融条件下可以制取
为原料可在加热熔融条件下可以制取 。该反应中包含的所有物质为MnO2、
。该反应中包含的所有物质为MnO2、 、KCl、KOH、
、KCl、KOH、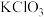 、
、 。写出该反应的化学方程式
。写出该反应的化学方程式(4)已知硫化亚铁(FeS)为难溶硫化物,在弱碱性溶液中,FeS与
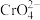 反应生成
反应生成 、
、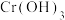 和单质S,其离子方程式为
和单质S,其离子方程式为(5)写出
 溶液与过量
溶液与过量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次



