利用下列装置不能达到相应目的的是


| A.①测定中和反应反应热 | B.②测定 溶液的 溶液的 |
C.③电解 溶液制备金属 溶液制备金属 | D.④牺牲阳极法保护钢铁桥墩 |
更新时间:2024-02-22 19:54:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在新制氯水中存在多种分子和离子,下列实验现象和结论一致且正确的是
| A.新制氯水使红色花瓣褪色,说明Cl2有漂白性 |
| B.向新制氯水中滴加紫色石蕊溶液后,溶液先变红后马上褪色,说明氯水有酸性和漂白性 |
| C.向新制氯水中加入NaOH溶液,氯水黄绿色消失,说明有HClO存在 |
| D.光照新制氯水有气泡逸出,该气体一定是Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】表述Ⅰ与表述Ⅱ中,两者之间因果关系错误 的是
| 选项 | 表述Ⅰ | 表述Ⅱ |
| A | 金属钠保存在煤油中,以隔绝空气 | 常温下,金属钠在空气中会发生反应 |
| B | 用 溶液腐蚀印刷电路板 溶液腐蚀印刷电路板 |  溶液能与 溶液能与 反应 反应 |
| C | 将干燥的氯气通入盛有红色鲜花的集气瓶中,鲜花褪色 | 干燥的氯气具有漂白性 |
| D | 氢氧化铝可用于治疗胃酸过多 | 氢氧化铝可与盐酸反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列叙述、解释或结论正确的是
| 选项 | 叙述 | 解释或结论 |
| A | SO2通入氢氧化钠的酚酞溶液中,溶液褪色 | SO2具有漂白作用 |
| B | 向NaBr溶液中加入过量氯水,再加入淀粉KI溶液,溶液变蓝 | 非金属性:Cl>Br>I |
| C | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
| D | 室温下,用pH试纸分别测定浓度0.1mol·L-1NaClO溶液、0.1mol·L−1NaF溶液的pH | 比较HClO和HF溶液的酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】分别取40mL的0.50mol/L盐酸与40mL0.55mol/L氢氧化钠溶液进行中和热的测定。下列说法错误的是
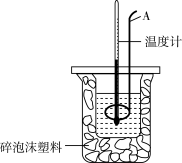

| A.稍过量的氢氧化钠是确保盐酸完全反应 |
| B.仪器A的名称是环形玻璃搅拌棒 |
| C.在实验过程中,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度 |
| D.用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,结果也是正确的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】课本测定中和反应反应热的实验中,下列说法正确的是
| A.使用金属搅拌器是为了加快反应速率,减小实验误差 |
B.为了准确测定反应混合溶液的温度,实验中 溶液迅速一次倒入装有盐酸的量热计内筒中,并立即盖上杯盖 溶液迅速一次倒入装有盐酸的量热计内筒中,并立即盖上杯盖 |
C.用 溶液分别与 溶液分别与 的盐酸、醋酸溶液反应,若所取的溶液体积都相等,则测得的中和反应反应热 的盐酸、醋酸溶液反应,若所取的溶液体积都相等,则测得的中和反应反应热 相同 相同 |
| D.在测定中和反应反应热的实验中,需要使用的仪器有天平、量筒、量热计、滴定管、温度计、搅拌器 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列有关实验内容、实验装置和对应的实验目的均正确的是
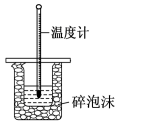 |  | 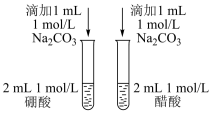 | 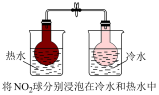 |
| A.可用于测定中和热 | B.验证CuCl2对双氧水分解的催化作用 | C.比较醋酸和硼酸的酸性强弱 | D.比较不同温度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】当前,受技术封锁的影响,我国芯片发展急需自我突破,而芯片的生产不仅仅是高纯硅的制备,其中还涉及到大量元素化合物之间的反应,如:①Si(粗)+2Cl2 SiCl4②TiCl4+2Mg
SiCl4②TiCl4+2Mg Ti+2MgCl2,下列关于元素化合物知识的说法正确的是
Ti+2MgCl2,下列关于元素化合物知识的说法正确的是
 SiCl4②TiCl4+2Mg
SiCl4②TiCl4+2Mg Ti+2MgCl2,下列关于元素化合物知识的说法正确的是
Ti+2MgCl2,下列关于元素化合物知识的说法正确的是| A.金刚石、硅单质是由碳原子、硅原子构成的物质,而碳化硅是由碳化硅分子构成的物质 |
| B.新制氯水具有漂白性,与活性炭、二氧化硫的漂白原理相同 |
| C.镁是国防金属,工业上采用电解熔融氧化镁的方法获得纯净的镁单质 |
| D.TiO2也称为钛白,是常见的白色颜料,可采用加热TiCl4的水溶液后焙烧的方法制备 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.使元素的化合态转化成游离态的过程就是还原的过程 |
| B.金属冶炼的实质是金属元素被氧化 |
| C.电解熔融氧化铝时,每还原出1 kg铝,必有约111mol电子转移 |
| D.工业上常用电解NaCl水溶液的方法制取金属钠 |
您最近一年使用:0次



