判断化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是
A.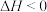 或 或 的反应一定能自发进行 的反应一定能自发进行 |
B.反应 能否自发进行与温度有关 能否自发进行与温度有关 |
C. 在不同状态时的熵值: 在不同状态时的熵值: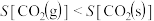 |
D.反应 的 的 |
更新时间:2024-02-13 10:27:08
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法或表示方法中正确的是
| A.由C(金刚石)=C(石墨) ΔH=-1.9kJ·mol-1可知,金刚石比石墨稳定 |
| B.相同条件下,1molCH4(g)的熵大于lmolH2(g) |
| C.在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则表示氢气燃烧热的热化学方程式为: 2H2(g)+O2(g)=2H2O(1) ΔH=-571.6kJ·mol-1 |
D.CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0,低温有利于该反应的自发进行 CO(g)+3H2(g) ΔH>0,低温有利于该反应的自发进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】298K时,反应2Al2O3(s)+3C(s)=4Al(s)+3CO2(g)的ΔH=+2171kJ·mol-1 ΔS=+635.5J·mol-1·K-1,则下列说法正确的是
| A.该反应是放热反应 | B.ΔS>0表明该反应是熵增反应 |
| C.吸热反应都不能自发进行 | D.不能确定该反应能否自发进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
| A.放热或熵减小均有利于反应的正向自发进行 |
| B.ΔH>0,ΔS<0的反应在任何温度下均能正向自发进行 |
| C.2H2O2(aq)==2H2O(l)+O2(g) ΔH=-189.3 kJ· mol−1,任何温度下均可正向自发进行 |
| D.向水中加入NH4NO3固体,溶液温度降低,可说明铵盐水解是吸热的 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】自由能的变化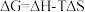 是判断反应进行方向的复合判据。
是判断反应进行方向的复合判据。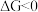 时,反应能自发进行。已知工业上常利用
时,反应能自发进行。已知工业上常利用 和
和 来制备水煤气,化学方程式为
来制备水煤气,化学方程式为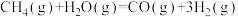 ,
, 则下列说法正确的是
则下列说法正确的是
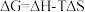 是判断反应进行方向的复合判据。
是判断反应进行方向的复合判据。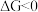 时,反应能自发进行。已知工业上常利用
时,反应能自发进行。已知工业上常利用 和
和 来制备水煤气,化学方程式为
来制备水煤气,化学方程式为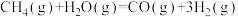 ,
, 则下列说法正确的是
则下列说法正确的是A. ,低温下该反应能自发进行 ,低温下该反应能自发进行 | B. ,高温下该反应能自发进行 ,高温下该反应能自发进行 |
C. ,低温下该反应能自发进行 ,低温下该反应能自发进行 | D. ,高温下该反应能自发进行 ,高温下该反应能自发进行 |
您最近一年使用:0次



