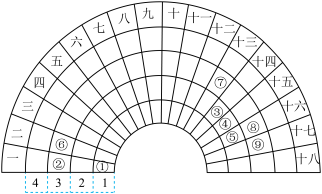
现代元素周期表是在门捷列夫首创的元素周期表基础上完善的。下图是扇形元素周期表,表中的“1、2、3、4”表示原子的核外电子层数,与现代元素周期表中的周期对应;“一、二、三……”与现代元素周期表中的族对应,共18列。①~⑨为现代元素周期表中1~18号元素。请按要求回答下列问题:_______ 。
(2)元素原子半径:②_______ (填“>”“<”或“=”,下同)⑥,比较最简单氢化物的热稳定性:⑤_______ ⑧。
(3)元素⑥形成的离子的结构示意图是_______ ,由元素⑥和元素⑨组成的常见化合物中所含化学键类型为_______ 。
(4)元素②⑥⑦的最高价氧化物对应的水化物中,碱性最强的是_______ (填化学式);写出元素⑦的最高价氧化物对应的水化物与元素⑨的最高价氧化物对应的水化物反应的离子方程式:_______ 。
(5)由①和⑤构成的原子个数比为1∶1的化合物与⑧的氢化物反应的化学方程式为_______ 。
(2)元素原子半径:②
(3)元素⑥形成的离子的结构示意图是
(4)元素②⑥⑦的最高价氧化物对应的水化物中,碱性最强的是
(5)由①和⑤构成的原子个数比为1∶1的化合物与⑧的氢化物反应的化学方程式为
更新时间:2024-02-14 19:53:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填空:
(1)有下列微粒或物质:① O、
O、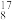 O、
O、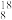 O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥
O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥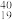 K、
K、 Ca、
Ca、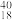 Ar,回答下列问题:
Ar,回答下列问题:
a.互为同位素的是_______ ;
b.互为同素异形体的是_______ ;
c.上述微粒中出现的核素符号有_______ 种;
d.由①和⑤中的微粒能结合成水,可得相对分子质量不同的水分子种数为_______ 种,相对分子质量最大的是_______ (写化学式)。
(2)相同质量的 H2
H2 O与
O与 H2
H2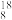 O所含中子数之比为
O所含中子数之比为_______ 。
(3)元素周期表中,甲、乙分别是第五周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为_______ 。
(4)某中学化学兴趣小组同学为探究元素周期律,设计了如下实验。利用下图所示装置可以验证元素的非金属性的变化规律。
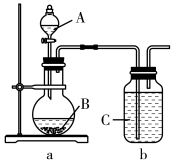
甲同学设计实验:A为硝酸,B为石灰石,C为硅酸钠溶液。实验现象:a装置中圆底烧瓶中产生大量气泡,b装置中出现浑浊或白色沉淀。
①甲同学由实验得出酸性由强到弱的顺序为:_______ 。
②乙同学分析甲同学设计的实验方案,认为该方案存在不足之处,请分析乙同学的理由_______ ,并提出改进实验方案_______ 。
(1)有下列微粒或物质:①
 O、
O、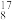 O、
O、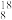 O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥
O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥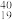 K、
K、 Ca、
Ca、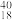 Ar,回答下列问题:
Ar,回答下列问题:a.互为同位素的是
b.互为同素异形体的是
c.上述微粒中出现的核素符号有
d.由①和⑤中的微粒能结合成水,可得相对分子质量不同的水分子种数为
(2)相同质量的
 H2
H2 O与
O与 H2
H2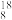 O所含中子数之比为
O所含中子数之比为(3)元素周期表中,甲、乙分别是第五周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为
(4)某中学化学兴趣小组同学为探究元素周期律,设计了如下实验。利用下图所示装置可以验证元素的非金属性的变化规律。

甲同学设计实验:A为硝酸,B为石灰石,C为硅酸钠溶液。实验现象:a装置中圆底烧瓶中产生大量气泡,b装置中出现浑浊或白色沉淀。
①甲同学由实验得出酸性由强到弱的顺序为:
②乙同学分析甲同学设计的实验方案,认为该方案存在不足之处,请分析乙同学的理由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
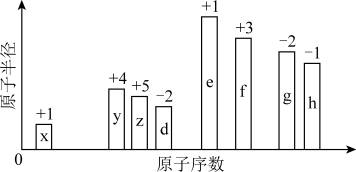
(1)元素x在元素周期表中的位置是___________ 。
(2)元素x、z可形成含10电子的分子甲,其结构式为___________ 。在微电子工业中,甲的水溶液可作刻蚀剂 的消除剂,所得产物不污染环境,其化学方程式是
的消除剂,所得产物不污染环境,其化学方程式是___________ 。
(3)x分别与yzd形成的化合物中,最稳定的物质是___________ (填化学式)
(4)元素d.e形成的简单离子,半径较大的离子是___________ (填离子符号)。
(5)元素g、h的最高价氧化物的水化物的酸性较强的是___________ (填化学式)。
(6)元素e、f的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(7)化合物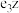 遇水反应生成氨气(
遇水反应生成氨气( )和一种强碱,反应的化学方程式为
)和一种强碱,反应的化学方程式为___________ 。
(8)NaH的电子式___________ 。

(1)元素x在元素周期表中的位置是
(2)元素x、z可形成含10电子的分子甲,其结构式为
 的消除剂,所得产物不污染环境,其化学方程式是
的消除剂,所得产物不污染环境,其化学方程式是(3)x分别与yzd形成的化合物中,最稳定的物质是
(4)元素d.e形成的简单离子,半径较大的离子是
(5)元素g、h的最高价氧化物的水化物的酸性较强的是
(6)元素e、f的最高价氧化物的水化物之间发生反应的离子方程式为
(7)化合物
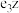 遇水反应生成氨气(
遇水反应生成氨气( )和一种强碱,反应的化学方程式为
)和一种强碱,反应的化学方程式为(8)NaH的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知 元素原子的核电荷数小于18,最外层电子数等于电子层数,且比最内层电子数多1。回答下列问题:
元素原子的核电荷数小于18,最外层电子数等于电子层数,且比最内层电子数多1。回答下列问题:
(1) 元素的原子结构示意图为
元素的原子结构示意图为______ 。
(2) 的最高价氧化物对应的水化物属于
的最高价氧化物对应的水化物属于______ 。(填“酸”“碱”或“两性氢氧化物”)。
(3) 的单质与
的单质与 溶液反应的化学方程式为
溶液反应的化学方程式为____________________________________ 。
(4) 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 溶液反应的离子方程式为
溶液反应的离子方程式为______________________ 。
 元素原子的核电荷数小于18,最外层电子数等于电子层数,且比最内层电子数多1。回答下列问题:
元素原子的核电荷数小于18,最外层电子数等于电子层数,且比最内层电子数多1。回答下列问题:(1)
 元素的原子结构示意图为
元素的原子结构示意图为(2)
 的最高价氧化物对应的水化物属于
的最高价氧化物对应的水化物属于(3)
 的单质与
的单质与 溶液反应的化学方程式为
溶液反应的化学方程式为(4)
 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
(1)元素⑨在周期表中的位置___________ 。
(2)在0~⑨元素中,某种元素的氧化物是两性氧化物,请写出该氧化物与氢氧化钠反应的化学方程式___________ 。
(3)请比较④⑨两元素的氢化物的稳定性___________ (用氢化物的分子式表示)。
(4)元素⑨的单质可使湿润的淀粉 试纸变蓝,请写出离子方程式
试纸变蓝,请写出离子方程式___________ 。
(5)将⑤⑥⑦三种元素的离子按半径从大到小排序___________ (用元素符号表示)。
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素⑨在周期表中的位置
(2)在0~⑨元素中,某种元素的氧化物是两性氧化物,请写出该氧化物与氢氧化钠反应的化学方程式
(3)请比较④⑨两元素的氢化物的稳定性
(4)元素⑨的单质可使湿润的淀粉
 试纸变蓝,请写出离子方程式
试纸变蓝,请写出离子方程式(5)将⑤⑥⑦三种元素的离子按半径从大到小排序
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请回答有关问题:
(1)④和⑦的元素符号是_________ 和_________ ;
(2)表中8种元素中,金属性最强的元素的元素符号是_________ ,非金属性最强的元素的元素符号是________ 。
(3)表中能形成两性氢氧化物的元素名称是________________ ,写出该元素的氢氧化物与③的最高价氧化物对应水化物反应的离子反应方程式:________________________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ① | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④和⑦的元素符号是
(2)表中8种元素中,金属性最强的元素的元素符号是
(3)表中能形成两性氢氧化物的元素名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用周期表中特殊位置的短周期元素填空
(1)族序数等于周期数的元素:___________ ;
(2)族序数等于周期数2倍的元素:___________ ;
(3)族序数等于周期数3倍的元素:___________ ;
(4)周期数是族序数2倍的元素:___________ ;
(5)周期数是族序数3倍的元素是:___________ ;
(6)最高正价不等于族序数的元素是:___________ 。
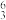 Li、
Li、 Li、
Li、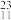 Na、
Na、 Mg、
Mg、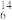 C、
C、 N中,
N中,
(7)___________ 和___________ 互为同位素;
(8)___________ 和___________ 的质量数相等,但不能互称同位素;
(1)族序数等于周期数的元素:
(2)族序数等于周期数2倍的元素:
(3)族序数等于周期数3倍的元素:
(4)周期数是族序数2倍的元素:
(5)周期数是族序数3倍的元素是:
(6)最高正价不等于族序数的元素是:
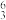 Li、
Li、 Li、
Li、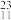 Na、
Na、 Mg、
Mg、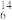 C、
C、 N中,
N中,(7)
(8)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】周期表前20号元素中,某两种元素的原子序数相差3,周期数相差1,它们形成化合物时原子数之比为1:2。写出这些化合物的化学式__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】人体必需的一些元素在周期表中的分布情况如下:

(1)请在上图中画出金属与非金属的分界线_______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为_______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为_______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确的是_______ (填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

(6)铬是胰岛素不可缺少的辅助成分,但食用不当也会带来很大的危害。六价铬的化合物有剧毒,所以要对Cr(VI)(罗马数字表示元素的化合价,下同)废水进行化学处理,可转化为重要产品磁性铁铬氧体(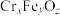 ):先向含
):先向含 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分 )并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
①写出 在酸性条件下被
在酸性条件下被 还原为
还原为 的离子方程式:
的离子方程式:_______ 。
②若处理含1mol (不考虑其他含铬微粒)的污水时恰好消耗10mol
(不考虑其他含铬微粒)的污水时恰好消耗10mol ,则当铁铬氧体中
,则当铁铬氧体中 时,铁铬氧体的化学式为
时,铁铬氧体的化学式为_______ 。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确的是
| A | B | C | D |
| HCl |  |  |  |
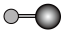 |  | 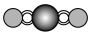 | 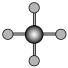 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
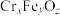 ):先向含
):先向含 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分 )并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。①写出
 在酸性条件下被
在酸性条件下被 还原为
还原为 的离子方程式:
的离子方程式:②若处理含1mol
 (不考虑其他含铬微粒)的污水时恰好消耗10mol
(不考虑其他含铬微粒)的污水时恰好消耗10mol ,则当铁铬氧体中
,则当铁铬氧体中 时,铁铬氧体的化学式为
时,铁铬氧体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C、D是原子序数依次增大的短周期主族元素。A元素的单质是一种清洁燃料,B元素的原子最外层电子数为次外层电子数的3倍,C元素的+1价离子与B元素的简单离子的电子层结构相同,D的周期数等于其主族序数。判断:
(1)A为___________ (填元素符号),D的原子结构示意图为___________ 。
(2)对这四种元素的原子半径从小到大排序___________ (填元素符号)。
(3)B元素在元素周期表中的位置为___________ ,其氢化物属于___________ (填下列字母)。
A.非电解质 B.共价化合物 C.电解质 D.离子化合物
(4)C的最高价氧化物的水化物所含化学键的类型为___________ ,其与D的单质发生反应的化学方程式为___________ 。
(1)A为
(2)对这四种元素的原子半径从小到大排序
(3)B元素在元素周期表中的位置为
A.非电解质 B.共价化合物 C.电解质 D.离子化合物
(4)C的最高价氧化物的水化物所含化学键的类型为
您最近一年使用:0次



