下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
(1)元素⑨在周期表中的位置___________ 。
(2)在0~⑨元素中,某种元素的氧化物是两性氧化物,请写出该氧化物与氢氧化钠反应的化学方程式___________ 。
(3)请比较④⑨两元素的氢化物的稳定性___________ (用氢化物的分子式表示)。
(4)元素⑨的单质可使湿润的淀粉 试纸变蓝,请写出离子方程式
试纸变蓝,请写出离子方程式___________ 。
(5)将⑤⑥⑦三种元素的离子按半径从大到小排序___________ (用元素符号表示)。
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素⑨在周期表中的位置
(2)在0~⑨元素中,某种元素的氧化物是两性氧化物,请写出该氧化物与氢氧化钠反应的化学方程式
(3)请比较④⑨两元素的氢化物的稳定性
(4)元素⑨的单质可使湿润的淀粉
 试纸变蓝,请写出离子方程式
试纸变蓝,请写出离子方程式(5)将⑤⑥⑦三种元素的离子按半径从大到小排序
更新时间:2023/04/17 21:59:53
|
相似题推荐
【推荐1】Ⅰ.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的________ 区元素,其价电子排布式是________ 。
(2)基态Fe原子核外电子排布式为________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的________ 区(用符号填空),原子序数最大的在周期表位置________ 。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为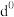 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
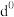 或
或 排布时,无颜色,为
排布时,无颜色,为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为__________ 。
(2)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与Na2O2的结构和化学性质相似,其溶液显黄色。H的电子式为______ 。
(3)化学家发现一种化学式为A4B4的化合物,由均带一个电荷的阴、阳离子组成,则该阴、阳离子为_______ 。
(4)B2A4C3是一种常见的炸药,其在常温下撞击时会生成一种气体(B2C)和一种常见液体,该反应的化学力程式为______________ 。8g该物质反应转移的电子数目为________ 。
(5)下列事实能说明元素F的非金属性比元素E的非金属性强的是______ 。
a.元素F形成的单质比元素E形成的单质的熔点低
b.F和E两元素的简单氢化物受热分解,前者的分解温度高
c.F2通入到D2E的溶液中出现浑浊
(1)E在元素周期表中的位置为
(2)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与Na2O2的结构和化学性质相似,其溶液显黄色。H的电子式为
(3)化学家发现一种化学式为A4B4的化合物,由均带一个电荷的阴、阳离子组成,则该阴、阳离子为
(4)B2A4C3是一种常见的炸药,其在常温下撞击时会生成一种气体(B2C)和一种常见液体,该反应的化学力程式为
(5)下列事实能说明元素F的非金属性比元素E的非金属性强的是
a.元素F形成的单质比元素E形成的单质的熔点低
b.F和E两元素的简单氢化物受热分解,前者的分解温度高
c.F2通入到D2E的溶液中出现浑浊
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:_____ (填具体化学用语,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是:_____ 。
(3)最高价氧化物是两性氧化物的元素是___ ;写出它的氧化物与氢氧化钠反应的离子方程式__ 。
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:______ 。
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因________ 。
(6)用结构式表示元素①与③形成的化合物____ ,该化合物在固体时俗称___ ,属于____ 晶体,指出它的一种用途___ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因
(6)用结构式表示元素①与③形成的化合物
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,请回答有关问题:
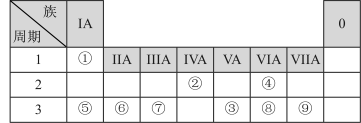
请按要求回答下列问题:
(1)元素⑦的原子结构示意图______________________ 。由②、④两种元素组成的化合物是___________ 化合物(填“共价”或“离子”)
(2)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式__________________ ;一种离子化合物的化学式_________
(3)④⑤⑥三种元素的离子半径由大到小的顺序是____________ (填离子符号)。
(4)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是________ (填化学式)。
(5)元素③的气态氢化物和元素⑧的气态氢化物更稳定的是___________ (填化学式)。
(6)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为_________________________________________

请按要求回答下列问题:
(1)元素⑦的原子结构示意图
(2)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式
(3)④⑤⑥三种元素的离子半径由大到小的顺序是
(4)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是
(5)元素③的气态氢化物和元素⑧的气态氢化物更稳定的是
(6)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化合物Q用作铝、铜和铝合金焊接助熔剂,结构如图所示, X、Y、Z、W为原子序数依次增大的主族元素,最外层电子数均为奇数且质子数之和为22。则X、Y、Z、W分别是________________ (填元素符号)。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】据报道,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将给量子计算机的研究带来重大突破。已知铷是37号元素。根据相关知识回答下列问题:
(1)铷(Rb)位于元素周期表的第___ 周期___ 族。
(2)关于铷的结构和性质判断正确的是___ (填序号)。
①与水反应比钠剧烈
②原子半径比钠的小
③氧化物暴露在空气中易吸收CO2
④阳离子最外层电子数和镁离子最外层电子数相同
⑤是还原剂
(3)现有铷和另一种碱金属形成的合金50g,当它与足量水反应时,放出标准状况下的氢气22.4L,这种碱金属可能是___ (填字母)。
A.Li B.Na C.K D.Cs
(1)铷(Rb)位于元素周期表的第
(2)关于铷的结构和性质判断正确的是
①与水反应比钠剧烈
②原子半径比钠的小
③氧化物暴露在空气中易吸收CO2
④阳离子最外层电子数和镁离子最外层电子数相同
⑤是还原剂
(3)现有铷和另一种碱金属形成的合金50g,当它与足量水反应时,放出标准状况下的氢气22.4L,这种碱金属可能是
A.Li B.Na C.K D.Cs
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下列为元素周期表中的一部分,用化学用语回答下列问题。
(1)③的原子结构示意图为___________ ;
(2)11种元素中,化学性质最不活泼的是___________ ,原子半径最小的是___________ ,金属性最强的是___________ ,非金属性最强的是___________ 。
(3)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(4)②③④中形成的简单离子半径由大到小的顺序是___________ 。
(5)元素⑦的简单氢化物电子式为___________ 。
(6)①和⑨两元素形成化合物中化学键的类型为___________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为___________ 。
(7)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(8)⑧⑨⑪三种元素形成的气态氢化物中,最稳定的是___________ ,沸点___________ (填化学式)更高,原因是___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)③的原子结构示意图为
(2)11种元素中,化学性质最不活泼的是
(3)①②⑤中,最高价氧化物的水化物,碱性最强的是
(4)②③④中形成的简单离子半径由大到小的顺序是
(5)元素⑦的简单氢化物电子式为
(6)①和⑨两元素形成化合物中化学键的类型为
(7)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(8)⑧⑨⑪三种元素形成的气态氢化物中,最稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大。短周期元素中C的原子半径最大,B、E同族,E的最外层电子数是电子层数的2倍,A的最高价氧化物水化物为H2AO3,D是地壳中含量最高的金属元素。
(1)A的元素符号是_______ ,C2B2的电子式为_______ 。
(2)B、C、D、F的离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)E和F相比,非金属性强的是_______ (用元素符号表示),下列事实能证明这一结论的是_______ (用符号填空)。
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为_______ (填化学式)。
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为_________________________ 。
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为_______ , pH=10的乙溶液中由水电离产生的c(OH-)=_______ mol·L-1。
(1)A的元素符号是
(2)B、C、D、F的离子半径由大到小的顺序是
(3)E和F相比,非金属性强的是
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ、已知34Se的原子结构示意图如图所示,回答下列问题:

(1)Se在元素周期表中的位置是__________ 。
(2)由Se在周期表中的位置分析判断下列说法正确的是__________ 。
A.热稳定性:PH3>H2S>H2Se B.还原性:H2Se>HBr>HCl
C.离子半径:Se2->Cl->K+ D.酸性:HClO3>HBrO3>H2SeO3
Ⅱ、已知:X表示卤族元素
(1)HClO的电子式是__________ 。
(2)氯气通入Ca(OH)2可以制得漂白粉,反应的化学方程式为__________ 。
(3)共价键的极性随着两元素的非金属性差异增大而增强,HX共价键的极性由强到弱的顺序是__________ 。
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式__________ .

(1)Se在元素周期表中的位置是
(2)由Se在周期表中的位置分析判断下列说法正确的是
A.热稳定性:PH3>H2S>H2Se B.还原性:H2Se>HBr>HCl
C.离子半径:Se2->Cl->K+ D.酸性:HClO3>HBrO3>H2SeO3
Ⅱ、已知:X表示卤族元素
(1)HClO的电子式是
(2)氯气通入Ca(OH)2可以制得漂白粉,反应的化学方程式为
(3)共价键的极性随着两元素的非金属性差异增大而增强,HX共价键的极性由强到弱的顺序是
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式
您最近一年使用:0次



