随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
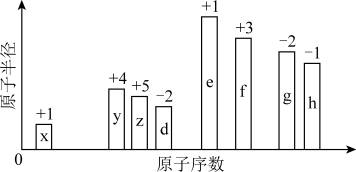
(1)元素x在元素周期表中的位置是___________ 。
(2)元素x、z可形成含10电子的分子甲,其结构式为___________ 。在微电子工业中,甲的水溶液可作刻蚀剂 的消除剂,所得产物不污染环境,其化学方程式是
的消除剂,所得产物不污染环境,其化学方程式是___________ 。
(3)x分别与yzd形成的化合物中,最稳定的物质是___________ (填化学式)
(4)元素d.e形成的简单离子,半径较大的离子是___________ (填离子符号)。
(5)元素g、h的最高价氧化物的水化物的酸性较强的是___________ (填化学式)。
(6)元素e、f的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(7)化合物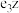 遇水反应生成氨气(
遇水反应生成氨气( )和一种强碱,反应的化学方程式为
)和一种强碱,反应的化学方程式为___________ 。
(8)NaH的电子式___________ 。

(1)元素x在元素周期表中的位置是
(2)元素x、z可形成含10电子的分子甲,其结构式为
 的消除剂,所得产物不污染环境,其化学方程式是
的消除剂,所得产物不污染环境,其化学方程式是(3)x分别与yzd形成的化合物中,最稳定的物质是
(4)元素d.e形成的简单离子,半径较大的离子是
(5)元素g、h的最高价氧化物的水化物的酸性较强的是
(6)元素e、f的最高价氧化物的水化物之间发生反应的离子方程式为
(7)化合物
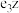 遇水反应生成氨气(
遇水反应生成氨气( )和一种强碱,反应的化学方程式为
)和一种强碱,反应的化学方程式为(8)NaH的电子式
更新时间:2024-01-14 18:43:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】2020年突如其来的“新冠病毒”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉、二氧化氯都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84“消毒液,可以说化学让生活更美好。
图为“84”消毒液说明书。
请回答下列问题。
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是_______ 。
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式_______ , 若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO 和NaClO3的混合液。当混合液中Cl-和 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为_______ 。
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目_______ 。
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐( ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是_______ (填字母)。
a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为: +FeS2+H+
+FeS2+H+ 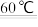 ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式_______ 。
图为“84”消毒液说明书。
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~ 60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1: 200水溶液餐饮具,瓜果等1: 100 水溶液 |
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式
 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐(
 ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为:
 +FeS2+H+
+FeS2+H+ 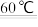 ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成_______ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______ 。
(1)钠在空气中燃烧生成
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则Al2O3是一种
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下列物质:①氢氧化钠溶液、②铝片、③碳酸钙、④偏铝酸钠溶液、⑤熔融的NaCl、⑥CO2气体、⑦碳酸氢钠、⑧盐酸;
(1)上述状态下能导电且属于电解质的是_________________ (填编号)
(2)写出碳酸氢钠在水溶液中的电离方程式______________________ ;
(3)写出铝片与氢氧化钠溶液反应的化学方程式__________________ ;
(4)写出碳酸氢钠与氢氧化钠溶液反应的离子方程式___________________________ ;
(5)写出将过量CO2气体通入偏铝酸钠溶液中,发生反应的离子方程式____________ 。
(1)上述状态下能导电且属于电解质的是
(2)写出碳酸氢钠在水溶液中的电离方程式
(3)写出铝片与氢氧化钠溶液反应的化学方程式
(4)写出碳酸氢钠与氢氧化钠溶液反应的离子方程式
(5)写出将过量CO2气体通入偏铝酸钠溶液中,发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.如图为元素周期表的一部分,请回答下列问题。

(1)图中阴影部分所示区域的元素称为_______ 元素,下列元素属于该区域的是_______ 。
A.Ba B.Mn C.I D.Rb
(2)下列说法不正确的是_______;
II.已知A、B、C、D、E、F六种短周期元素的原子半径和主要化合价如表:
(3)写出C元素在元素周期表中的位置_______ ;
(4)E和F的最高价氧化物的水化物相互反应的离子方程式为_______ ;
(5)以上元素的单质中还原性最强的是_______ (填化学式);
(6)上述某种元素其最高价氧化物的水化物与其气态氢化物相互反应的化学方程式_______ 。

(1)图中阴影部分所示区域的元素称为
A.Ba B.Mn C.I D.Rb
(2)下列说法不正确的是_______;
| A.最高正价与最低负价绝对值相等的元素一定处于IVA族 |
| B.图中①形成的最高价氧化物的水化物比③形成的最高价氧化物的水化物碱性强 |
| C.图中②的单质可与冷水剧烈反应 |
| D.同周期相邻主族元素的原子序数可能相差1、11或25 |
II.已知A、B、C、D、E、F六种短周期元素的原子半径和主要化合价如表:
| 元素代号 | A | B | C | D | E | F |
| 原子半径/nm | 0.074 | 0.075 | 0.077 | 0.160 | 0.186 | 0.143 |
| 主要化合价 |  |  、 、 |  、 、 |  |  |  |
(4)E和F的最高价氧化物的水化物相互反应的离子方程式为
(5)以上元素的单质中还原性最强的是
(6)上述某种元素其最高价氧化物的水化物与其气态氢化物相互反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯。目前Cl2O、ClO2、Cl2O7已能制取。
有关数据见下表:
完成下列填空:
(1)Cl2O是____ 酸的酸酐,Cl2O电子式为____________ 。
(2)下列能判断Cl和O两种元素非金属性强弱的是______ (选填编号)。
a.氧化氯的分子式 b.与金属反应得电子的数目
c.气态氢化物的稳定性 d.最高价氧化物对应水化物的酸性
(3)根据分子间作用力对沸点影响的变化规律:组成和结构相似的分子,其沸点随着相对分子质量的增大而升高,但上表中相对分子质量是Cl2O7>Cl2O>ClO2,其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是___________________________ 。
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2-)和氯酸盐,其离子方程式是________ ,氧化产物________ 。(填离子符号)
有关数据见下表:
| 化学式 | Cl2O | ClO2 | Cl2O7 |
| 相对分子质量 | 87 | 67.5 | 183 |
| 沸点/℃ | 2 | 9.7 | 81 |
完成下列填空:
(1)Cl2O是
(2)下列能判断Cl和O两种元素非金属性强弱的是
a.氧化氯的分子式 b.与金属反应得电子的数目
c.气态氢化物的稳定性 d.最高价氧化物对应水化物的酸性
(3)根据分子间作用力对沸点影响的变化规律:组成和结构相似的分子,其沸点随着相对分子质量的增大而升高,但上表中相对分子质量是Cl2O7>Cl2O>ClO2,其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2-)和氯酸盐,其离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硫、硒、碲的化合物在农药、石油工业、矿物开采、萃取及有机合成等领域的应用广泛。回答下列问题:
(1)基态Se原子的价层电子排布式为___________ 。
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
(3)类卤素 分子结构式为
分子结构式为___________ ,1mol 中含有π键的数目为
中含有π键的数目为___________ ,HSCN结构有两种,已知硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是___________ 。
(4)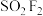 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
___________  (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是___________ 。
(1)基态Se原子的价层电子排布式为
(2)下列有关氧族元素单质及其化合物的性质说法正确的是___________。
A.氧族元素气态氢化物的稳定性按 、 、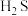 、 、 、 、 的顺序依次减弱 的顺序依次减弱 |
| B.其氢化物中的键长按O―H、S―H、Se―H、Te―H的顺序依次减小 |
C.其阴离子的还原性按 、 、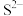 、 、 、 、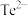 的顺序依次增强 的顺序依次增强 |
D.其最高价氧化物的水化物酸性按 、 、 、 、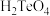 顺序依次增强 顺序依次增强 |
(3)类卤素
 分子结构式为
分子结构式为 中含有π键的数目为
中含有π键的数目为 )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸( ),其原因是
),其原因是(4)
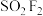 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是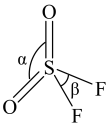

 (填“>”或“<”或“=”),其原因是
(填“>”或“<”或“=”),其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】一些元素在周期表中的分布情况如图:___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(3)Sn的价电子数为___________ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
(6)用电子式表示 的形成过程
的形成过程___________ 。
(7)在下列物质中:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是___________ ;既存在离子键又存在极性键的是___________ 。
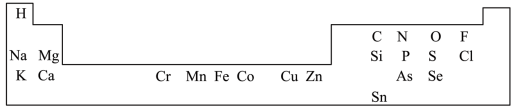
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序
(3)Sn的价电子数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
| A | B | C | D |
 |  |  |  |
|
|
|
|
| 直线形 | 直线形 | 直线形 | 平面正方形 |
| A.A | B.B | C.C | D.D |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
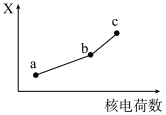
| A.若a、b、c表示ⅠA族金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示ⅦA族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)用电子式表示
 的形成过程
的形成过程(7)在下列物质中:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】土壤中的硝酸盐会被细菌分解。有一种细菌是利用土壤中的硫化物来分解硝酸盐,其主要化学反应原理是:
(1) 、
、 、
、 、O元素的原子半径从大到小的顺序是
、O元素的原子半径从大到小的顺序是_______ 。
(2)上述反应中的各物质属于共价化合物是_______ ;氧化剂是_______ 。氮气的电子式是_______ 。
(3)非金属性S_______ O(写“ ”或“
”或“ ”)。用一个化学方程式证明硫与氧的非金属性强弱:
”)。用一个化学方程式证明硫与氧的非金属性强弱:_______ 。
(4)配平上述反应方程式,并标出电子转移的方向和数目。_______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______

(1)
 、
、 、
、 、O元素的原子半径从大到小的顺序是
、O元素的原子半径从大到小的顺序是(2)上述反应中的各物质属于共价化合物是
(3)非金属性S
 ”或“
”或“ ”)。用一个化学方程式证明硫与氧的非金属性强弱:
”)。用一个化学方程式证明硫与氧的非金属性强弱:(4)配平上述反应方程式,并标出电子转移的方向和数目。
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
(1)⑦元素的离子半径__ S2-(填“>”或“<”),比较③与⑥的氢化物,___ 更稳定(填化学式),最不活泼的元素是___ (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是____ ,碱性最强的化合物的化学式是:_____ 。
(3)比较①与⑤的最高价氧化物对应的水化物,_____ 的酸性强(填化学式),能证明两者酸性强弱的离子反应方程式为______
(4)实验室制取②的氢化物的化学方程式________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑦元素的离子半径
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)比较①与⑤的最高价氧化物对应的水化物,
(4)实验室制取②的氢化物的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表中的一部分,列出10种元素在周期表中的位置,用化学符号回答下列各题。
(1)10种元素中,化学性质最不活泼的是___________ 。
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物的化学式为___________ 。
(5)①和⑨两元素形成化合物的电子式为___________ :该化合物焰色试验为___________ 色。
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为___________ 。
| 主族 周期 | ||||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(4)元素⑦的氢化物的化学式为
(5)①和⑨两元素形成化合物的电子式为
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
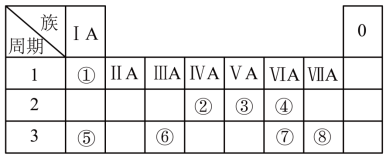
(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素⑧和⑥组成的化合物是_______ (填“离子化合物”或“共价化合物”),可以证明你的判断正确的实验依据是_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式),该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含 的分子的电子式是
的分子的电子式是_______ 。

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素④⑦的最简单氢化物的稳定性关系为
(3)由元素⑧和⑥组成的化合物是
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含
 的分子的电子式是
的分子的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分。

⑴下列说法正确且能说明元素⑩的非金属性比元素⑨强的是_______ 。
⑵某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是_____ ,与该元素单质分子互为等电子体的二价阴离子是______ 。
⑶已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与盐酸反应的离子方程式:
__________________________________________________________________ 。
⑷上述元素⑦形成的晶体对应的晶胞为下图中的___________________ (填写序号)。
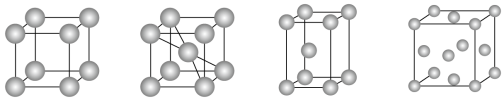
甲 乙 丙 丁
⑸元素④的含氧酸的结构式可表示为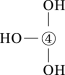 则可判断该酸为
则可判断该酸为__ 酸(填强或弱)
一分子该酸与水作用,只能产生1个H+,请写出该酸溶于水后溶液显酸性的离子方程式__________________________________________ 。
⑹已知元素⑧气态氯化物的化学式为R2Cl6,结构式如下,试并标出其中的配位键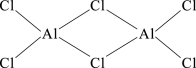

⑴下列说法正确且能说明元素⑩的非金属性比元素⑨强的是
| A.同温同压下,元素⑩的气态氢化物溶解度大于元素⑨的气态氢化物 |
| B.元素的最高价氧化物对应的水化物的酸性⑩强于⑨ |
| C.元素⑨和⑩的单质与铁反应分别得到低价、高价铁的化合物 |
| D.元素⑩的电负性大于元素⑨ |
⑵某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
⑶已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与盐酸反应的离子方程式:
⑷上述元素⑦形成的晶体对应的晶胞为下图中的

甲 乙 丙 丁
⑸元素④的含氧酸的结构式可表示为
 则可判断该酸为
则可判断该酸为一分子该酸与水作用,只能产生1个H+,请写出该酸溶于水后溶液显酸性的离子方程式
⑹已知元素⑧气态氯化物的化学式为R2Cl6,结构式如下,试并标出其中的配位键

您最近一年使用:0次