江苏省苏州高新区第一中学教育集团2023-2024学年高一上学期12月月考化学试题
江苏
高一
阶段练习
2024-01-15
66次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、物质结构与性质、化学反应原理
江苏省苏州高新区第一中学教育集团2023-2024学年高一上学期12月月考化学试题
江苏
高一
阶段练习
2024-01-15
66次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
1. 下列哪种物质不列入城市“空气质量日报”的首要污染物( )
| A.CO2 | B.NO2 | C.SO2 | D.可吸入颗粒物PM2.5 |
【知识点】 硫的氧化物对人体、环境的危害 酸雨解读 大气污染
您最近一年使用:0次
2020-02-23更新
|
175次组卷
|
2卷引用:江苏省南通市如东高级中学2019-2020学年高一上学期12月月考化学试题
单选题
|
容易(0.94)
名校
解题方法
2. 下列有关化学用语正确的是
A.中子数为12的钠原子: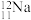 | B.KBrO3中Br元素的化合价:-1 |
C.Cl-的结构示意图: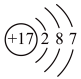 | D.硫酸钾的电离方程式: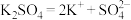 |
您最近一年使用:0次
2023-08-20更新
|
127次组卷
|
3卷引用:江苏省徐州市沛县汉兴高级中学等2校2022-2023学年高一上学期12月联考化学试题
单选题
|
容易(0.94)
名校
3. 实验室从草木灰中获得碳酸钾并检验钾元素存在的原理和装置不能达到实验目的的是
A.溶解 | B.过滤 |
C.蒸发结晶 | D.焰色反应 |
您最近一年使用:0次
2022-01-14更新
|
410次组卷
|
5卷引用:江苏省苏州市2021-2022学年高一上学期期末学业质量阳光指标调研化学试题
单选题
|
较易(0.85)
名校
4. 下列有关物质的性质与用途具有对应关系的是
| A.细铁粉具有还原性,可用作食品抗氧剂 | B.NaHCO3受热易分解,可用于制胃酸中和剂 |
| C.漂白粉在空气中不稳定,可用于漂白纸张 | D.Al2O3是两性氧化物,可用作耐高温材料 |
您最近一年使用:0次
2020-06-04更新
|
348次组卷
|
5卷引用:山东省临沂市2019-2020学年高一上学期期末水平监测化学试题
单选题
|
适中(0.65)
名校
解题方法
5. 碳元素形成的化合物品种多样,常见有CO、CO2、Na2CO3、NaHCO3、酒精、醋酸等,它们在生活与生产中应用广泛。NaHCO3俗称小苏打,下列有关NaHCO3的说法正确的是
A.NaHCO3在水溶液中的电离方程式:NaHCO3= Na+ +H+ +CO |
| B.NaHCO3溶液呈酸性,可与 NaOH溶液反应 |
| C.可用石灰水区别NaHCO3溶液和Na2CO3溶液 |
| D.NaHCO3粉末与相同浓度的盐酸反应比Na2CO3粉末更剧烈 |
您最近一年使用:0次
2022-12-07更新
|
128次组卷
|
3卷引用:江苏省百校联考2022-2023学年高一12月份阶段检测化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.强碱性溶液中: 、 、 、 、 、 、 |
B.新制饱和氯水中: 、 、 、 、 、 、 |
C.澄清透明的溶液中: 、 、 、 、 、 、 |
D.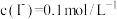 的溶液中: 的溶液中: 、 、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读 氧化还原反应的规律解读
您最近一年使用:0次
2023-03-22更新
|
122次组卷
|
3卷引用:江苏省南通市如东高级中学2019-2020学年高一上学期12月月考化学试题
单选题
|
较易(0.85)
名校
解题方法
7. 下列表示对应化学反应的离子方程式正确的是( )
| A.FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- |
B.氯气溶于水:Cl2+H2O  H++CI-+HClO H++CI-+HClO |
| C.次氯酸钙中通二氧化硫:SO2+Ca2++H2O+2ClO-=CaSO3↓+2HClO |
| D.水玻璃(硅酸钠水溶液)中滴加醋酸:SiO32-+2H+=H2SiO3↓ |
【知识点】 离子反应的发生及书写
您最近一年使用:0次
2020-02-23更新
|
42次组卷
|
2卷引用:江苏省南通市如东高级中学2019-2020学年高一上学期12月月考化学试题
8. 亚氯酸钠( )是一种高效的漂白剂和氧化剂,一种制备亚氯酸钠的流程如下。下列说法正确的是
)是一种高效的漂白剂和氧化剂,一种制备亚氯酸钠的流程如下。下列说法正确的是

 )是一种高效的漂白剂和氧化剂,一种制备亚氯酸钠的流程如下。下列说法正确的是
)是一种高效的漂白剂和氧化剂,一种制备亚氯酸钠的流程如下。下列说法正确的是
A.反应①阶段,参加反应的 和 和 的物质的量之比为1:2 的物质的量之比为1:2 |
| B.为加快反应②速率,可以选用高温条件 |
C.反应②中的 ,可用 ,可用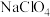 代替 代替 |
D.反应②的条件下, 的氧化性大于 的氧化性大于 |
【知识点】 氧化还原反应的几组概念解读 氧化性、还原性强弱的比较解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
9. 硫酸亚铁是一种重要的化工原料,部分转化如下图所示。下列说法正确的是
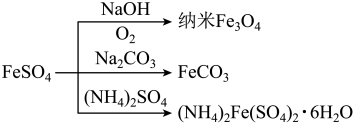

A.只用KSCN溶液不可以检验 是否变质 是否变质 |
B.制纳米 时通入的 时通入的 需过量 需过量 |
C.制 时应将饱和 时应将饱和 溶液加入 溶液加入 溶液中 溶液中 |
D.生成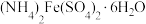 的反应为氧化还原反应 的反应为氧化还原反应 |
您最近一年使用:0次
2023-07-31更新
|
161次组卷
|
2卷引用:江苏省南通市2022-2023学年高三上学期12月月考化学试题
单选题
|
适中(0.65)
名校
10. 已知X、Y、Z、W四种元素,原子序数小于18且依次增大。其中X元素原子最外层电子数是内层电子总数的2倍:Y元素最外层电子数比其次外层电子数多4个;Z元素原子最外层有1个电子;W元素原子K层和M层电子总数等于其L层电子数。下列说法正确的是
A.W元素形成的阴离子的结构示意图为 |
| B.化合物XY属于酸性氧化物 |
C.化合物 能与 能与 发生化合反应 发生化合反应 |
D.化合物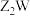 中阴、阳离子的最外层电子数均达到8个电子稳定结构 中阴、阳离子的最外层电子数均达到8个电子稳定结构 |
您最近一年使用:0次
2023-12-03更新
|
408次组卷
|
4卷引用:江苏省连云港市赣榆区2023-2024学年高一上学期期中学业质量监测测化学试题
单选题
|
较易(0.85)
名校
解题方法
11. 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中加入 溶液,将湿润的红色石蕊试纸靠近试管口,试纸不变蓝 溶液,将湿润的红色石蕊试纸靠近试管口,试纸不变蓝 | 溶液中一定不含 |
| B | 将除去表面氧化膜的相同大小的镁片和铝片分别投入 的盐酸中,镁片反应更剧烈 的盐酸中,镁片反应更剧烈 | 金属性: |
| C | 将铁锈溶于过量浓盐酸,再滴入几滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 铁锈中不含 |
| D | 向 酸化的 酸化的 溶液中加入Cu片,观察Cu片溶解 溶液中加入Cu片,观察Cu片溶解 |  氧化性比 氧化性比 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
12. 海洋是一个资源宝库,海水资源的开发和利用是现代和未来永恒的主题。下面是海水利用的流程如下:

下列有关说法不正确的是

下列有关说法不正确的是
A.反应②加热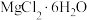 应在HCl气流保护下制备无水 应在HCl气流保护下制备无水 |
| B.氯碱工业与电源正极相连的电极上产生了使湿润淀粉碘化钾试纸变蓝的气体 |
C.过程中制得 是先往精盐溶液中通入 是先往精盐溶液中通入 ,再通入 ,再通入 |
D.反应⑤中,用 水溶液吸收 水溶液吸收 后,用70~80%硫酸富集 后,用70~80%硫酸富集 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
13. 将 和空气的混合气体通入
和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收S,其物质转化如题图所示。下列说法正确的是
的混合溶液中反应回收S,其物质转化如题图所示。下列说法正确的是
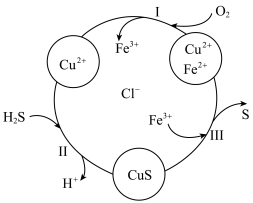
 和空气的混合气体通入
和空气的混合气体通入 、
、 、
、 的混合溶液中反应回收S,其物质转化如题图所示。下列说法正确的是
的混合溶液中反应回收S,其物质转化如题图所示。下列说法正确的是
| A.在图示转化中,化合价不变的元素只有铜、氢 |
B.过程Ⅲ反应的离子方程式为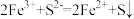 |
C.通入过量的氧气或者增大 的浓度可以减少回收的S中CuS的含量 的浓度可以减少回收的S中CuS的含量 |
D.有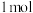  转化为硫单质时,理论上消耗 转化为硫单质时,理论上消耗 的物质的量为2mol[若溶液中 的物质的量为2mol[若溶液中 不变] 不变] |
【知识点】 氧化还原反应的应用 氧化还原反应有关计算 硫化氢解读 铁盐
您最近一年使用:0次
2023-04-22更新
|
200次组卷
|
3卷引用:江苏省黄埭中学2022-2023学年高一下学期期中调研测试化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
14. 随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
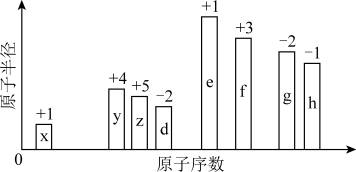
(1)元素x在元素周期表中的位置是___________ 。
(2)元素x、z可形成含10电子的分子甲,其结构式为___________ 。在微电子工业中,甲的水溶液可作刻蚀剂 的消除剂,所得产物不污染环境,其化学方程式是
的消除剂,所得产物不污染环境,其化学方程式是___________ 。
(3)x分别与yzd形成的化合物中,最稳定的物质是___________ (填化学式)
(4)元素d.e形成的简单离子,半径较大的离子是___________ (填离子符号)。
(5)元素g、h的最高价氧化物的水化物的酸性较强的是___________ (填化学式)。
(6)元素e、f的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(7)化合物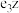 遇水反应生成氨气(
遇水反应生成氨气( )和一种强碱,反应的化学方程式为
)和一种强碱,反应的化学方程式为___________ 。
(8)NaH的电子式___________ 。

(1)元素x在元素周期表中的位置是
(2)元素x、z可形成含10电子的分子甲,其结构式为
 的消除剂,所得产物不污染环境,其化学方程式是
的消除剂,所得产物不污染环境,其化学方程式是(3)x分别与yzd形成的化合物中,最稳定的物质是
(4)元素d.e形成的简单离子,半径较大的离子是
(5)元素g、h的最高价氧化物的水化物的酸性较强的是
(6)元素e、f的最高价氧化物的水化物之间发生反应的离子方程式为
(7)化合物
 遇水反应生成氨气(
遇水反应生成氨气( )和一种强碱,反应的化学方程式为
)和一种强碱,反应的化学方程式为(8)NaH的电子式
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
15. 硫代硫酸钠(Na2S2O3)常用作纸浆漂白的脱氯剂。实验室可用下图装置制备少量Na2S2O3。
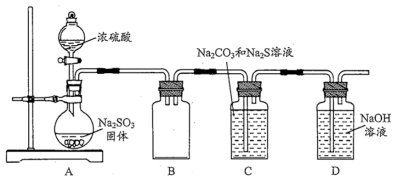
已知∶ ①BaS2O3难溶于水;
②Na2S2O3在酸性溶液中发生反应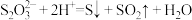
(1)装置A用于制备SO2,其化学方程式为_____ 。装置B的作用是_____ 。
(2)装置C中反应生成Na2S2O3的同时放出CO2,其离子方程式为___ ,该反应中SO2体现了____ 性(填“氧化”或“还原”)。
(3)装置C所得溶液经过结晶等操作获得的Na2S2O3晶体中含有少量Na2SO4,检验其中含有Na2SO4的方法是∶ 取少量固体,______ ,静置,过滤,_____ ,有白色沉淀生成。
(4)装置 D的作用是_____
(5)为验证装置C中生成了 CO2,下列所选的试剂组合和顺序合理的是____ 。
a.品红→NaOH溶液→澄清石灰水
b.酸性KMnO4溶液→品红→澄清石灰水
c.NaOH 溶液→品红→澄清石灰水

已知∶ ①BaS2O3难溶于水;
②Na2S2O3在酸性溶液中发生反应
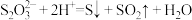
(1)装置A用于制备SO2,其化学方程式为
(2)装置C中反应生成Na2S2O3的同时放出CO2,其离子方程式为
(3)装置C所得溶液经过结晶等操作获得的Na2S2O3晶体中含有少量Na2SO4,检验其中含有Na2SO4的方法是∶ 取少量固体,
(4)装置 D的作用是
(5)为验证装置C中生成了 CO2,下列所选的试剂组合和顺序合理的是
a.品红→NaOH溶液→澄清石灰水
b.酸性KMnO4溶液→品红→澄清石灰水
c.NaOH 溶液→品红→澄清石灰水
您最近一年使用:0次
2021-01-31更新
|
626次组卷
|
7卷引用:江苏省苏州市2020-2021学年高一上学期学业质量阳光指标调研考试化学试题
江苏省苏州市2020-2021学年高一上学期学业质量阳光指标调研考试化学试题四川省泸州市泸县第五中学2022-2023学年高一上学期12月月考化学试题江苏师范大学附属实验学校2022-2023学年高一上学期期末考试化学试题江苏省南京航空航天大学苏州附属中学2022-2023学年高一上学期12月月考化学试题(已下线)专题07 硫及含硫化合物 环境保护-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)江苏省苏州市吴江中学2023-2024学年高一上学期12月月考化学试题(2卷)江苏省苏州高新区第一中学教育集团2023-2024学年高一上学期12月月考化学试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
16. I.侯氏联合制碱法的工艺流程如下:
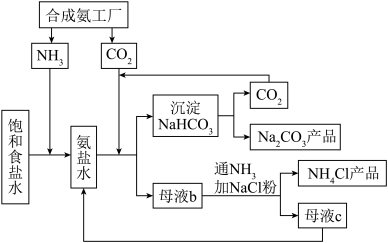
(1)该流程中生成 的化学方程式为
的化学方程式为___________ 。
(2)向母液b中通氨气并加入食盐粉,通氨气的作用有___________(填序号)。
Ⅱ.常温下,向 含
含 的溶液中,逐滴加入含溶质
的溶液中,逐滴加入含溶质 的盐酸溶液
的盐酸溶液 ,溶液中含碳元素的各种微粒的含量随溶液
,溶液中含碳元素的各种微粒的含量随溶液 变化如图
变化如图

(3)在滴加盐酸的过程中 的数目变化的原因是
的数目变化的原因是___________ 、___________ (分别用离子方程式表示)。
(4)反应结束时,溶液中含碳元素的微粒的含量比反应开始时低的原因是___________ 。
Ⅲ.某实验小组将 和固体分别配制成
和固体分别配制成 的溶液,设计如下方案并对反应现象作出预测:
的溶液,设计如下方案并对反应现象作出预测:
(5)实际实验后,发现操作2的现象为产生白色沉淀和气体,与预测有差异。则该条件下, 溶液与
溶液与 液反应的离方程式为
液反应的离方程式为___________ 。

(1)该流程中生成
 的化学方程式为
的化学方程式为(2)向母液b中通氨气并加入食盐粉,通氨气的作用有___________(填序号)。
A.使 结晶析出 结晶析出 |
B.使 更多地析出 更多地析出 |
C.增大 浓度,使 浓度,使 更多地析出 更多地析出 |
D.使 转化为 转化为 ,提高析出的 ,提高析出的 纯度 纯度 |
Ⅱ.常温下,向
 含
含 的溶液中,逐滴加入含溶质
的溶液中,逐滴加入含溶质 的盐酸溶液
的盐酸溶液 ,溶液中含碳元素的各种微粒的含量随溶液
,溶液中含碳元素的各种微粒的含量随溶液 变化如图
变化如图
(3)在滴加盐酸的过程中
 的数目变化的原因是
的数目变化的原因是(4)反应结束时,溶液中含碳元素的微粒的含量比反应开始时低的原因是
Ⅲ.某实验小组将
 和固体分别配制成
和固体分别配制成 的溶液,设计如下方案并对反应现象作出预测:
的溶液,设计如下方案并对反应现象作出预测:| 实验方案 | 预测现象 | 预测依据 |
操作1:向 溶液中滴加 溶液中滴加 溶液 溶液 | 有白色沉淀 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
操作2:向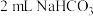 溶液中滴加 溶液中滴加 溶液 溶液 | 无白色沉淀 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应 反应 |
(5)实际实验后,发现操作2的现象为产生白色沉淀和气体,与预测有差异。则该条件下,
 溶液与
溶液与 液反应的离方程式为
液反应的离方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
名校
解题方法
17.  是重要的化工原料,由软锰矿(主要成分为
是重要的化工原料,由软锰矿(主要成分为 ,主要杂质有
,主要杂质有 和
和 )制备
)制备 的一种工艺流程如图:
的一种工艺流程如图:
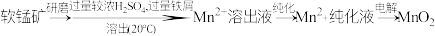
资料:①该工艺条件下 与
与 不反应。
不反应。
②部分金属阳离子沉淀的 (25℃)。
(25℃)。
(1)“溶出”前,软锰矿需要进行研磨的目的___________ 。
(2)“溶出”时,Fe的氧化过程及得到 的主要途径如图所示。
的主要途径如图所示。
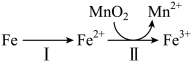
①Ⅱ是从软锰矿石中溶出 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是___________ 。
②若 全部来自于反应
全部来自于反应 ,完全溶出
,完全溶出 所需Fe与
所需Fe与 的物质的量比值为2,而实际比值约0.9小于2,原因是
的物质的量比值为2,而实际比值约0.9小于2,原因是___________ 。
(3)“纯化”时,先向溶出液中先加入 ,将溶液中
,将溶液中 氧化;再加入
氧化;再加入 调节溶液
调节溶液 ,使
,使 、
、 转化为氢氧化物沉淀而除去。适宜调节的
转化为氢氧化物沉淀而除去。适宜调节的 范围是
范围是___________ 。
(4)“纯化”后,过滤所得的滤渣中含有 和
和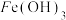 ,实验室欲以该滤渣为原料制备少量
,实验室欲以该滤渣为原料制备少量 ,实验操作为:取少量滤渣放入烧杯中,
,实验操作为:取少量滤渣放入烧杯中,___________ 。(须使用的试剂: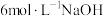 溶液、干冰)
溶液、干冰)
(5)向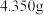 所得
所得 产品中依次加入足量
产品中依次加入足量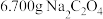 和足量稀
和足量稀 ,加热至充分反应,再用
,加热至充分反应,再用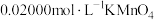 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。计算该产品中
。计算该产品中 的纯度(杂质不参加反应,写出计算过程)
的纯度(杂质不参加反应,写出计算过程)___________ 。
已知过程中发生的反应为: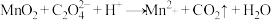 (未配平)、
(未配平)、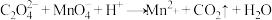 (未配平)
(未配平)
 是重要的化工原料,由软锰矿(主要成分为
是重要的化工原料,由软锰矿(主要成分为 ,主要杂质有
,主要杂质有 和
和 )制备
)制备 的一种工艺流程如图:
的一种工艺流程如图: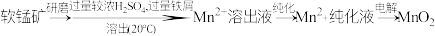
资料:①该工艺条件下
 与
与 不反应。
不反应。②部分金属阳离子沉淀的
 (25℃)。
(25℃)。 |  |  |  | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)“溶出”前,软锰矿需要进行研磨的目的
(2)“溶出”时,Fe的氧化过程及得到
 的主要途径如图所示。
的主要途径如图所示。
①Ⅱ是从软锰矿石中溶出
 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是②若
 全部来自于反应
全部来自于反应 ,完全溶出
,完全溶出 所需Fe与
所需Fe与 的物质的量比值为2,而实际比值约0.9小于2,原因是
的物质的量比值为2,而实际比值约0.9小于2,原因是(3)“纯化”时,先向溶出液中先加入
 ,将溶液中
,将溶液中 氧化;再加入
氧化;再加入 调节溶液
调节溶液 ,使
,使 、
、 转化为氢氧化物沉淀而除去。适宜调节的
转化为氢氧化物沉淀而除去。适宜调节的 范围是
范围是(4)“纯化”后,过滤所得的滤渣中含有
 和
和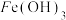 ,实验室欲以该滤渣为原料制备少量
,实验室欲以该滤渣为原料制备少量 ,实验操作为:取少量滤渣放入烧杯中,
,实验操作为:取少量滤渣放入烧杯中,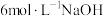 溶液、干冰)
溶液、干冰)(5)向
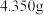 所得
所得 产品中依次加入足量
产品中依次加入足量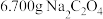 和足量稀
和足量稀 ,加热至充分反应,再用
,加热至充分反应,再用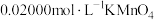 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。计算该产品中
。计算该产品中 的纯度(杂质不参加反应,写出计算过程)
的纯度(杂质不参加反应,写出计算过程)已知过程中发生的反应为:
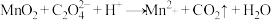 (未配平)、
(未配平)、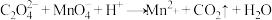 (未配平)
(未配平)
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、物质结构与性质、化学反应原理
试卷题型(共 17题)
题型
数量
单选题
13
填空题
1
解答题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 硫的氧化物对人体、环境的危害 酸雨 大气污染 | |
| 2 | 0.94 | 有关粒子结构的化学用语 原子结构示意图、离子结构示意图 电离方程式 | |
| 3 | 0.94 | 焰色试验 物质的分离、提纯 物质分离、提纯的常见物理方法 蒸发与结晶 | |
| 4 | 0.85 | 漂白粉的变质原因及检验 碳酸氢钠的俗称、物理性质及用途 碳酸氢钠与酸反应 氧化铝的物理性质与用途 | |
| 5 | 0.65 | 电离方程式 碳酸氢钠与碱反应 碳酸钠与碳酸氢钠性质的比较 碳酸钠与碳酸氢钠鉴别的实验 | |
| 6 | 0.65 | 限定条件下的离子共存 氧化还原反应的规律 | |
| 7 | 0.85 | 离子反应的发生及书写 | |
| 8 | 0.85 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 | |
| 9 | 0.65 | Fe2+的鉴别及其应用 Fe2+的还原性 Fe3+的检验 | |
| 10 | 0.65 | 原子结构示意图、离子结构示意图 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 原子核外电子的排布 | |
| 11 | 0.85 | 氧化性、还原性强弱的比较 铵根离子的检验 元素金属性强弱的比较方法 物质性质实验方案的设计 | |
| 12 | 0.85 | 氯碱工业 物质分离、提纯综合应用 海水提取溴 海水提取镁 | |
| 13 | 0.65 | 氧化还原反应的应用 氧化还原反应有关计算 硫化氢 铁盐 | |
| 二、填空题 | |||
| 14 | 0.65 | 离子方程式的书写 元素非金属性强弱的比较方法 微粒半径大小的比较方法 “位构性”关系理解及应用 | |
| 三、解答题 | |||
| 15 | 0.65 | 二氧化硫的制备 物质制备的探究 | 实验探究题 |
| 16 | 0.65 | 离子方程式的书写 碳酸钠与碳酸氢钠性质的比较 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 17 | 0.4 | 化学方程式中物质的量的运用 离子方程式的书写 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |



