对物质进行分类和相关化学计算在化学研究中有重要意义。
(1)下列物质中:①液态氯化氢;② ;③熔融
;③熔融 ;④
;④ 固体;⑤氨水;⑥氢氧化钡溶液;⑦铝;⑧纯醋酸;⑨酒精。属于电解质的是
固体;⑤氨水;⑥氢氧化钡溶液;⑦铝;⑧纯醋酸;⑨酒精。属于电解质的是_______ (填序号,下同),能导电的是________ 。
(2)长征系列运载火箭的燃料之一是肼( )。
)。
①32g肼( )中含有氮原子的数目是
)中含有氮原子的数目是______ ,含有相同电子数的 的质量是
的质量是_____ 。
②肼在氧气中燃烧只生成 和
和 ,燃烧后生成的氧化产物和还原产物的物质的量之比是
,燃烧后生成的氧化产物和还原产物的物质的量之比是______ 。
(3)实验室需用98%浓硫酸配制80mL
 溶液。
溶液。
①所需用到的玻璃仪器有量筒、烧杯、玻璃棒、______ 。
②若实验中出现下列情况,导致所配溶液的物质的量浓度偏低的是_____ (填字母)。
A.配制前,容量瓶中有少量蒸馏水
B.用量筒量取浓硫酸时俯视刻度线
C.定容时俯视刻度线
D.加蒸馏水时不慎超过了刻度线
E.定容后将容量瓶塞盖紧颠倒摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
(1)下列物质中:①液态氯化氢;②
 ;③熔融
;③熔融 ;④
;④ 固体;⑤氨水;⑥氢氧化钡溶液;⑦铝;⑧纯醋酸;⑨酒精。属于电解质的是
固体;⑤氨水;⑥氢氧化钡溶液;⑦铝;⑧纯醋酸;⑨酒精。属于电解质的是(2)长征系列运载火箭的燃料之一是肼(
 )。
)。①32g肼(
 )中含有氮原子的数目是
)中含有氮原子的数目是 的质量是
的质量是②肼在氧气中燃烧只生成
 和
和 ,燃烧后生成的氧化产物和还原产物的物质的量之比是
,燃烧后生成的氧化产物和还原产物的物质的量之比是(3)实验室需用98%浓硫酸配制80mL

 溶液。
溶液。①所需用到的玻璃仪器有量筒、烧杯、玻璃棒、
②若实验中出现下列情况,导致所配溶液的物质的量浓度偏低的是
A.配制前,容量瓶中有少量蒸馏水
B.用量筒量取浓硫酸时俯视刻度线
C.定容时俯视刻度线
D.加蒸馏水时不慎超过了刻度线
E.定容后将容量瓶塞盖紧颠倒摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
更新时间:2024-02-16 20:09:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】标况下,现有96克的氧气和44.8升的二氧化碳两者的密度之比为___________ ;两者的体积之比为______________ ;两者所含原子总数之比为_______________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列填空:
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(2)相同质量的CO和CO2,它们所含的原子数之比为_______ 。
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是_______ ,密度之比为_______ ,质量之比为_______ 。
(4)写出实验室制氯气的化学方程式_______ ,在此过程中呈酸性的HCl与参加反应的总HCl的质量之比为_______ ,每产生1mol氯气转移电子数为 _______ 。
(5)配平化学方程式:_______ 。
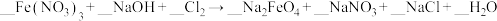
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为
(2)相同质量的CO和CO2,它们所含的原子数之比为
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是
(4)写出实验室制氯气的化学方程式
(5)配平化学方程式:
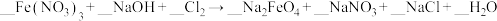
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】通过计算填空。
(1)3.01×1023个H3O+的物质的量为___________ mol,其中,所含原子的物质的量为___________ mol,所含电子的数目为___________ 。
(2)已知12.4 g Na2R含0.4 mol Na+,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(3)将1.42 g Na2SO4溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为____ g。
(4)标准状况下,22.4 L HCl气体溶于水,配制成250 mL盐酸,若将该盐酸稀释成1 L溶液A,则A溶液中氯化氢的物质的量浓度为___________ 。
(5)从(4)中溶液A中取出250mL盐酸与足量Zn反应,标准状况下可以生成的气体体积为___________
(1)3.01×1023个H3O+的物质的量为
(2)已知12.4 g Na2R含0.4 mol Na+,则Na2R的摩尔质量为
(3)将1.42 g Na2SO4溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
(4)标准状况下,22.4 L HCl气体溶于水,配制成250 mL盐酸,若将该盐酸稀释成1 L溶液A,则A溶液中氯化氢的物质的量浓度为
(5)从(4)中溶液A中取出250mL盐酸与足量Zn反应,标准状况下可以生成的气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】早期人们用氯气 给自来水消毒。下列方法均可制得氯气:
给自来水消毒。下列方法均可制得氯气:
①
②
(1)反应①中,氧化剂是_______ ,还原剂是_______ 。并用双线桥法表示下列反应方程式的电子转移方向和数目:_______

(2)反应①中有71g氯气生成时,有_______ g HCl被氧化:
(3)反应②中 、
、 的氧化性由强到弱的顺序是_______>_______;
的氧化性由强到弱的顺序是_______>_______;____
(4)若要制得相同质量的氯气,反应①和反应②中电子转移数目之比为_______ 。
(5)配平反应②_____
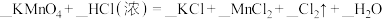
 给自来水消毒。下列方法均可制得氯气:
给自来水消毒。下列方法均可制得氯气:①

②

(1)反应①中,氧化剂是

(2)反应①中有71g氯气生成时,有
(3)反应②中
 、
、 的氧化性由强到弱的顺序是_______>_______;
的氧化性由强到弱的顺序是_______>_______;(4)若要制得相同质量的氯气,反应①和反应②中电子转移数目之比为
(5)配平反应②
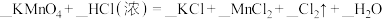
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为_______ ,钠在反应中容易_______ 电子(填“得到”或“失去”)。
(2)某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
ⅰ.当汽车发生较严重的碰撞时,引发NaN3分解:2NaN3 = 2Na + 3N2,从而为气囊充气。其中Na是_______ (填“氧化剂”、“还原剂”、“氧化产物”或“还原产物”)。
ⅱ.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是_______ 。
ⅲ.NaHCO3是冷却剂,吸收产气过程释放的热量。NaHCO3起冷却作用时发生反应的化学方程式为_______ 。
ⅳ.一个安全气囊通常装有50 g NaN3,其完全分解所释放的N2为_______ g。 (保留小数点后一位。)
(1)钠的原子结构示意图为
(2)某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
ⅰ.当汽车发生较严重的碰撞时,引发NaN3分解:2NaN3 = 2Na + 3N2,从而为气囊充气。其中Na是
ⅱ.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是
ⅲ.NaHCO3是冷却剂,吸收产气过程释放的热量。NaHCO3起冷却作用时发生反应的化学方程式为
ⅳ.一个安全气囊通常装有50 g NaN3,其完全分解所释放的N2为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。
试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________ (填序号)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方程式:____
(4)Fe与过量稀硫酸反应可以制取FeSO4。若将反应所得的酸性溶液中Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________ (填序号)。
A.Cl2 B.Fe
C.H2O2 D.HNO2
试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4。若将反应所得的酸性溶液中Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe
C.H2O2 D.HNO2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据所学知识回答下列问题:
(1)①欲用98%的浓硫酸配制质量分数为20%的稀硫酸,实验中需要用到的仪器除了烧杯、玻璃棒以外,还需要_______________ ,其中玻璃棒的作用是________________ 。
②实验室需要0.1 mol·L-1的NaOH溶液450 mL。下列操作使所配NaOH溶液浓度偏高的是__________ (填写序号)。
A.定容时俯视刻度线
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.NaOH溶解后,未冷却就立即转移到容量瓶中
(2)焊接钢轨时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。根据题意,判断X的化学式是____________ ,发生氧化反应的物质是___________ ,若有1mol Fe2O3参加反应,转移电子的物质的量为________ mol。
(3)200mL某溶液中有5种离子大量共存,其中4种离子的物质的量如下表:
则另外一种离子是_______ (填写代号),该离子的浓度为_________________ 。
A.Fe2+ B.Cl- C. Al3+ D.ClO-
(1)①欲用98%的浓硫酸配制质量分数为20%的稀硫酸,实验中需要用到的仪器除了烧杯、玻璃棒以外,还需要
②实验室需要0.1 mol·L-1的NaOH溶液450 mL。下列操作使所配NaOH溶液浓度偏高的是
A.定容时俯视刻度线
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.NaOH溶解后,未冷却就立即转移到容量瓶中
(2)焊接钢轨时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。根据题意,判断X的化学式是
(3)200mL某溶液中有5种离子大量共存,其中4种离子的物质的量如下表:
| 离子 | H+ | K+ | NO3- | SO42- |
| 物质的量(mol) | 0.5 | 0.1 | 0.6 | 0.15 |
则另外一种离子是
A.Fe2+ B.Cl- C. Al3+ D.ClO-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.病人输液用的氯化钠注射液,其标签部分内容如下图所示。根据标签所提供的内容,回答下列问题:
(1)该注射液约含有_______ gNaCl。
(2)该注射液中NaCl的物质的量浓度为__ mol/L。(保留2 位有效数字)
II.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1000mL“鲜花保鲜剂中含有的成分,阅读后问答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是_________ 。(填字母)
A.硫酸钾 B.蔗糖 C.高锰酸钾 D.硝酸银
(2)高锰酸钾在水中的电离方程式为_____________________ 。
(3)配制1000mL 上述“鲜花保鲜剂"所需的仪器有: 量筒、天平、药匙、烧杯、__________ 、______ 、_______ 。(在横线上填写所缺仪器的名称);需要高锰酸钾_______ mol。
(4)在溶液配制过程中,下列操作对配制结果没有影响的是________ 。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
C.容量瓶在使用前未干燥,里面有少量蒸馏水
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)“鲜花保鲜剂中K+”的物质的量浓度为_______ 。
| 0.9% 氯化钠注射液500mL [性状]本品为无色或几乎无色的透明液体 [规格]500mL,4.5g |
(1)该注射液约含有
(2)该注射液中NaCl的物质的量浓度为
II.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是1000mL“鲜花保鲜剂中含有的成分,阅读后问答下列问题:
| 成分 | 质量 | 摩尔质量 |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是
A.硫酸钾 B.蔗糖 C.高锰酸钾 D.硝酸银
(2)高锰酸钾在水中的电离方程式为
(3)配制1000mL 上述“鲜花保鲜剂"所需的仪器有: 量筒、天平、药匙、烧杯、
(4)在溶液配制过程中,下列操作对配制结果没有影响的是
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
C.容量瓶在使用前未干燥,里面有少量蒸馏水
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)“鲜花保鲜剂中K+”的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】欲用18.4mol•L-1的浓硫酸配制成浓度为3mol•L-1的稀硫酸100mL。
(1)请将下列各操作,按正确的序号填在横线上。
A.盖上瓶塞反复颠倒摇匀
B.用量筒量取浓H2SO4
C.稀释浓H2SO4
D.用胶头滴管加蒸馏水至刻度线
E.洗涤烧杯和玻璃棒,并将洗涤液转移到容量瓶中
F.向容量瓶中加水至距离刻度线1~2cm处
G.将溶液转入容量瓶
其操作正确的顺序依次为___________ 。
(2)简要回答下列问题:
①所需浓硫酸的体积为___________ mL(保留一位小数)。
②量取时仰视读数将使最终所配浓度___________ (“偏高”、“偏低”、“无影响”)
③将溶液转移到容量瓶后,要洗涤烧杯和玻璃棒2~3次,洗涤液也要转入容量瓶,否则会使浓度___________ 。(“偏高”、“偏低”、“无影响”)
④定容时必须使溶液凹液面与刻度线相切,若俯视会使浓度___________ 。(“偏高”、“偏低”、“无影响”)
(1)请将下列各操作,按正确的序号填在横线上。
A.盖上瓶塞反复颠倒摇匀
B.用量筒量取浓H2SO4
C.稀释浓H2SO4
D.用胶头滴管加蒸馏水至刻度线
E.洗涤烧杯和玻璃棒,并将洗涤液转移到容量瓶中
F.向容量瓶中加水至距离刻度线1~2cm处
G.将溶液转入容量瓶
其操作正确的顺序依次为
(2)简要回答下列问题:
①所需浓硫酸的体积为
②量取时仰视读数将使最终所配浓度
③将溶液转移到容量瓶后,要洗涤烧杯和玻璃棒2~3次,洗涤液也要转入容量瓶,否则会使浓度
④定容时必须使溶液凹液面与刻度线相切,若俯视会使浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为“鲜花保鲜剂”的配比表。
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是_______。
(2)配制240 mL的上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、电子天平、 _______ 、_______ 。
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_______。
(4)“鲜花保鲜剂”中K+(蔗糖和阿司匹林中不含K+)的物质的量浓度为_______ mol/L。
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿可匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是_______。
| A.蔗糖 | B.硫酸钾 | C.高锰酸钾 | D.硝酸银 |
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_______。
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
①配制0.01mol·L-1、0.008mol·L-1等一系列浓度的[Fe(SCN)6]3-(红色)标准比色液。
②样品处理:

③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10mL。
④比色,直到与选取的标准颜色一致或相近即可。
试回答下列问题:
(1)配制100mL0.01mol·L-1溶液,需要的玻璃仪器有:烧杯、玻璃棒,还需要:___________ 、___________ 。
(2)步骤②脱色过程包括加入:___________ (填脱有机色素的吸附剂名称)→搅拌煮沸→冷却→___________ (填操作)。
(3)比色法确定待测液的浓度的原理是___________ 。
①配制0.01mol·L-1、0.008mol·L-1等一系列浓度的[Fe(SCN)6]3-(红色)标准比色液。
②样品处理:

③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10mL。
④比色,直到与选取的标准颜色一致或相近即可。
试回答下列问题:
(1)配制100mL0.01mol·L-1溶液,需要的玻璃仪器有:烧杯、玻璃棒,还需要:
(2)步骤②脱色过程包括加入:
(3)比色法确定待测液的浓度的原理是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I、烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下检测方法。回答下列问题:将vL气样通入适量酸化的H2O2溶液中,恰好使NOx完全被氧化成NO3-,加水稀释至100.00mL。量取20.00mL该溶液,加入v1mLc1mol·L-1FeSO4标准溶液(过量),充分反应后,用c2mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2mL。
(1)NO被H2O2氧化为NO3-的离子方程式为___ 。
(2)加水稀释到100.00ml所用的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要___ ;滴定操作使用的玻璃仪器主要有___ 。
(3)滴定过程中发生下列反应:3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O、Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NOx的物质的量为___ mol。
(4)下列操作会使滴定结果偏高的是___
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4标准溶液部分变质
II、常温下,用酚酞作指示剂,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1的 CH3COOH溶液和HCN溶液所得滴定曲线如图。
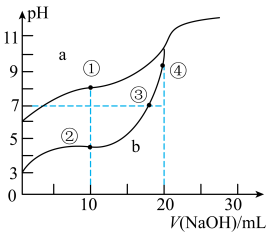
(已知:CH3COOH、 HCN的电离平衡常数分别为1.75×10-5、6.4×10-10)
(1)图___ (a或b)是NaOH溶液滴定HCN溶液的pH变化的曲线。
(2)点③所示溶液中所含离子浓度的从大到小的顺序:___ 。
(3)点①和点②所示溶液中:c(CH3COO-)-c(CN-)___ c(HCN)-c(CH3COOH)(填“>、<或=”)
(1)NO被H2O2氧化为NO3-的离子方程式为
(2)加水稀释到100.00ml所用的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要
(3)滴定过程中发生下列反应:3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O、Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NOx的物质的量为
(4)下列操作会使滴定结果偏高的是
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4标准溶液部分变质
II、常温下,用酚酞作指示剂,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1的 CH3COOH溶液和HCN溶液所得滴定曲线如图。

(已知:CH3COOH、 HCN的电离平衡常数分别为1.75×10-5、6.4×10-10)
(1)图
(2)点③所示溶液中所含离子浓度的从大到小的顺序:
(3)点①和点②所示溶液中:c(CH3COO-)-c(CN-)
您最近一年使用:0次



