某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O),其实验方案如下:
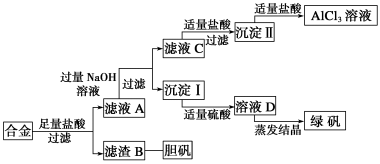
(1)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:___________ 。写出由沉淀Ⅱ转化为AlCl3溶液的离子方程式:___________ 。
(2)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为___________ 。

(1)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:
(2)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为
2024高三下·全国·专题练习 查看更多[1]
(已下线)题型一 工艺流程中陌生方程式的书写-备战2024年高考化学答题技巧与模板构建
更新时间:2024-02-29 16:08:13
|
相似题推荐
填空题
|
适中
(0.65)
真题
【推荐1】碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。完成下列填空:
(1)二氧化碳通入氨水的过程中,先有__ 晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
(2)含0.800 mol NH3的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为____ %。
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③__ ;④加入盐酸调pH;⑤加入__ ;⑥过滤;⑦灼烧,冷却,称重。
(4)上述步骤②中所加入的试剂为__ 、__ 。
(5)上述步骤④中加盐酸调pH的目的是__ 。
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:含0.1 mol NH4HCO3的溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀,则NH4HCO3与NaOH的反应可能为_____ (写离子方程式);若无沉淀,则NH4HCO3与NaOH的反应可能为______ (写离子方程式)。该实验方案有无不妥之处?若有,提出修正意见_____ 。
(1)二氧化碳通入氨水的过程中,先有
(2)含0.800 mol NH3的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③
(4)上述步骤②中所加入的试剂为
(5)上述步骤④中加盐酸调pH的目的是
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:含0.1 mol NH4HCO3的溶液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀,则NH4HCO3与NaOH的反应可能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有如下物质:①Na;②NaOH溶液;③ 固体;④
固体;④ ;⑤酒精(
;⑤酒精( );⑥蒸馏水;⑦
);⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体。
晶体。
(1)以上物质中,属于电解质的是_______ (填序号,右同),属于非电解质的是_______ 。
(2)将②与⑦进行混合,该过程中发生反应的离子方程式是_______ 。
(3)向氢氧化钡溶液中加入物质③的溶液至 恰好沉淀完全,其离子方程式为
恰好沉淀完全,其离子方程式为_______ 。
(4)向100mL②溶液中通入一定量的④,然后向该溶液中逐滴加入2 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示:
的体积(标准状况)关系如图所示:
①0A段发生反应的离子方程式为_______ 。
②m=_______ mL。
③原②溶液的物质的量浓度为_______ 。
(5)将0.1mol⑤在足量氧气中充分燃烧,再将全部产物缓慢通过足量的 固体,
固体, 固体质量增加
固体质量增加______ g。
 固体;④
固体;④ ;⑤酒精(
;⑤酒精( );⑥蒸馏水;⑦
);⑥蒸馏水;⑦ 溶液;⑧
溶液;⑧ 晶体。
晶体。(1)以上物质中,属于电解质的是
(2)将②与⑦进行混合,该过程中发生反应的离子方程式是
(3)向氢氧化钡溶液中加入物质③的溶液至
 恰好沉淀完全,其离子方程式为
恰好沉淀完全,其离子方程式为(4)向100mL②溶液中通入一定量的④,然后向该溶液中逐滴加入2
 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示:
的体积(标准状况)关系如图所示:
①0A段发生反应的离子方程式为
②m=
③原②溶液的物质的量浓度为
(5)将0.1mol⑤在足量氧气中充分燃烧,再将全部产物缓慢通过足量的
 固体,
固体, 固体质量增加
固体质量增加
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2020年11月20日,北京硒博会全国农业展览馆1号馆盛大开幕。硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中含量稀少且分布分散,故常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作___________ (填“阴”或“阳”)极,阳极溶解铜的质量___________ (填“>”“=”或“<”)阴极析出铜的质量。
(2)Se与S处于同一主族,比S原子多1个电子层,硒化氢的电子式为____ ,该族2~5周期元素的单质分别与 反应生成1mol气态氢化物的反应热如下,其中表示生成1mol硒化氢的反应热是
反应生成1mol气态氢化物的反应热如下,其中表示生成1mol硒化氢的反应热是____ (填字母)。
A. B.
B.
C.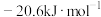 D.
D.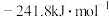
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:i.将含硒的阳极泥与浓硫酸混合后隔绝空气焙烧,产生 、
、 的混合气体;ii.用水吸收i中产生的混合气体,可得Se固体。
的混合气体;ii.用水吸收i中产生的混合气体,可得Se固体。
①尾气中含有少量 ,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为
,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为____ 。
②写出步骤i中发生反应的化学方程式:___________ 。
(1)粗铜精炼时,通常用精铜作
(2)Se与S处于同一主族,比S原子多1个电子层,硒化氢的电子式为
 反应生成1mol气态氢化物的反应热如下,其中表示生成1mol硒化氢的反应热是
反应生成1mol气态氢化物的反应热如下,其中表示生成1mol硒化氢的反应热是A.
 B.
B.
C.
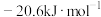 D.
D.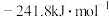
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:i.将含硒的阳极泥与浓硫酸混合后隔绝空气焙烧,产生
 、
、 的混合气体;ii.用水吸收i中产生的混合气体,可得Se固体。
的混合气体;ii.用水吸收i中产生的混合气体,可得Se固体。①尾气中含有少量
 ,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为
,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为②写出步骤i中发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学与人类生活密切相关。请按要求,回答下列问题:
(1)现有以下生产、生活中常见的物质
A.铜丝B.蔗糖C.NaCl晶体D.醋酸溶液E.医用酒精F.Na2CO3粉末G.氨气
①属于电解质是___________ (填写序号,下同);②在上述所给状态下能导电的是___________ 。
(2)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaClO氧化Fe(OH)3来制备,请配平反应方程式:____ClO-+_____Fe(OH)3+___OH-=_______ +____+___Cl-。
+____+___Cl-。_______ ,向制得的Na2FeO4溶液中加入适量的饱和KOH溶液会析出K2FeO4晶体,写出该反应的离子方程式:___________ 。
(3)病人输液用的葡萄糖注射液是葡萄糖(化学式:C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:

①葡萄糖的摩尔质量为___________ 。
②该注射液中葡萄糖的物质的量浓度为___________ 。(保留两位小数)
(4)人体中含有铁元素,+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分,缺铁会引起贫血问题。已知含亚铁离子的溶液易被氧化为Fe3+,现有某品牌补铁口服液,检验其中是否含有Fe3+的方法及操作是:___________ 。
(1)现有以下生产、生活中常见的物质
A.铜丝B.蔗糖C.NaCl晶体D.醋酸溶液E.医用酒精F.Na2CO3粉末G.氨气
①属于电解质是
(2)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaClO氧化Fe(OH)3来制备,请配平反应方程式:____ClO-+_____Fe(OH)3+___OH-=_______
 +____+___Cl-。
+____+___Cl-。(3)病人输液用的葡萄糖注射液是葡萄糖(化学式:C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:

①葡萄糖的摩尔质量为
②该注射液中葡萄糖的物质的量浓度为
(4)人体中含有铁元素,+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分,缺铁会引起贫血问题。已知含亚铁离子的溶液易被氧化为Fe3+,现有某品牌补铁口服液,检验其中是否含有Fe3+的方法及操作是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
图1 图2
图2
①在图示的转化中,被还原的元素是_______ ,X的化学式为_______ 。
②钡元素在周期表中的位置是_______ 。
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:_______ 。
(3)利用ClO2氧化氮氧化物反应过程如下:NO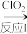 NO2
NO2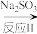 N2
N2
反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+2HCl,反应Ⅱ的离子方程式是_______ 。
(4)加入过量次氯酸钠可使废水中NH 完全转化为N2,而本身被还原为NaCl。
完全转化为N2,而本身被还原为NaCl。
①写出次氯酸钠的电子式_______ 。
②检验废水中是否存在NH 的方法是
的方法是_______ 。
③若处理废水产生了0.448L N2(标准状况),则需消耗浓度为2mol·L-1的次氯酸钠的体积为_______ mL。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
图1
 图2
图2
①在图示的转化中,被还原的元素是
②钡元素在周期表中的位置是
(2)SCR技术可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学方程式:
(3)利用ClO2氧化氮氧化物反应过程如下:NO
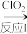 NO2
NO2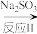 N2
N2反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+2HCl,反应Ⅱ的离子方程式是
(4)加入过量次氯酸钠可使废水中NH
 完全转化为N2,而本身被还原为NaCl。
完全转化为N2,而本身被还原为NaCl。①写出次氯酸钠的电子式
②检验废水中是否存在NH
 的方法是
的方法是③若处理废水产生了0.448L N2(标准状况),则需消耗浓度为2mol·L-1的次氯酸钠的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某兴趣小组用铬铁矿[Fe(CrO2)2] 制备K2Cr2O7晶体,流程如下: 8Na2CrO4+4NaFeO2+10CO2
8Na2CrO4+4NaFeO2+10CO2
2H++2CrO
 Cr2O
Cr2O +H2O
+H2O
相关物质的溶解度随温度变化如下图。
(1)步骤I,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是___ 。
(2)下列说法正确的是___________。
(3)步骤V,重结晶前,为了得到杂质较少的K2Cr2O7粗产品,从下列选项中选出合理的操作(操作不能重复使用)并排序:溶解KCl→___ (______)→(______)→(_____)→(_____)→重结晶。
a.50℃蒸发溶剂;b.100 ℃蒸发溶剂;c.抽滤;d.冷却至室温;e.蒸发至溶液出现晶膜,停止加热;f.蒸发至溶液中出现大量晶体,停止加热。

 8Na2CrO4+4NaFeO2+10CO2
8Na2CrO4+4NaFeO2+10CO22H++2CrO

 Cr2O
Cr2O +H2O
+H2O相关物质的溶解度随温度变化如下图。

(1)步骤I,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是
(2)下列说法正确的是___________。
| A.步骤II,低温可提高浸取率 |
| B.步骤II,过滤可除去NaFeO2水解产生的Fe(OH)3 |
| C.步骤III,酸化的目的主要是使Na2CrO4转变为Na2Cr2O7 |
| D.步骤IV,所得滤渣的主要成分是Na2SO4和Na2CO3 |
a.50℃蒸发溶剂;b.100 ℃蒸发溶剂;c.抽滤;d.冷却至室温;e.蒸发至溶液出现晶膜,停止加热;f.蒸发至溶液中出现大量晶体,停止加热。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂.工业上通常用自然界分布最广的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:

已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5.
②PbCl2(s)+2Cl-(aq) PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的pH值分别为1.9和7.
(I)流程中加入盐酸可以控制溶液的pH<1.9,主要目的是_____________________ ,反应过程中可观察到淡黄色沉淀,则步骤(1)对应的主要反应的离子方程式为 ____________________________ ;
(II)步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是___________ (请用平衡移动原理解释)
(III)上述流程中可循环利用的物质有___________ ;
(Ⅵ)步骤(4)中反应的离子方程式为_____________________ .对滤液C中氯离子的测定可中和后采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl−,利用Ag+与CrO42-生成砖红色沉淀,指示到达滴定终点。选用K2CrO4溶液的最好浓度等于 _____________ mol·L−1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(Ⅴ)PbO2与MnO2性质相似,请写出PbO2与浓盐酸加热条件下反应的离子方程式______________________

已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5.
②PbCl2(s)+2Cl-(aq)
 PbCl42-(aq) △H>0
PbCl42-(aq) △H>0③Fe3+、Pb2+以氢氧化物形式开始沉淀时的pH值分别为1.9和7.
(I)流程中加入盐酸可以控制溶液的pH<1.9,主要目的是
(II)步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是
(III)上述流程中可循环利用的物质有
(Ⅵ)步骤(4)中反应的离子方程式为
(Ⅴ)PbO2与MnO2性质相似,请写出PbO2与浓盐酸加热条件下反应的离子方程式
您最近一年使用:0次

 (
( ):试剂
):试剂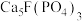 ,含
,含 等杂质]为原料生产磷酸和石膏,工艺流程如下:
等杂质]为原料生产磷酸和石膏,工艺流程如下:
 产生。氢氟酸与
产生。氢氟酸与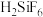 ,离子方程式为
,离子方程式为

