核外电子排布与元素周期系的基本结构
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有_______ 种元素。其余各周期总是从ns能级开始,以np结束,而从ns能级开始以np结束递增的核电荷数(或电子数)就_______ 每个周期里的元素数。
②周期、能级组、元素种类的对应关系
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有
②周期、能级组、元素种类的对应关系
| 周期 | 对应能级组 | 对应能级组最多所能容纳的电子数 | 周期中所含元素种类 |
| 1 | 1s | 2 | 2 |
| 2 | 8 | ||
| 3 | 3s、3p | 8 | 8 |
| 4 | 18 | ||
| 5 | 5s、4d、5p | 18 | 18 |
| 6 | 32 | ||
| 7 | 7s、5f、6d、7p | 32 | 32 |
23-24高一下·全国·课前预习 查看更多[1]
(已下线)1.2.1 原子结构与元素周期表
更新时间:2024-03-01 10:46:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)原子序数大于4的主族元素A和B的离子Am+和Bn-,它们的核外电子排布相同,则:
①A和B的质子数之差为_________________ (用m、n 表示)。
②B和A的族序数之差为_________________ (用含m、n的代数式表示)。
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为_____________________ ;
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为_____________ 。
①A和B的质子数之差为
②B和A的族序数之差为
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)写出铜的基态原子的电子排布式:______ 。
(2)基态Fe原子有______ 个未成对电子,Fe3+的电子排布式为______ 。
(3)Fe在周期表中位于第______ 周期第______ 族,属于______ 区。
Ⅱ.回答下列问题:
(4)p电子的原子轨道呈______ 形。
(5)基态Al3+核外共有______ 种不同运动状态的电子。
(6)钒(V)元素广泛用于催化及钢铁工业,其价层电子的轨道表示式为_______ 。
(1)写出铜的基态原子的电子排布式:
(2)基态Fe原子有
(3)Fe在周期表中位于第
Ⅱ.回答下列问题:
(4)p电子的原子轨道呈
(5)基态Al3+核外共有
(6)钒(V)元素广泛用于催化及钢铁工业,其价层电子的轨道表示式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
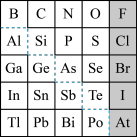
(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
②氢化物的还原性:H2O___ H2S(填“>”、“<”或“=”)。
(2)可在图中分界线(虚线部分)附近寻找___ (填序号)。
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为___ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是___ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4
②氢化物的还原性:H2O
(2)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)下列物质变化,只与范德华力有关的是___ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:
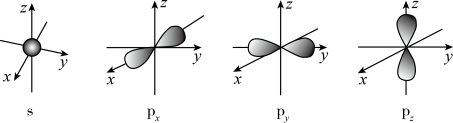
请回答下列问题:
s电子的原子轨道呈__ 形,每个s能级有__ 个原子轨道;p电子的原子轨道呈___ 形,每个p能级有___ 个原子轨道.
(3)Na、Mg、Al第一电离能的由大到小的顺序:___ 。
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是___ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:

请回答下列问题:
s电子的原子轨道呈
(3)Na、Mg、Al第一电离能的由大到小的顺序:
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】基态原子X的电子在L层上只有一个空轨道,则X的原子结构示意图为______________________ ;基态原子R的4p轨道上只有一个未成对电子,则R原子可能是(用化学符号表示)___________ 、__________ ;Y原子的核电荷数为33,其外围电子排布式是_________________ ,在元素周期表中的位置是第_______ 周期第_______ 族,属于__________ 区的元素,其最高价氧化物对应水化物的化学式为_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业的关键原料之一,可由氨气和氟气反应得到:_______NH3+_______F2→_______NF3+_______NH4F。完成下列填空:
(1)配平上述反应方程式_______ 。
(2)F原子的结构示意图是_______ ,其能量最高的电子所占据的电子亚层符号为_______ 。从原子结构角度比较F和N元素的非金属性强弱_______ 。
(3)写出NH4F的电子式_______ ,溶液中NH 的检验方法是
的检验方法是_______ 。
(4)与NH 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是_______ ,该产物的水溶液呈_______ 性,用适当的化学用语解释该溶液酸碱性的原因:_______ 。其稀溶液中存在关系式:c(OH-)-c(H+) =c(HCO ) +
) + _______
(1)配平上述反应方程式
(2)F原子的结构示意图是
(3)写出NH4F的电子式
 的检验方法是
的检验方法是(4)与NH
 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是 ) +
) +
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为:S + 2KNO3 + 3C → K2S + 3CO2↑+ N2↑。请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是________ ;钾元素在周期表中的位置为___________________ 。

(2)上述元素中,简单离子电子层结构与氩原子相同,且离子半径最大的元素,其原子核外有_____ 种不同能级的电子;已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是__________________________________ 。
(3)上述反应生成物中,属于非电解质的是_________________ (写结构式);其中熔点最高的物质的电子式是______________ 。
(4)上述化学方程式的元素中,属于同周期元素的非金属性由强到弱的顺序为_______________ ,能证明其递变规律的事实是_______________ (填字母)。
A、最高价氧化物对应水化物的酸性 B、气态氢化物的沸点
C、单质与氢气反应的难易程度 D、其两两组合形成的化合物中元素的化合价
(5)上述反应中,如1.5mol还原剂________ (填“得到”或“失去”)________ mol电子,则生成_________ g还原产物。
(1)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是

(2)上述元素中,简单离子电子层结构与氩原子相同,且离子半径最大的元素,其原子核外有
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的非金属性由强到弱的顺序为
A、最高价氧化物对应水化物的酸性 B、气态氢化物的沸点
C、单质与氢气反应的难易程度 D、其两两组合形成的化合物中元素的化合价
(5)上述反应中,如1.5mol还原剂
您最近一年使用:0次
【推荐2】中国“奋斗者”号深潜器研制及海试的成功,在钛合金材料制备、锂离子电池等方面实现了重大突破。
(1)深潜器的壳体由含钛、铝等元素的Ti-62A钛合金材料制成,该合金材料的熔点比组成成分的金属___________ (选填“高”或“低”);铝元素的原子核外共有___________ 种不同能级的电子;以下方法可以比较钠和铝金属性强弱的方法___________ 。
a.比较两种金属单质的硬度和熔点
b.用钠置换氯化铝溶液中的铝
c.比较等物质的量的两种金属单质和足量盐酸反应失去的电子数
d.将空气中放置已久的这两种元素的单质分别和热水作用
e.在氯化铝溶液中逐滴滴加过量的氢氧化钠溶液
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,属于________ 晶体,Al、O、N三种元素的简单离子半径由大到小的排列顺序是___________ 。
(3)明矾[KAl(SO4)2·12H2O]溶液中离子浓度从大到小的顺序为_______ 。Mg(OH)2固体能除去镁盐溶液中的Al3+,原因是__________ ,(用离子方程式表达)
(4)在周期表中,锂的性质与镁相似,写出锂在氧气中燃烧产物的电子式________ 。
(5)已知:M(g)→M+(g)+Q(M代表碱金属元素)
从原子结构的角度解释上述金属Q值递变的原因:___________ 。
(1)深潜器的壳体由含钛、铝等元素的Ti-62A钛合金材料制成,该合金材料的熔点比组成成分的金属
a.比较两种金属单质的硬度和熔点
b.用钠置换氯化铝溶液中的铝
c.比较等物质的量的两种金属单质和足量盐酸反应失去的电子数
d.将空气中放置已久的这两种元素的单质分别和热水作用
e.在氯化铝溶液中逐滴滴加过量的氢氧化钠溶液
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,属于
(3)明矾[KAl(SO4)2·12H2O]溶液中离子浓度从大到小的顺序为
(4)在周期表中,锂的性质与镁相似,写出锂在氧气中燃烧产物的电子式
(5)已知:M(g)→M+(g)+Q(M代表碱金属元素)
| 元素 | Li | Na | K | Rb |
| Q(kJ) | -520 | -496 | -419 | -403 |
从原子结构的角度解释上述金属Q值递变的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分。
回答下列问题
(1)表中元素原子半径最大的是(写元素符号)__________ ,Z原子核外电子能量最高的电子亚层是__________ 。
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:_________________ ;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因______________________________________________________ 。
(4)硫酸工业生产中接触室内发生的反应方程式为______________________________________ ;
在实际生产中,操作温度选定400—500℃、压强通常采用常压的原因分别是__________________________________________________________________________________________________ 。
碳 | 氮 | Y | |
X | 硫 | Z |
(1)表中元素原子半径最大的是(写元素符号)
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:
(4)硫酸工业生产中接触室内发生的反应方程式为
在实际生产中,操作温度选定400—500℃、压强通常采用常压的原因分别是
您最近一年使用:0次



