1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
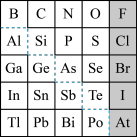
(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
②氢化物的还原性:H2O___ H2S(填“>”、“<”或“=”)。
(2)可在图中分界线(虚线部分)附近寻找___ (填序号)。
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为___ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是___ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4
②氢化物的还原性:H2O
(2)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
19-20高一下·江西南昌·期末 查看更多[3]
(已下线)专题16 元素周期律和元素周期表(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第14讲 元素周期表和元素周期律-2021年高考化学一轮复习名师精讲练江西省南昌市八一中学2019-2020学年高一下学期期末考试化学试题
更新时间:2020-07-13 16:44:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第____ 周期第_____ 族,A、B、C三种元素原子半径从大到小的顺序是_________________ ;
(2)D简单离子的结构示意图为_____________ ,D、E中金属性较强的元素是________ 。D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
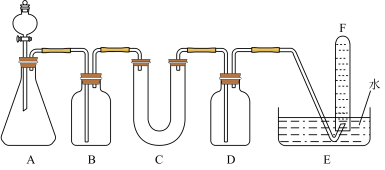
(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去_____________ ;
(4)装置C中X与CO2反应的化学方程式是_____________________ ,装置D盛放NaOH溶液的作用是除去____________ ;
(5)为检验试管F收集的气体,进行____________ 操作,出现_________ 现象,即证明X可作供氧剂。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第
(2)D简单离子的结构示意图为

(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去
(4)装置C中X与CO2反应的化学方程式是
(5)为检验试管F收集的气体,进行
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑧的元素符号是_____ 和_____ ;
(2)表中最活泼的金属元素是_____ ;非金属性最强的元素是____ (填元素符号,下同)
(3)表中能形成两性氢氧化物的元素是_____ ;分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应的水化物反应的化学方程式________________________ ; ________________________ 。
(4)写出元素⑥、⑦的最高价氧化物的化学式分别是______ 和______ ,最高价氧化物水化物的酸性比较是______ ﹥______ 。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)⑤和⑧的元素符号是
(2)表中最活泼的金属元素是
(3)表中能形成两性氢氧化物的元素是
(4)写出元素⑥、⑦的最高价氧化物的化学式分别是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】原子结构与元素周期表存在内在联系,按要求回答下列问题:
(1)根据元素在周期表中的位置,写出元素基态原子的价电子排布式。
①第四周期第ⅥB族_______ ;
②第五周期第ⅠB族_______ ;
③第五周期第ⅣA族_______ ;
④第六周期第ⅡA族_______ 。
(2)根据元素电子排布可以确定元素在周期表中的位置。
①具有(n-1)d10ns2电子排布的元素位于周期表中的第_______ 族。
②已知某元素+2价离子的核外电子排布式为1s22s22p63s23p63d3。该元素位于元素周期表_______ (填序号)。
A.第二周期第ⅡB族
B.第四周期第ⅡA族
C.第四周期第ⅤB族
D.第五周期第ⅡB族
③某元素原子的核电荷数为33,则其原子的价电子排布式为_______ ,其位于元素周期表中的_______ ,属于_______ 区的元素。
(3)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti)元素,基态原子价电子轨道表示式为_______ ,Ti元素形成的化合物中,Ti呈现的最高价态为_______ 价。
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价电子排布式为3d54s1,该元素的名称是_______ 。
(1)根据元素在周期表中的位置,写出元素基态原子的价电子排布式。
①第四周期第ⅥB族
②第五周期第ⅠB族
③第五周期第ⅣA族
④第六周期第ⅡA族
(2)根据元素电子排布可以确定元素在周期表中的位置。
①具有(n-1)d10ns2电子排布的元素位于周期表中的第
②已知某元素+2价离子的核外电子排布式为1s22s22p63s23p63d3。该元素位于元素周期表
A.第二周期第ⅡB族
B.第四周期第ⅡA族
C.第四周期第ⅤB族
D.第五周期第ⅡB族
③某元素原子的核电荷数为33,则其原子的价电子排布式为
(3)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti)元素,基态原子价电子轨道表示式为
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价电子排布式为3d54s1,该元素的名称是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】用化学式填写下列空白:元素周期表的第三周期元素中,除稀有气体外,原子半径最大的是_______ ;最高价氧化物对应的水化物碱性最强的是_______ ;最高价氧化物对应的水化物呈两性的是_______ ;最高价氧化物对应的水化物酸性最强的是_______ .
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】请利用元素周期律和元素周期表的有关知识回答下列问题。
(1)下列关于元素性质或原子结构递变情况的叙述中,错误的是______
(2)A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层电子数是最外层电子数的2倍,则A、B元素。______
(3)短周期元素A、B、C在元素周期表中的位置如图所示。已知B、C两元素的原子序数之和是A元素的原子序数的4倍,则A、B、C分别是______
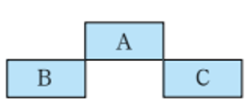
(4)X、Y、Z是相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z分别是_________
(1)下列关于元素性质或原子结构递变情况的叙述中,错误的是______
| A.Li、Be、B原子的最外层电子数依次增多 |
| B.P、S、Cl元素的最高正化合价依次升高 |
| C.N、O、F原子的半径依次增大 |
| D.Na、K、Rb原子核外的电子层数依次增多 |
| A.一定是第2周期元素 | B.一定是同一周期元素 |
| C.一定分别位于第2、3周期 | D.可以相互化合形成化合物 |

| A.Be、Na、Al | B.B、Mg、Si | C.O、P、Cl | D.C、Al、P |
| A.Mg、Al、Si | B.Li、Be、Mg | C.N、O、S | D.P、S、O |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】如表为10种元素在元素周期表中的位置,请回答有关问题:
(1)⑥和⑨形成的化合物为_______ (填离子或共价)化合物,电子式为_______ 。
(2)表中最活泼的金属是_______ (填元素符号,下同),非金属性最强的元素是_______ 。
(3)表中能形成两性氢氧化物的元素是_______ ,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应的水化物反应的化学方程式:_______ 、_______ 。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:_______ 。
| ⅠA | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑥和⑨形成的化合物为
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是______________________ 。
(2)碲的化合价可能有______________________ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是________ (填化学式)。
(4)氢硒酸有较强的________ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______________________________________ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
________ Al2Te3+( ) ===2Al(OH)3↓+________ H2Te↑
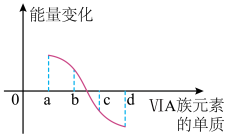
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表________ ,d代表________ (均写单质名称)。
元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1 390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热 化合 | 加热 难化合 | 不能直 接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】用“ ”或“
”或“ ”回答下列问题。
”回答下列问题。
(1)酸性:H2CO3______ H2SiO3,H2SiO3 ______ H3PO4。
(2)碱性:Ca(OH)2______ Mg(OH)2,Mg(OH)2 ______ Al(OH)3。
(3)简单氢化物的稳定性:H2O______ H2S,H2S ______ HCl。
(4)还原性:H2O______ H2S,H2S ______ HCl。
(5)酸性:H2SO4______ H2SO3,HClO4 ______ HClO。
(6)从以上答案中可以归纳出:
①元素的非金属性越强,其最高价氧化物对应的水化物的酸性越______ ;
②元素的金属性越强,其最高价氧化物对应的水化物的碱性越______ ;
③元素的______ 性越强,其对应简单氢化物的稳定性越强;
④非金属性越强的元素生成的简单氢化物的还原性越______ ;
⑤同种非金属元素形成的氧化物对应的水化物,其成酸元素的价态越高,其酸性越______ 。
 ”或“
”或“ ”回答下列问题。
”回答下列问题。(1)酸性:H2CO3
(2)碱性:Ca(OH)2
(3)简单氢化物的稳定性:H2O
(4)还原性:H2O
(5)酸性:H2SO4
(6)从以上答案中可以归纳出:
①元素的非金属性越强,其最高价氧化物对应的水化物的酸性越
②元素的金属性越强,其最高价氧化物对应的水化物的碱性越
③元素的
④非金属性越强的元素生成的简单氢化物的还原性越
⑤同种非金属元素形成的氧化物对应的水化物,其成酸元素的价态越高,其酸性越
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某同学学了元素周期表后,自己设计了一套实验方案,验证元素性质的递变性,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
实验目的:研究同周期元素性质的递变性
(1)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。
仪器:_____ (写两种以上的玻璃仪器),试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(2)实验记录:(填写与实验步骤对应的实验现象的编号和步骤②、步骤⑤反应的离子方程式)
步骤②_____ ,
步骤⑤______ ,
(3)实验结论:____ 。
(4)总结反思:从原子结构角度分析,同周期元素产生性质递变性的原因是______ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体。 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体。 |
| ⑤将铝条投入稀盐酸中 | E.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
实验目的:研究同周期元素性质的递变性
(1)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。
仪器:
(2)实验记录:(填写与实验步骤对应的实验现象的编号和步骤②、步骤⑤反应的离子方程式)
| 实验内容 | ① | ② | ③ | ④ | ⑤ |
| 实验现象(填A~E) |
步骤②
步骤⑤
(3)实验结论:
(4)总结反思:从原子结构角度分析,同周期元素产生性质递变性的原因是
您最近半年使用:0次
【推荐1】磷是人体所必需的重要矿物质元素,磷的化合物在生产和生活中应用广泛。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
(1)磷原子的核外电子排布式:___________ ;磷原子核外有_____ 种能量不同的电子。
(2)上述反应的反应物和生成物中含有非极性键的分子是______ 。(写出物质的化学式)
(3)将Na、O、P三种原子的原子半径大小按由大到小的顺序排列___________________ 。
(4)NH3的稳定性比PH3的(填“强”或“弱”)_________ ,判断理由是____________ 。
(5)A、配平上述反应,并标出电子转移方向与数目_________
P4+ NaOH+ H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为___________ 。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
(1)磷原子的核外电子排布式:
(2)上述反应的反应物和生成物中含有非极性键的分子是
(3)将Na、O、P三种原子的原子半径大小按由大到小的顺序排列
(4)NH3的稳定性比PH3的(填“强”或“弱”)
(5)A、配平上述反应,并标出电子转移方向与数目
P4+ NaOH+ H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】Na2S 常用作皮革脱毛剂,工业上用反应 Na2SO4 +2C Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。
完成下列填空:
(1)硫元素在周期表中的位置为______________ 。上述反应中涉及的各元素中原子半径最小的是
__________ (填元素符号)。写出硫化钠的电子式:___________ 。
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。_____________
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。________________________________
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为______________ mol/(L·h) 。
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。______________________________
 Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。完成下列填空:
(1)硫元素在周期表中的位置为
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
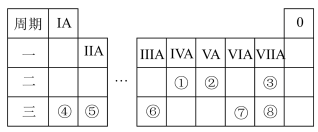
【推荐3】元素周期表反映了元素之间的内在联系,是研究物质性质的重要工具。下图是元素周期表的一部分,请结合推断回答下列问题:________ (填元素符号);简单离子半径最小的元素是:________ (填离子符号)。
(2)由这些元素中原子半径最大与最小的两种元素形成的化合物X的电子式为________ ;画出X中阴离子的离子结构示意图:________ 。
(3)⑦⑧两种元素的最高价氧化物的水化物酸性较强的是________ (填化学式)。
(4)⑥的单质与强碱反应的离子方程式为________ 。
(5)根据周期表的结构特点,推断在第四周期中与⑤和⑥同族的元素原子序数相差________ 。
(6)查阅资料可知:⑤的单质可以在①的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:________ 。
(2)由这些元素中原子半径最大与最小的两种元素形成的化合物X的电子式为
(3)⑦⑧两种元素的最高价氧化物的水化物酸性较强的是
(4)⑥的单质与强碱反应的离子方程式为
(5)根据周期表的结构特点,推断在第四周期中与⑤和⑥同族的元素原子序数相差
(6)查阅资料可知:⑤的单质可以在①的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:
您最近半年使用:0次



