请利用元素周期律和元素周期表的有关知识回答下列问题。
(1)下列关于元素性质或原子结构递变情况的叙述中,错误的是______
(2)A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层电子数是最外层电子数的2倍,则A、B元素。______
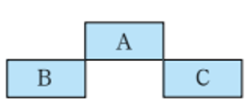
(3)短周期元素A、B、C在元素周期表中的位置如图所示。已知B、C两元素的原子序数之和是A元素的原子序数的4倍,则A、B、C分别是______
(4)X、Y、Z是相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z分别是_________
(1)下列关于元素性质或原子结构递变情况的叙述中,错误的是______
| A.Li、Be、B原子的最外层电子数依次增多 |
| B.P、S、Cl元素的最高正化合价依次升高 |
| C.N、O、F原子的半径依次增大 |
| D.Na、K、Rb原子核外的电子层数依次增多 |
| A.一定是第2周期元素 | B.一定是同一周期元素 |
| C.一定分别位于第2、3周期 | D.可以相互化合形成化合物 |

| A.Be、Na、Al | B.B、Mg、Si | C.O、P、Cl | D.C、Al、P |
| A.Mg、Al、Si | B.Li、Be、Mg | C.N、O、S | D.P、S、O |
20-21高一·全国·课后作业 查看更多[2]
更新时间:2022-11-26 13:14:20
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】用元素符号(或化学式)回答原子序数从1~18的元素的有关问题
(1)与水反应最剧烈的金属是_____________ 。
(2)与水反应最剧烈的非金属是_____________
(3)硬度最大的单质是____________ 。(填名称)
(4)最高正价为+7价的元素是_____________ 。
(1)与水反应最剧烈的金属是
(2)与水反应最剧烈的非金属是
(3)硬度最大的单质是
(4)最高正价为+7价的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素在周期表中的位置反映了元素的原子结构和元素的性质。针对下表中的①~⑩种元素,回答以下问题:

(1)第三周期金属元素中原子半径最小的元素为________ (写序号);表中的X元素在第________ 周期第________ 族。
(2)④、⑤分别与①元素组成含10个电子的分子化学式分别为________ 、________ ;
(3)通过单质之间的置换反应,可以比较卤素单质的氧化性强弱。请用离子方程式表示⑧和⑨元素单质的氧化性强弱:________________ ;
(4)用电子式表示②与⑦形成化合物的过程:________________ ;
(5)由①②⑤元素组成的化合物的化学键类型为________ 、________ ;
(6)写出能证明②的金属性强于③的化学事实________ (任写一条)。

(1)第三周期金属元素中原子半径最小的元素为
(2)④、⑤分别与①元素组成含10个电子的分子化学式分别为
(3)通过单质之间的置换反应,可以比较卤素单质的氧化性强弱。请用离子方程式表示⑧和⑨元素单质的氧化性强弱:
(4)用电子式表示②与⑦形成化合物的过程:
(5)由①②⑤元素组成的化合物的化学键类型为
(6)写出能证明②的金属性强于③的化学事实
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素的相关知识回答下列问题。
(1)按原子序数递增的顺序(稀有气体元素除外),下列说法正确的是____________ (填标号)。
a.原子半径和离子半径均减小
b.元素金属性逐渐减弱,非金属性逐渐增强
c.氧化物的水化物的碱性逐渐减弱,酸性逐渐增强
d.单质的熔点逐渐降低
(2)原子最外层电子数与次外层电子数相同的元素名称为_______ ,氧化性最弱的简单阳离子是________ 。
(3)已知:
①工业制镁时,电解熔融MgCl2而不电解熔融MgO的原因是__________________ 。
②工业制铝时,电解熔融Al2O3而不电解熔融AlCl3的原因是__________ 。
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是__________ (填标号)。
a.NH3 b.HI c.SO2 d.CO2
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时KClO3分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴、阳离子个数比为1:1,写出该反应的化学方程式:__________ 。
(1)按原子序数递增的顺序(稀有气体元素除外),下列说法正确的是
a.原子半径和离子半径均减小
b.元素金属性逐渐减弱,非金属性逐渐增强
c.氧化物的水化物的碱性逐渐减弱,酸性逐渐增强
d.单质的熔点逐渐降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2852 | 2050 | 714 |
|
①工业制镁时,电解熔融MgCl2而不电解熔融MgO的原因是
②工业制铝时,电解熔融Al2O3而不电解熔融AlCl3的原因是
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时KClO3分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴、阳离子个数比为1:1,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】图为元素周期表的一部分,元素①~⑨在元素周期表中的位置如下:
请回答下列问题:
(1)元素⑧周期表中的位置是____ 。
(2)可利用一个化学反应比较⑥⑧非金属性的强弱,写出该反应的化学方程式____________ 。
(3)②和③可形成一种化合物,能作呼吸面具中的供氧剂的。写出该化合物的电子式___ 。
(4)元素③的最高价氧化物对应水化物中含有的化学键类型为______ 。
(5)比较元素⑤⑥的最高价氧化物对应的水化物的酸性强弱______ (用化学式表示)。
(6)比较元素③和⑨的简单离子半径大小_____ (用离子符号表示)。
(7)锗为第四周期与硅同主族,根据元素周期率推测其单质、化合物的性质正确的是 。(填字母)
① | ② | ⑨ | ⑩ | ||||||
③ | ④ | ⑤ | ⑥ | ||||||
⑦ | ⑧ |
(1)元素⑧周期表中的位置是
(2)可利用一个化学反应比较⑥⑧非金属性的强弱,写出该反应的化学方程式
(3)②和③可形成一种化合物,能作呼吸面具中的供氧剂的。写出该化合物的电子式
(4)元素③的最高价氧化物对应水化物中含有的化学键类型为
(5)比较元素⑤⑥的最高价氧化物对应的水化物的酸性强弱
(6)比较元素③和⑨的简单离子半径大小
(7)锗为第四周期与硅同主族,根据元素周期率推测其单质、化合物的性质正确的是 。(填字母)
| A.锗的金属性比⑦强 | B.锗的原子半径比⑧大 |
| C.锗的单质可用于制半导体 | D.锗的最高正价为+3 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表是指导我们系统学习化学的重要工具。(答案都填写化学式)
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图__ ,自然界中存在的54Fe和56Fe,它们互称为___ 。将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是__ 。通常证明某溶液中含Fe2+的化学方法是___ 。
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的__ 相同。处于同一列的N和P位于元素周期表的__ 族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为_ ,其气态氢化物的结构式为__ 。
②与硅元素处于同一周期,两性金属元素是__ ,并写出其在元素周期表中的位置:第__ 周期,__ 族,该元素的最高价氧化物对应水化物的电离方程式为__ 。
③第三周期半径最大的金属元素__ ,该元素形成氢氧化物的电子式_ ,检验物质中是否含有该元素的方法是:__ 。
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是__ (写化学式)。该元素与硫元素相比,非金属性较强的元素是__ (填元素符号),请写出证明该结论的一个实验事实:__ 。
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是___ 。

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第__ 族,又有人提议可将它放在周期表中第IVA族,这样建议的原因是__ 。
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的__ (选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为
②与硅元素处于同一周期,两性金属元素是
③第三周期半径最大的金属元素
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图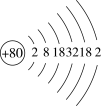 汞在第
汞在第___________ 周期。
(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷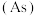 也是氮族元素。
也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是___________ (填序号)。
a、含有离子键和共价键
b、能与 溶液反应
溶液反应
c、与 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样
③砷酸 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:___________ 。
 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)据汞的原子结构示意图
 汞在第
汞在第(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷
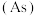 也是氮族元素。
也是氮族元素。①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是a、含有离子键和共价键
b、能与
 溶液反应
溶液反应c、与
 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样③砷酸
 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一种麻醉剂的分子结构式如图所示。其中, 的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于
的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于 的下一周期;元素
的下一周期;元素 的原子比
的原子比 原子多8个电子。则X、Y、Z、W、E分别为
原子多8个电子。则X、Y、Z、W、E分别为____________ 。
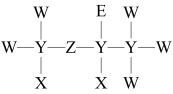
 的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于
的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于 的下一周期;元素
的下一周期;元素 的原子比
的原子比 原子多8个电子。则X、Y、Z、W、E分别为
原子多8个电子。则X、Y、Z、W、E分别为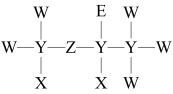
您最近一年使用:0次
【推荐2】回答下列问题:
(1)某元素的原子序数为33,该元素原子的价电子排布式为____ ,该元素原子核外有____ 个电子层,____ 个能级,____ 个原子轨道。
(2)D元素的正三价离子的3d能级为半充满,D的元素符号为____ ,其基态原子的电子排布式____ 。
(3)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为____ ,其基态原子的电子排布式为____ 。
(1)某元素的原子序数为33,该元素原子的价电子排布式为
(2)D元素的正三价离子的3d能级为半充满,D的元素符号为
(3)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表前三周期,针对表中的①~⑧元素,回答下列问题:
(1)元素④在周期表中的位置是________ 。
(2)在这些元素原子中,得电子能力最强的是______ (填元素符号)。
(3)单质化学性质最不活泼的元素是______ (填元素符号),元素②原子结构示意图为______ 。
(4)元素⑥、⑦形成的氢化物中,沸点高的是______ (填化学式)。
(5)元素①的最高价氧化物对应的水化物所含化学键的类型是_______ 。
(6)元素⑤最简单的氢化物和最高价氧化物对应的水化物相互反应的产物是_______ 。
(7)写出元素③的单质与稀盐酸反应的离子方程式_______ 。
⑤ | ⑥ | ||||||||||||||||
① | ② | ③ | ④ | ⑦ | ⑧ | ||||||||||||
(2)在这些元素原子中,得电子能力最强的是
(3)单质化学性质最不活泼的元素是
(4)元素⑥、⑦形成的氢化物中,沸点高的是
(5)元素①的最高价氧化物对应的水化物所含化学键的类型是
(6)元素⑤最简单的氢化物和最高价氧化物对应的水化物相互反应的产物是
(7)写出元素③的单质与稀盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.俄美科学家联合小组宣布合成出第114号元素(Fl)的一种新核素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中位置是___________ ,属于___________ 元素(填“金属”或“非金属”)。
(2)上述新核素的原子核内中子数为___________ 。
(3)如果该元素存在最高价氧化物,则它的化学式为___________ 。
Ⅱ.下图为元素周期表的一部分,该部分中8种元素的位置如图所示,试回答下列问题:

(1)8种元素中,原子半径最小的是___________ (填元素符号)。
(2)⑥⑦元素对应的简单氢化物最稳定的是___________ (填化学式)。
(3)②③④三种元素最高价氧化物对应水化物的碱性最强的是___________ (填化学式)。
(4)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为___________ 。
(5)元素②和⑤的最高价氧化物对应水化物之间反应的化学方程式为___________ 。
(1)该元素在周期表中位置是
(2)上述新核素的原子核内中子数为
(3)如果该元素存在最高价氧化物,则它的化学式为
Ⅱ.下图为元素周期表的一部分,该部分中8种元素的位置如图所示,试回答下列问题:

(1)8种元素中,原子半径最小的是
(2)⑥⑦元素对应的简单氢化物最稳定的是
(3)②③④三种元素最高价氧化物对应水化物的碱性最强的是
(4)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为
(5)元素②和⑤的最高价氧化物对应水化物之间反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:④_______ ;⑫________ 。
(2)画出原子的结构示意图:⑤_________ ;⑪________ 。
(3)在①~⑫元素中,金属性最强的元素是_________ ,非金属性最强的元素是_______ ,最不活泼的元素是________ (均填元素符号)。
(4)元素⑦与元素⑧相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是___________ (填序号)。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)元素⑥是构成地壳的主要元素之一,其氧化物是现代光学及光纤制品的基本原料,该氧化物的化学式为_____ 。且该氧化物可溶解在强碱NaOH中其离子方程式_______ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出下列元素符号:④
(2)画出原子的结构示意图:⑤
(3)在①~⑫元素中,金属性最强的元素是
(4)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)元素⑥是构成地壳的主要元素之一,其氧化物是现代光学及光纤制品的基本原料,该氧化物的化学式为
您最近一年使用:0次




