下列说法正确的有
①离子键的本质是静电作用
②任何物质中都存在化学键
③离子键就是阴、阳离子之间的静电吸引力
④活泼金属与活泼非金属化合时能形成离子键
⑤任何共价键中,成键原子成键后均满足 稳定结构
稳定结构
⑥验证化合物是否为离子化合物的实验方法是可以看其熔融状态下能否导电
⑦两种非金属元素形成的化合物不可能含有离子键
⑧化学键断裂,一定发生化学变化
①离子键的本质是静电作用
②任何物质中都存在化学键
③离子键就是阴、阳离子之间的静电吸引力
④活泼金属与活泼非金属化合时能形成离子键
⑤任何共价键中,成键原子成键后均满足
 稳定结构
稳定结构 ⑥验证化合物是否为离子化合物的实验方法是可以看其熔融状态下能否导电
⑦两种非金属元素形成的化合物不可能含有离子键
⑧化学键断裂,一定发生化学变化
| A.1个 | B.2个 | C.3个 | D.4个 |
更新时间:2024-03-05 11:23:33
|
相似题推荐
【推荐1】工业上通常利用反应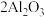 (熔融)
(熔融)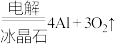 来获得单质铝,反应时还需要向
来获得单质铝,反应时还需要向 (熔点2050℃)中添加冰晶石(
(熔点2050℃)中添加冰晶石(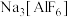 )以降低熔化温度。下列有关说法
)以降低熔化温度。下列有关说法不正确 的是
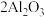 (熔融)
(熔融)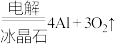 来获得单质铝,反应时还需要向
来获得单质铝,反应时还需要向 (熔点2050℃)中添加冰晶石(
(熔点2050℃)中添加冰晶石(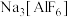 )以降低熔化温度。下列有关说法
)以降低熔化温度。下列有关说法A. 和 和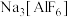 熔化时会破坏离子键 熔化时会破坏离子键 |
B.制得的Al是金属晶体,由“自由电子”和 之间强的相互作用而形成 之间强的相互作用而形成 |
| C.电解过程将电能转化为化学能 |
D.可将该反应中的 换成 换成 (熔点194℃)进行电解获得单质铝 (熔点194℃)进行电解获得单质铝 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列物质中,含有极性键的离子化合物是
| A.MgCl2 | B.HCl | C.H2O2 | D.NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.H2O的热稳定性比H2S强, 是由于H2O的分子间作用力较大 |
| B.KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物 |
| C.非极性键既可以存在单质中,也可以存在化合物中 |
| D.加热无水Na2CO3固体使之熔化,不需要破坏化学键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的的是
| A.只含非金属元素的化合物一定是共价化合物 |
| B.Na2CO3和CaCl2中化学键类型完全相同 |
| C.含有共价键的物质不一定是共价化合物 |
| D.溶于水能导电的化合物一定是电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】推理是化学学习中常用的思维方法,下列推理合理的是
| A.NaOH和CaCl2都是离子化合物,所以二者化学键类型相同 |
| B.可逆反应达平衡时,体系中各组分的浓度不再变化,可推知正、逆反应停止了 |
| C.原电池加快某些反应的速率,所以用锌与稀硫酸反应制取氢气常加入少量硫酸铜 |
| D.同条件下反应物浓度越大反应越快,所以铁在浓硝酸中比在稀硝酸中溶解得快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.HCl、HBr、HI的熔沸点依次增大,热稳定性也依次增强 |
| B.CO2和N2中,各原子的最外层都具有8电子稳定结构 |
| C.Na2O和Na2O2的阴、阳离子的个数比相同,化学键类型也相同 |
| D.MgF2既含有离子键又含有非极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关物质结构的说法中,正确的说法有
①两种非金属元素形成AB型化合物一定含共价键
②物质中化学键被破坏,一定发生化学变化
③水的沸点和稳定性都比硫化氢要高均与氢键有关
④CF4、CCl4、CBr4、CI4的分子间作用力依次增大,沸点依次升高
⑤只有活泼金属与活泼非金属之间才能形成离子键
⑥仅由非金属元素组成的化合物一定是共价化合物
⑦碘化氢气体分解和氯化钠熔化克服的化学键类型不同
⑧F2、PCl3、HClO分子中,每个原子的最外层都具有8电子稳定结构
⑨H2O2、NH4Cl、H2S、NaOH、Ca(ClO)2中都存在极性共价键
①两种非金属元素形成AB型化合物一定含共价键
②物质中化学键被破坏,一定发生化学变化
③水的沸点和稳定性都比硫化氢要高均与氢键有关
④CF4、CCl4、CBr4、CI4的分子间作用力依次增大,沸点依次升高
⑤只有活泼金属与活泼非金属之间才能形成离子键
⑥仅由非金属元素组成的化合物一定是共价化合物
⑦碘化氢气体分解和氯化钠熔化克服的化学键类型不同
⑧F2、PCl3、HClO分子中,每个原子的最外层都具有8电子稳定结构
⑨H2O2、NH4Cl、H2S、NaOH、Ca(ClO)2中都存在极性共价键
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次



