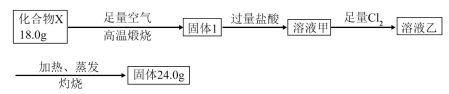
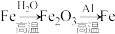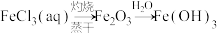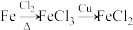聚合硫酸铁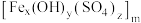 (铁元素化合价为
(铁元素化合价为 )是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁,配成 的溶液.
的溶液.
②准确量取 溶液,加入盐酸酸化的
溶液,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 .
.
③准确量取 溶液,加入足量的
溶液,加入足量的 溶液至沉淀完全,过滤、洗涤、灼烧至恒重,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、灼烧至恒重,得到红棕色固体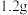 .
.
该聚合硫酸铁组成中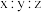 的值为
的值为
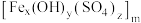 (铁元素化合价为
(铁元素化合价为 )是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁,配成
 的溶液.
的溶液.②准确量取
 溶液,加入盐酸酸化的
溶液,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 .
.③准确量取
 溶液,加入足量的
溶液,加入足量的 溶液至沉淀完全,过滤、洗涤、灼烧至恒重,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、灼烧至恒重,得到红棕色固体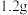 .
.该聚合硫酸铁组成中
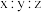 的值为
的值为A. | B.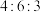 | C.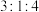 | D. |
更新时间:2024/03/07 19:12:50
|
相似题推荐
单选题-单题
|
较难
(0.4)
【推荐1】 表示阿伏加德罗常数,下列叙述正确的是
表示阿伏加德罗常数,下列叙述正确的是
 表示阿伏加德罗常数,下列叙述正确的是
表示阿伏加德罗常数,下列叙述正确的是A.0.2mol/LAlCl3溶液中Cl-物质的量为 |
B.标准状况下,22.4LCO2所含原子数为 |
C.足量的Cl2与5.6gFe完全反应时,转移的电子数为 |
D.7.8gNa2O2中含有的离子总数为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】CuSO4•5H2O在不同温度下分解情况不同,取5.00g该晶体在密闭容器中进行实验,测得分解后剩余固体质量与温度关系如图,下列说法不正确 的是
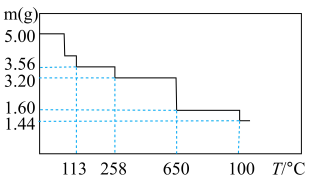

| A.113℃分解得到的固体产物为CuSO4•H2O |
| B.温度低于650℃时的分解反应,均不属于氧化还原反应 |
| C.650℃时的气态产物冷却至室温,可得组成为n(H2SO4):n(H2O)=1:4的硫酸溶液 |
| D.1000℃分解得到的固体产物为CuO |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】现取一定质量 、
、 和NaCl混合物,分为三等份,进行实验探究:
和NaCl混合物,分为三等份,进行实验探究:
实验一:将一份混合物溶于水,向其中加入适量 溶液,有白色沉淀X生成。
溶液,有白色沉淀X生成。
实验二:将另一份混合物溶于水,加入足量 溶液,有白色沉淀Y生成。
溶液,有白色沉淀Y生成。
实验三:将第三份混合物溶于25mL 盐酸中,生成0.56L(标准状况下)气体,并得到溶液Z,测得溶液Z中
盐酸中,生成0.56L(标准状况下)气体,并得到溶液Z,测得溶液Z中 为
为 (溶解少量固体和产生气体后溶液体积的变化可忽略不计)。下列说法正确的是
(溶解少量固体和产生气体后溶液体积的变化可忽略不计)。下列说法正确的是
 、
、 和NaCl混合物,分为三等份,进行实验探究:
和NaCl混合物,分为三等份,进行实验探究:实验一:将一份混合物溶于水,向其中加入适量
 溶液,有白色沉淀X生成。
溶液,有白色沉淀X生成。实验二:将另一份混合物溶于水,加入足量
 溶液,有白色沉淀Y生成。
溶液,有白色沉淀Y生成。实验三:将第三份混合物溶于25mL
 盐酸中,生成0.56L(标准状况下)气体,并得到溶液Z,测得溶液Z中
盐酸中,生成0.56L(标准状况下)气体,并得到溶液Z,测得溶液Z中 为
为 (溶解少量固体和产生气体后溶液体积的变化可忽略不计)。下列说法正确的是
(溶解少量固体和产生气体后溶液体积的变化可忽略不计)。下列说法正确的是| A.实验一中白色沉淀X为AgCl |
| B.实验二可得到4.925g白色沉淀Y |
C.原混合物中 、 、 的物质的量之比为2:3 的物质的量之比为2:3 |
D.若溶液Z中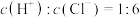 ,则原混合物中有0.06molNaCl ,则原混合物中有0.06molNaCl |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】向含Na2CO3、Na[Al(OH)4](NaAlO2)的混合溶液中逐滴加入150mL1mol·L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是
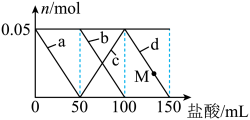

| A.a曲线表示的离子方程式为:[Al(OH)4]-+H+=Al(OH)3↓+H2O |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时,溶液中沉淀的质量为3.9g |
D.原混合溶液中的CO 与[Al(OH)4]-的物质的量之比为1∶2 与[Al(OH)4]-的物质的量之比为1∶2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合下图。其中甲和X可能是
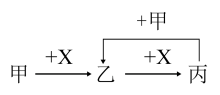

| A.甲为Fe、X为Cl2 | B.甲为S、X为O2 |
| C.甲为SO2、X为NaOH溶液 | D.甲为AlCl3溶液、X为NH3·H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】铁是人体必需的微量元素之一,某小组设计实验测定菠菜中铁的含量(mg/100g,即每100g菠菜中铁元素的质量),实验过程如图:
I.配制溶液

II.测定含量
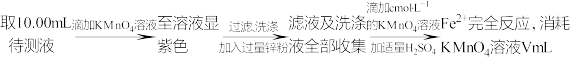 下列说法正确的是
下列说法正确的是
I.配制溶液

II.测定含量
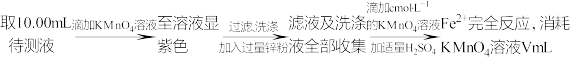 下列说法正确的是
下列说法正确的是| A.灼烧时用到的主要仪器有:蒸发皿、三脚架、泥三角、酒精灯 |
| B.该菠菜中铁的含量为2800cVmg/100g |
| C.取少量待测液滴加KSCN溶液,溶液变为红色则含有Fe2+ |
| D.配制100mL待测液时,若仰视容量瓶上的刻度线,浓度偏高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100 mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如图所示。则原H2SO4物质的量浓度是
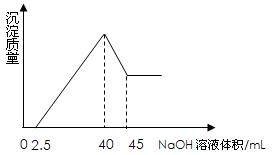

| A.1mol/L | B.2mol/L | C.3mol/L | D.4mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】有600 mL某种混合物溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现将此溶液分成三等份,进行如下实验:
(1)向第一份中加入AgNO3溶液,有沉淀产生;
(2)向第二份中加足量NaOH溶液并加热后,收集到气体0.04 mol;
(3)向第三份中加足量BaCl2溶液后,得干燥的沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。 根据上述实验现象,以下推测正确的是
(1)向第一份中加入AgNO3溶液,有沉淀产生;
(2)向第二份中加足量NaOH溶液并加热后,收集到气体0.04 mol;
(3)向第三份中加足量BaCl2溶液后,得干燥的沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。 根据上述实验现象,以下推测正确的是
| A.K+不一定存在 | B.Ba2+、Mg2+不一定都存在 |
| C.Cl-不一定存在 | D.混合溶液中CO32-的浓度为0.2 mol/L |
您最近一年使用:0次

 的物质的量相同;
的物质的量相同; 和14g
和14g 的体积相同;
的体积相同; 、Ba2+、
、Ba2+、 、
、 、Cl-中的若干种,取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。已知:
、Cl-中的若干种,取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。已知: NH3+ H2O。下列说法中不正确的是
NH3+ H2O。下列说法中不正确的是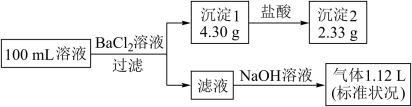
 可用作净水剂,
可用作净水剂, 胶体,碱性条件下KClO氧化性大于
胶体,碱性条件下KClO氧化性大于