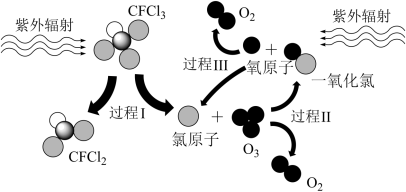
某温度下,关于可逆反应mA(g)+nB(g)⇌pC(g) ΔH<0,下列说法正确的是
| A.其他条件不变,升高温度,活化能减小,活化分子百分数增加,速率增大 |
| B.其他条件不变,恒容条件下,通入稀有气体(不参加反应),正、逆反应速率均增大 |
| C.其他条件不变,减小C(g)的浓度,正反应速率增大,逆反应速率减小 |
| D.其他条件不变,压缩体积增大压强,活化分子百分数不变,有效碰撞几率增加 |
更新时间:2024-03-15 08:03:16
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】在一定温度下,某密闭容器中发生反应:2C(g) A(g)+2B(s) △H>0,若0~10s内c(C)由0.1mol/L降到0.08mol/L,则下列说法正确的是
A(g)+2B(s) △H>0,若0~10s内c(C)由0.1mol/L降到0.08mol/L,则下列说法正确的是
 A(g)+2B(s) △H>0,若0~10s内c(C)由0.1mol/L降到0.08mol/L,则下列说法正确的是
A(g)+2B(s) △H>0,若0~10s内c(C)由0.1mol/L降到0.08mol/L,则下列说法正确的是| A.0~10s内用B表示的平均反应速率为v(B)=0.002mol•L-1•s-1 |
| B.c(C)由0.05mol/L降到0.04mol/L所需的反应时间小于5s |
| C.升高温度正反应速率加快,逆反应速率减慢 |
| D.减小反应体系的体积,化学反应速率加快 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】北京化工大学研究了过渡金属Pd8簇催化乙炔氢化的反应机理,Pd8簇上的反应中间体亚乙烯基吸附物R,多步连续加氢反应路径的能量变化示意图如下(TS为过渡态,M为中间体)。下列说法错误的是


| A.乙炔与氢气生成乙烷的反应为加成反应 |
| B.图示反应历程中,最大能垒的反应过程为IM1到TS2 |
| C.生产中将催化剂处理成纳米级颗粒可提高乙炔的平衡转化率 |
| D.乙炔氢化历程中涉及非极性键的断裂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法正确的是
| A.化学反应都伴有能量变化 |
| B.使用催化剂可以改变反应的平衡常数 |
| C.升高温度使反应加快,是因为降低了反应的活化能 |
| D.对于同一个化学反应,从反应物到生成物是一步完成还是几步完成,过程不同焓变也不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于有效碰撞理论的说法一定正确的是
| A.活化分子之间发生的碰撞一定是有效碰撞 |
| B.增大压强,反应的有效碰撞次数增多,反应速率加快 |
| C.升高温度,反应的活化能降低,反应速率加快 |
| D.使用催化剂,单位体积内活化分子数增多,反应速率加快 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下图体现了有无催化剂参与反应过程的能量变化图。下列有关说法正确的是( )
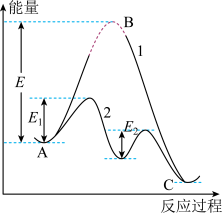

| A.使用催化剂能够加快反应的速率,根本上是由于催化剂降低了正逆反应的活化能 |
| B.C(s)+H2O(g)=CO(g)+H2(g),该反应过程可用上图图象表示 |
| C.使用催化剂不仅能加快反应速率,而且可以让不可能发生的反应发生,如利用催化技术处理汽车尾气:2CO+2NO===2CO2+N2 |
| D.化学反应的本质是旧键的断裂、新键的生成,如图可知反应的能量变化由旧键断裂释放的能量和新键形成吸收的能量大小决定 |
您最近一年使用:0次