已知乙醇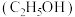 能与
能与 和
和 的混合溶液在一定条件下发生反应:
的混合溶液在一定条件下发生反应: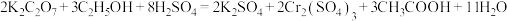 ,
, 和
和 在溶液中分别显橙色和绿色,回答下列问题:
在溶液中分别显橙色和绿色,回答下列问题:
(1)该反应现象是___________ 。
(2)该反应___________ (填“是”或“不是”)氧化还原反应,判断的依据是___________ 。
(3)你认为能否用这一反应来检测司机是否酒后驾车?___________ (填“能”或“不能”),简述其原理:___________ 。
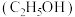 能与
能与 和
和 的混合溶液在一定条件下发生反应:
的混合溶液在一定条件下发生反应: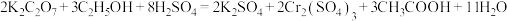 ,
, 和
和 在溶液中分别显橙色和绿色,回答下列问题:
在溶液中分别显橙色和绿色,回答下列问题:(1)该反应现象是
(2)该反应
(3)你认为能否用这一反应来检测司机是否酒后驾车?
更新时间:2024-04-04 00:40:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知反应4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(1)在该反应中氧化剂是___ ,还原剂是___ ,1摩尔氧气完全参与反应,转移电子数目___ 。
(2)用双线桥标出该反应的电子转移方向及数目_____________ ,4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(3)该反应中氧化剂与氧化产物的氧化性由强到弱的关系是__________ 。
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3 + C+S = K2S + 2NO2↑ + CO2↑。其中被还原的元素是____ ,被氧化的元素是____ ,氧化剂是___ ,还原剂是____ ,氧化产物是____ ,还原产物是_______ 。
(1)在该反应中氧化剂是
(2)用双线桥标出该反应的电子转移方向及数目
(3)该反应中氧化剂与氧化产物的氧化性由强到弱的关系是
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3 + C+S = K2S + 2NO2↑ + CO2↑。其中被还原的元素是
您最近一年使用:0次
【推荐2】按要求填空:
(1)在S2-、Fe2+、Mg2+、S、I- 、H+ 中,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO +HNO3 →N2O3+ H2O;②NH3 +NO→HNO2+ H2O;③N2O4 +H2O→HNO3 + HNO2
其中你认为一定不可能实现的是___________ 。
(3)用双线桥标出方程式6HCl+KClO3=KCl+3Cl2↑+3H2O 中电子转移的方向和数目___________ ,该反应中若生成 426g Cl2,则被氧化的HCl的有多少___________ g。
(4)As2O3、Zn、AsH3 (气态)、ZnSO4、H2SO4、H2O组成的一个氧化还原反应体系中,已知As2O3作氧化剂, ZnSO4 作氧化产物。该反应的化学反应方程式为:___________ 。
(5)已知氧化性:Cl2 > Br2 > Fe3+ > I2,写出下列离子方程式:
a.少量氯气与FeI2溶液反应:___________ 。
b.氯气与FeBr2溶液以按个数比 1∶1 反应:___________ 。
(6)新型纳米材料氧缺位铁酸盐(MFe2Ox,3 < x < 4,M=Mn,Zn,Ni且均为+2 价,下同)是由铁酸盐 MFe2O4 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于___________ ,铁酸盐MFe2O4经过高温反应得到 MFe2Ox的反应属于___________ (填“氧化还原”或“非氧化还原”)反应。
(7)在酸性条件下。 容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子,
容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子, 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是___________ 。
(1)在S2-、Fe2+、Mg2+、S、I- 、H+ 中,既有氧化性又有还原性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO +HNO3 →N2O3+ H2O;②NH3 +NO→HNO2+ H2O;③N2O4 +H2O→HNO3 + HNO2
其中你认为一定不可能实现的是
(3)用双线桥标出方程式6HCl+KClO3=KCl+3Cl2↑+3H2O 中电子转移的方向和数目
(4)As2O3、Zn、AsH3 (气态)、ZnSO4、H2SO4、H2O组成的一个氧化还原反应体系中,已知As2O3作氧化剂, ZnSO4 作氧化产物。该反应的化学反应方程式为:
(5)已知氧化性:Cl2 > Br2 > Fe3+ > I2,写出下列离子方程式:
a.少量氯气与FeI2溶液反应:
b.氯气与FeBr2溶液以按个数比 1∶1 反应:
(6)新型纳米材料氧缺位铁酸盐(MFe2Ox,3 < x < 4,M=Mn,Zn,Ni且均为+2 价,下同)是由铁酸盐 MFe2O4 经过高温反应得到的。将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于
(7)在酸性条件下。
 容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子,
容易转化为 Fe2+,某反应体系中共存在下列 6 种粒子, 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的还原剂是
您最近一年使用:0次
【推荐3】K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
(1)该反应中的还原剂是________________ 。
(2)若司机酒后开车,检测仪器内物质显示出____________ 色。
(3)在反应中,铬元素的化合价从_______ 价变为________ 价。
(4)写出并配平该反应的化学方程式________________ 。
(5)如果在反应中生成1mol氧化产物,转移的电子总数为_____________ 。
(1)该反应中的还原剂是
(2)若司机酒后开车,检测仪器内物质显示出
(3)在反应中,铬元素的化合价从
(4)写出并配平该反应的化学方程式
(5)如果在反应中生成1mol氧化产物,转移的电子总数为
您最近一年使用:0次
填空题
|
适中
(0.65)
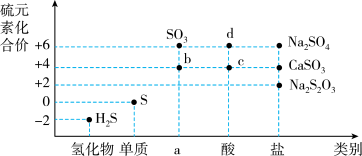
【推荐1】物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据图正确回答下列含硫物质有关问题。
(1)a对应物质的类别是___________ ;
(2)图中 b、c、d 这三种物质中属于弱电解质的是_______________ (填化学式)。
(3)欲制备Na2S2O3(硫代硫酸钠),根据价类二维图信息分析,合理的是_______。
(4)请结合SO2类别、价态及特性,在如下图实验装置分析SO2的性质(经检验,装置的气密性良好)。
①是检验SO2的___________ 。
②中的现象褪色,体现了SO2的___________ 。
③中产生淡黄色浑浊,体现了SO2的___________ 。
(5)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
产生沉淀的化学式是:①___________ ,②___________ 。
(6)写出SO2与氢氧化钠溶液反应的化学方程式______________ 。
(1)a对应物质的类别是
(2)图中 b、c、d 这三种物质中属于弱电解质的是
(3)欲制备Na2S2O3(硫代硫酸钠),根据价类二维图信息分析,合理的是_______。
| A.Na2S+S | B.Na2SO3+S |
| C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
(4)请结合SO2类别、价态及特性,在如下图实验装置分析SO2的性质(经检验,装置的气密性良好)。

①是检验SO2的
②中的现象褪色,体现了SO2的
③中产生淡黄色浑浊,体现了SO2的
(5)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
| 加入的物质 | H2O2 | 氨水 |
| 沉淀的化学式 | ① | ② |
(6)写出SO2与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式正确的是_______ 。
A.(2023·浙江卷)碘化亚铁溶液与等物质的量的氯气:
B.(2023·浙江卷)向次氯酸钙溶液通入足量二氧化碳: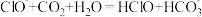
C.(2022·全国卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO4↓+2H2O
=BaSO4↓+2H2O
D.(2021·全国卷)硫酸铝溶液中滴加少量氢氧化钾溶液: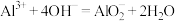
E.(2021·湖北卷)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO
A.(2023·浙江卷)碘化亚铁溶液与等物质的量的氯气:

B.(2023·浙江卷)向次氯酸钙溶液通入足量二氧化碳:
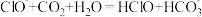
C.(2022·全国卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
 =BaSO4↓+2H2O
=BaSO4↓+2H2OD.(2021·全国卷)硫酸铝溶液中滴加少量氢氧化钾溶液:
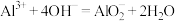
E.(2021·湖北卷)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】乙烯和乙醇是重要的有机化合物。请根据题意填空:
(1)乙烯的分子式为_______ (如乙烷的分子式为C2H6);
(2)将乙烯通入溴水中,溴水逐渐褪色。请写出相关化学方程式:_______ ;
(3)乙醇的官能团为_______ ;
(4)交警查酒驾,通常让司机向盛有酸性重铬酸钾的测试仪吹气,若变色,说明司机饮了酒。该过程中乙醇被_______ (填“氧化”或者“还原”);
(5)乙醇和乙酸能发生酯化反应,生成物乙酸乙酯的结构简式为_______ 。
(1)乙烯的分子式为
(2)将乙烯通入溴水中,溴水逐渐褪色。请写出相关化学方程式:
(3)乙醇的官能团为
(4)交警查酒驾,通常让司机向盛有酸性重铬酸钾的测试仪吹气,若变色,说明司机饮了酒。该过程中乙醇被
(5)乙醇和乙酸能发生酯化反应,生成物乙酸乙酯的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)下图A、B、C、D分别是四种有机物的分子结构模型,请回答下列问题:

①图中A是有机物分子的______ 模型。上述有机物中,所有原子均共平面的是______ (填有机物的名称)
②下列关于D的叙述正确的是_______ (填序号)。
a.D能使酸性高锰酸钾溶液褪色
b.D的水溶液可用于消毒,95%的D溶液消毒效果最好
c.一定条件下,由C生成D的反应原子利用率为100%
d.向盛有溴水的试管中加入适量D,充分振荡后静置,溶液分层,上层呈橙红色
③B的最简单同系物与足量氢气加成后的产物的一氯代物有_____ 种。
(2)2 L某烷烃的蒸气完全燃烧时,消耗同温同压下16 L氧气,该烷烃的分子式为______ ,其同分异构体中沸点最低的叫______ (习惯命名法)。
(3)某烷烃分子中C—H键个数比C—C键个数多了10,该烷烃同分异构体中含有3个甲基的有_____ 种。

①图中A是有机物分子的
②下列关于D的叙述正确的是
a.D能使酸性高锰酸钾溶液褪色
b.D的水溶液可用于消毒,95%的D溶液消毒效果最好
c.一定条件下,由C生成D的反应原子利用率为100%
d.向盛有溴水的试管中加入适量D,充分振荡后静置,溶液分层,上层呈橙红色
③B的最简单同系物与足量氢气加成后的产物的一氯代物有
(2)2 L某烷烃的蒸气完全燃烧时,消耗同温同压下16 L氧气,该烷烃的分子式为
(3)某烷烃分子中C—H键个数比C—C键个数多了10,该烷烃同分异构体中含有3个甲基的有
您最近一年使用:0次
【推荐3】K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
(1)该反应中的还原剂是________________ 。
(2)若司机酒后开车,检测仪器内物质显示出____________ 色。
(3)在反应中,铬元素的化合价从_______ 价变为________ 价。
(4)写出并配平该反应的化学方程式________________ 。
(5)如果在反应中生成1mol氧化产物,转移的电子总数为_____________ 。
(1)该反应中的还原剂是
(2)若司机酒后开车,检测仪器内物质显示出
(3)在反应中,铬元素的化合价从
(4)写出并配平该反应的化学方程式
(5)如果在反应中生成1mol氧化产物,转移的电子总数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】小组同学探究+3价铬元素和+6价铬元素的相互转化。
资料: (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (砖红色,难溶于水)
(砖红色,难溶于水)
实验Ⅰ:向 溶液中滴入
溶液中滴入 溶液,无明显变化,得到溶液a,取少量溶液a,加入
溶液,无明显变化,得到溶液a,取少量溶液a,加入 溶液,未观察到砖红色沉淀。
溶液,未观察到砖红色沉淀。
实验Ⅱ:向溶液a中加入 溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为
溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为 ,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的
,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的 约为3,再加入
约为3,再加入 溶液,有砖红色沉淀生成。
溶液,有砖红色沉淀生成。
(1)实验Ⅱ中加入稀硫酸的目的是___________ 。
(2)甲同学认为实验Ⅱ中溶液变黄生成 的原因是
的原因是 将+3价铬元素氧化为
将+3价铬元素氧化为 ,乙同学认为该说法不严谨。乙的理由是
,乙同学认为该说法不严谨。乙的理由是___________ 。
(3)对比实验Ⅰ和Ⅱ,小组同学研究碱性环境对+3价铬元素或 性质的影响。
性质的影响。
①提出假设:
假设a:碱性增强, 的氧化性增强
的氧化性增强
假设b:___________ 。
② 参与的电极反应式是
参与的电极反应式是___________ ,据此分析,假设a不成立。
实验Ⅲ:向实验Ⅱ中的黄色溶液中加入稀硫酸,溶液变为橙色,再加入 溶液,溶液最终变为绿色,有气泡生成。
溶液,溶液最终变为绿色,有气泡生成。
(4)实验Ⅲ中溶液由橙色变为绿色的离子方程式是___________ 。
(5)综上, 在+3价铬元素和+6价铬元素相互转化中的作用是
在+3价铬元素和+6价铬元素相互转化中的作用是___________ 。
资料:
 (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (砖红色,难溶于水)
(砖红色,难溶于水)实验Ⅰ:向
 溶液中滴入
溶液中滴入 溶液,无明显变化,得到溶液a,取少量溶液a,加入
溶液,无明显变化,得到溶液a,取少量溶液a,加入 溶液,未观察到砖红色沉淀。
溶液,未观察到砖红色沉淀。实验Ⅱ:向溶液a中加入
 溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为
溶液,产生少量气泡,水浴加热,有大量气泡产生,经检验气体为 ,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的
,溶液最终变为黄色。取少量黄色溶液,加入稀硫酸调节溶液的 约为3,再加入
约为3,再加入 溶液,有砖红色沉淀生成。
溶液,有砖红色沉淀生成。(1)实验Ⅱ中加入稀硫酸的目的是
(2)甲同学认为实验Ⅱ中溶液变黄生成
 的原因是
的原因是 将+3价铬元素氧化为
将+3价铬元素氧化为 ,乙同学认为该说法不严谨。乙的理由是
,乙同学认为该说法不严谨。乙的理由是(3)对比实验Ⅰ和Ⅱ,小组同学研究碱性环境对+3价铬元素或
 性质的影响。
性质的影响。①提出假设:
假设a:碱性增强,
 的氧化性增强
的氧化性增强假设b:
②
 参与的电极反应式是
参与的电极反应式是实验Ⅲ:向实验Ⅱ中的黄色溶液中加入稀硫酸,溶液变为橙色,再加入
 溶液,溶液最终变为绿色,有气泡生成。
溶液,溶液最终变为绿色,有气泡生成。(4)实验Ⅲ中溶液由橙色变为绿色的离子方程式是
(5)综上,
 在+3价铬元素和+6价铬元素相互转化中的作用是
在+3价铬元素和+6价铬元素相互转化中的作用是
您最近一年使用:0次



