K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
(1)该反应中的还原剂是________________ 。
(2)若司机酒后开车,检测仪器内物质显示出____________ 色。
(3)在反应中,铬元素的化合价从_______ 价变为________ 价。
(4)写出并配平该反应的化学方程式________________ 。
(5)如果在反应中生成1mol氧化产物,转移的电子总数为_____________ 。
(1)该反应中的还原剂是
(2)若司机酒后开车,检测仪器内物质显示出
(3)在反应中,铬元素的化合价从
(4)写出并配平该反应的化学方程式
(5)如果在反应中生成1mol氧化产物,转移的电子总数为
9-10高三·福建厦门·阶段练习 查看更多[2]
更新时间:2016-12-09 00:55:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氧化还原反应在高中化学中是一类重要的反应类型。 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:
(1)下列基本反应类型中一定属于氧化还原反应的是___________(填字母)。
(2)实验室迅速制备少量氯气可利用如下反应: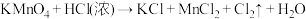 (未配平)
(未配平)
①上述反应中被还原的元素为___________ (填元素符号)。
② 与
与 反应生成
反应生成 ,反应后
,反应后 转化为
转化为___________ , 发生
发生___________ 反应(填“氧化”或“还原”)。
(3) 溶液能与
溶液能与 反应制作印刷电路板,其制作原理可用
反应制作印刷电路板,其制作原理可用 表示。
表示。
①上式中X的化学式为___________ 。
②若有 铜被氧化,则参与反应的
铜被氧化,则参与反应的 的质量为
的质量为___________ g。
③该反应的离子方程式为___________ 。
(4)已知方程式: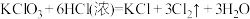 。用双线桥法标出电子转移的方向和数目:
。用双线桥法标出电子转移的方向和数目:___________ 。
(5)某反应的反应物与生成物有 ,已知氧化性:K2Cr2O7>Cl2,写出并配平该化学方程式:
,已知氧化性:K2Cr2O7>Cl2,写出并配平该化学方程式:___________ 。
 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:(1)下列基本反应类型中一定属于氧化还原反应的是___________(填字母)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
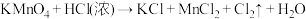 (未配平)
(未配平)①上述反应中被还原的元素为
②
 与
与 反应生成
反应生成 ,反应后
,反应后 转化为
转化为 发生
发生(3)
 溶液能与
溶液能与 反应制作印刷电路板,其制作原理可用
反应制作印刷电路板,其制作原理可用 表示。
表示。①上式中X的化学式为
②若有
 铜被氧化,则参与反应的
铜被氧化,则参与反应的 的质量为
的质量为③该反应的离子方程式为
(4)已知方程式:
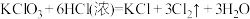 。用双线桥法标出电子转移的方向和数目:
。用双线桥法标出电子转移的方向和数目:(5)某反应的反应物与生成物有
 ,已知氧化性:K2Cr2O7>Cl2,写出并配平该化学方程式:
,已知氧化性:K2Cr2O7>Cl2,写出并配平该化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,有研究人员提出,在碱性条件下用铝粉将
的浓度,有研究人员提出,在碱性条件下用铝粉将 转化为无毒的
转化为无毒的 ,其化学方程式为
,其化学方程式为 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,氧化剂是______ ;______ 发生氧化反应。
(2)用双线桥法表示出反应中电子转移的方向和数目_____ 。
(3)上述反应的离子方程式为______ 。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,有研究人员提出,在碱性条件下用铝粉将
的浓度,有研究人员提出,在碱性条件下用铝粉将 转化为无毒的
转化为无毒的 ,其化学方程式为
,其化学方程式为 。请回答下列问题:
。请回答下列问题:(1)上述反应中,氧化剂是
(2)用双线桥法表示出反应中电子转移的方向和数目
(3)上述反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】建筑工地常用的 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应:
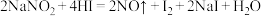 。(已知:淀粉遇
。(已知:淀粉遇 变蓝色)
变蓝色)
(1)上述反应的还原化剂是___________ 。
(2)用双线桥法标出上述反应电子转移的方向与数目:
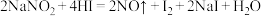
___________ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别 和NaCl,实验可选用的物质有:①水;②淀粉碘化钾试纸;③淀粉;④白酒;⑤食醋,下列几组合适的是___________(填字母)。
和NaCl,实验可选用的物质有:①水;②淀粉碘化钾试纸;③淀粉;④白酒;⑤食醋,下列几组合适的是___________(填字母)。
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: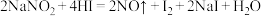 。(已知:淀粉遇
。(已知:淀粉遇 变蓝色)
变蓝色)(1)上述反应的还原化剂是
(2)用双线桥法标出上述反应电子转移的方向与数目:
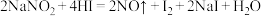
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别
 和NaCl,实验可选用的物质有:①水;②淀粉碘化钾试纸;③淀粉;④白酒;⑤食醋,下列几组合适的是___________(填字母)。
和NaCl,实验可选用的物质有:①水;②淀粉碘化钾试纸;③淀粉;④白酒;⑤食醋,下列几组合适的是___________(填字母)。| A.③⑤ | B.①②⑤ | C.①②④ | D.①②③⑤ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________ 。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_____CuSO4+_____PH3+_____H2O=_____Cu3P↓+_____H3PO4+_____H2SO4,_____
有0.4mol电子转移时被氧化的PH3的物质的量为________ mol。
(3)工业制备PH3的流程如图所示。
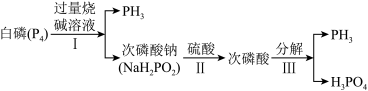
①次磷酸属于________ 元酸。
②白磷和烧碱溶液反应的化学方程式为:_________________ 。
③若起始时有1 mol P4参加反应,则整个工业流程中共生成________ mol PH3。
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_____CuSO4+_____PH3+_____H2O=_____Cu3P↓+_____H3PO4+_____H2SO4,
有0.4mol电子转移时被氧化的PH3的物质的量为
(3)工业制备PH3的流程如图所示。

①次磷酸属于
②白磷和烧碱溶液反应的化学方程式为:
③若起始时有1 mol P4参加反应,则整个工业流程中共生成
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜广泛应用于电气、轻工、机械制造、国防工业等。回答下列问题:

(1)用黄铜矿冶铜原理如图所示。
①CuFeS2中Fe的化合价为___________ 。
②反应III的化学方程式为___________ 。
(2)铜锈中有无害的Cu2(OH)2CO3和有害的“粉状锈”[Cu2(OH)3Cl]。
①Cu2(OH)2CO3和Cu2(OH)3Cl均属于______ (填“正”、“酸式”或“碱式”)盐;CuCl在湿的空气中生成Cu2(OH)3Cl的反应中,CuCl作________ 。(填“氧化剂”或“还原剂”)
②上述流程图中涉及的物质中属于酸性氧化物的是______ ,属于碱性氧化物的是______ 。

(1)用黄铜矿冶铜原理如图所示。
①CuFeS2中Fe的化合价为
②反应III的化学方程式为
(2)铜锈中有无害的Cu2(OH)2CO3和有害的“粉状锈”[Cu2(OH)3Cl]。
①Cu2(OH)2CO3和Cu2(OH)3Cl均属于
②上述流程图中涉及的物质中属于酸性氧化物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列物质(括号内为对应物质的主要成分):a.熔融NaOH;b.医用酒精;c.蔗糖晶体;d.加碘盐(NaCl和KIO3);e.“84”消毒液(NaClO);f.小苏打(NaHCO3);g.洁厕灵(HCl),回答下列问题:
(1)上述状态下的物质中,属于电解质且能导电的是_______ (填字母,下同);d和f均为厨房中的常用物质,可用于区分两者的物质是________ 。
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:________ 。
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:___________ ;该反应中被氧化的Ⅰ原子与被还原的Ⅰ原子的个数之比为___________ 。
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:_____ ,__NaClO2+__NaHSO4=___ClO2+___NaCl+__Na2SO4+____H2O;若每片泡腾片中NaClO2的质量分数≥17%为合格品,上述所得ClO2溶液的物质的量浓度为0.002mol/L,则所用泡腾片____ (填“属于”或“不属于”)合格品。
(1)上述状态下的物质中,属于电解质且能导电的是
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,Fe2O3 + 3CO 2Fe + 3CO2反应中,
2Fe + 3CO2反应中,__________ (填名称)是氧化剂,_______ (填化学式)发生氧化反应,_________ (填元素符号)元素被氧化,生成42g Fe时转移的电子的物质的量是_____________ mol .
 2Fe + 3CO2反应中,
2Fe + 3CO2反应中,
您最近一年使用:0次
【推荐3】回答下列问题
(1)已知某反应体系中有如下反应物和生成物: ,和一种未知物质X,X是一种气态单质,其密度是相同条件下H2密度的35.5倍
,和一种未知物质X,X是一种气态单质,其密度是相同条件下H2密度的35.5倍
①已知KMnO4 在反应中得电子,写出该反应的化学方程式_________
②已知当生成标准状况下2.24L气体X时,消耗的氧化剂的物质的量为_________
③根据该反应事实可知_________
A.氧化性:X>KMnO4 B.氧化性:KMnO4 >X
C.还原性:HCl>MnCl2 D.还原性:MnCl2 > HCl
(2)配平下列离子反应方程式
①_____KI+_____KIO3+_____H2SO4___________I2+_____K2SO4+_____H2O;____
②_____S+_____KOH___________K2S+_____K2SO3+_____H2O;_________
③_____ClO +_____Fe2++________Cl-+_____Fe3++______________;
+_____Fe2++________Cl-+_____Fe3++______________;_________
(1)已知某反应体系中有如下反应物和生成物:
 ,和一种未知物质X,X是一种气态单质,其密度是相同条件下H2密度的35.5倍
,和一种未知物质X,X是一种气态单质,其密度是相同条件下H2密度的35.5倍①已知KMnO4 在反应中得电子,写出该反应的化学方程式
②已知当生成标准状况下2.24L气体X时,消耗的氧化剂的物质的量为
③根据该反应事实可知
A.氧化性:X>KMnO4 B.氧化性:KMnO4 >X
C.还原性:HCl>MnCl2 D.还原性:MnCl2 > HCl
(2)配平下列离子反应方程式
①_____KI+_____KIO3+_____H2SO4___________I2+_____K2SO4+_____H2O;
②_____S+_____KOH___________K2S+_____K2SO3+_____H2O;
③_____ClO
 +_____Fe2++________Cl-+_____Fe3++______________;
+_____Fe2++________Cl-+_____Fe3++______________;
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】交警常用“司机饮酒检测仪”检查司机是否酒后驾车,其原理是硫酸酸化的重铬酸盐( 橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬。请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是_____________________ 。
(2)写出碳和重铬酸钠高温反应的化学方程式______________________ 。
Cr2O3经铝热法还原制得金属铬的化学方程式是__________________ 。
(3)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是_________ 。
(4)某Na2Cr2O7样品2.00 g恰好和4.56 gFeSO4完全反应,该样品的纯度为___________ 。
 橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬。请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是
(2)写出碳和重铬酸钠高温反应的化学方程式
Cr2O3经铝热法还原制得金属铬的化学方程式是
(3)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是
(4)某Na2Cr2O7样品2.00 g恰好和4.56 gFeSO4完全反应,该样品的纯度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙烯和乙醇是重要的有机化合物。请根据题意填空:
(1)乙烯的分子式为_______ (如乙烷的分子式为C2H6);
(2)将乙烯通入溴水中,溴水逐渐褪色。请写出相关化学方程式:_______ ;
(3)乙醇的官能团为_______ ;
(4)交警查酒驾,通常让司机向盛有酸性重铬酸钾的测试仪吹气,若变色,说明司机饮了酒。该过程中乙醇被_______ (填“氧化”或者“还原”);
(5)乙醇和乙酸能发生酯化反应,生成物乙酸乙酯的结构简式为_______ 。
(1)乙烯的分子式为
(2)将乙烯通入溴水中,溴水逐渐褪色。请写出相关化学方程式:
(3)乙醇的官能团为
(4)交警查酒驾,通常让司机向盛有酸性重铬酸钾的测试仪吹气,若变色,说明司机饮了酒。该过程中乙醇被
(5)乙醇和乙酸能发生酯化反应,生成物乙酸乙酯的结构简式为
您最近一年使用:0次
【推荐3】I写出最简单的有机化合物的结构式:_________ 。
II已知:①气态烃A在标准状况下的密度为1.25g/L
②2CH3CHO+O2 2CH3COOH;
2CH3COOH;
A物质与其他物质的转化关系如图所示:CH3COOH←CH3CHO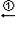 C2H5OH
C2H5OH 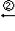 A
A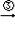 C2H5Br则:
C2H5Br则:
(1)A的结构简式为__ .
(2)反应①的化学方程式为______________________ .
(3)反应③的化学方程式为_____________________ ,反应类型为______ .
II已知:①气态烃A在标准状况下的密度为1.25g/L
②2CH3CHO+O2
 2CH3COOH;
2CH3COOH;A物质与其他物质的转化关系如图所示:CH3COOH←CH3CHO
 C2H5OH
C2H5OH  A
A C2H5Br则:
C2H5Br则:(1)A的结构简式为
(2)反应①的化学方程式为
(3)反应③的化学方程式为
您最近一年使用:0次



