第19届杭州亚运会开幕式首次使用废碳再生的绿色甲醇作为主火炬塔燃料。某化学兴趣小组设计如图所示装置来模拟 合成甲醇。
合成甲醇。

回答下列问题:
(1)仪器D的名称为___________ 。
(2)为除HCl,仪器B中应盛装的试剂是___________ 。
(3)使A中反应顺利进行的操作为___________ ,加快A中反应的方法是___________ 。
(4)C中主要生成甲醇,该反应的化学方程式为___________ 。
(5)E中接收的液体中甲醇的检测方法为___________ (写出一种即可)。
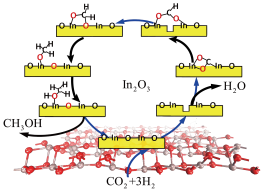
(6)合成甲醇过程的催化机理如图所示。在该历程中,优先与催化剂反应的物质是___________ ;生成的甲醇分子的氧原子来自___________ 。(填化学式)
 合成甲醇。
合成甲醇。
回答下列问题:
(1)仪器D的名称为
(2)为除HCl,仪器B中应盛装的试剂是
(3)使A中反应顺利进行的操作为
(4)C中主要生成甲醇,该反应的化学方程式为
(5)E中接收的液体中甲醇的检测方法为
(6)合成甲醇过程的催化机理如图所示。在该历程中,优先与催化剂反应的物质是

更新时间:2024-03-20 08:08:59
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组同学欲完成两个实验,涉及到下列有关实验操作。甲实验为食盐的精制,乙实验通过精制的食盐来配制0.4mol·L-1的氯化钠溶液。

(1)甲实验中除去难溶性杂质的操作步骤是___________ (填写上述序号),其中关键实验操作名称是___________ 。
(2)甲实验中,为有效除去粗盐中的Ca2+、Mg2+、SO42-杂质,精制过程中加入试剂:
①NaOH溶液②Na2CO3溶液③BaCl2溶液④盐酸,合理的加入顺序为____ (填序号)。其中加入NaOH溶液所发生反应的离子方程式为________________ 。
(3)乙实验,使用仪器③前必须进行的一步操作是______ 。配制时,除了上述仪器外,还可能用到的玻璃仪器是_____________ 。
(4)乙实验称量的NaCl质量为________ g。

(1)甲实验中除去难溶性杂质的操作步骤是
(2)甲实验中,为有效除去粗盐中的Ca2+、Mg2+、SO42-杂质,精制过程中加入试剂:
①NaOH溶液②Na2CO3溶液③BaCl2溶液④盐酸,合理的加入顺序为
(3)乙实验,使用仪器③前必须进行的一步操作是
(4)乙实验称量的NaCl质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。

(1)沉淀A的主要成分是_________ (填化学式)。
(2)②中反应的离子方程式是_________ 。
(3)③加入过量的Na2CO3溶液的目的是________ 。
(4)溶液3中肯定含有的杂质是_______ ,为除去杂质可向溶液3中加入过量的_______ 。

(1)沉淀A的主要成分是
(2)②中反应的离子方程式是
(3)③加入过量的Na2CO3溶液的目的是
(4)溶液3中肯定含有的杂质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化钠溶液中混有硫酸钠、氯化钙溶液和淀粉胶体。选择适当的试剂和方法从中提纯出氯化钠晶体。相应的实验过程如图:
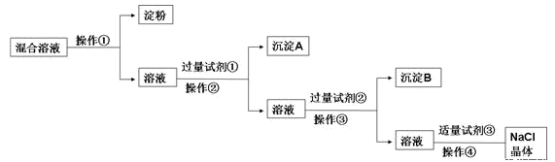
(1)写出上述实验过程中所用试剂(写化学式):试剂②_______ ;试剂③_______ 。
(2)判断试剂②已过量的方法是:_______ 。
(3)操作①时利用半透膜进行分离提纯。操作①的实验结果:淀粉_______ (填“能”或“不能”)透过半透膜;硫酸根离子_______ (填“能”或“不能”)透过半透膜。请用实验证明上述结果,完成表格(可不填满,也可增加)。限选试剂:1mol/L硝酸银溶液、1mol/L氯化钡溶液,1mol/L硝酸钡溶液、碘水、稀盐酸、稀硝酸

(1)写出上述实验过程中所用试剂(写化学式):试剂②
(2)判断试剂②已过量的方法是:
(3)操作①时利用半透膜进行分离提纯。操作①的实验结果:淀粉
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】兴趣小组同学为探究影响化学反应速率及化学平衡的因素,设计以下实验:
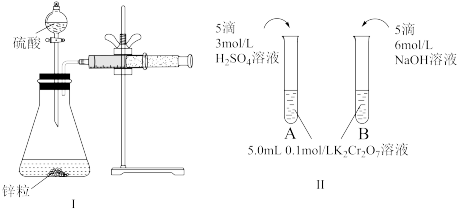
(1)利用实验Ⅰ探究锌与1mol/L硫酸和4mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项即可):___________ 。
(2)利用实验Ⅱ探究浓度对化学平衡的影响。
已知:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+ 推测B试管中实验现象为
(黄色)+2H+ 推测B试管中实验现象为___________ ,用平衡移动原理解释原因:___________ 。
(3)该小组同学继续用酸性KMnO4溶液和草酸(H2C2O4)溶液进行实验,实验操作及现象如下表:
已知:2MnO + 5H2C2O4 +6H+ =2Mn2+ +10CO2↑+8H2O
+ 5H2C2O4 +6H+ =2Mn2+ +10CO2↑+8H2O
① 由实验ⅰ、实验ⅱ可得出的结论是___________ 。
② 关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组同学提出了猜想:反应中生成的Mn2+对反应有催化作用。利用下列提供的试剂设计实验ⅲ,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸, MnSO4固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入5mL0.01mol/L酸性KMnO4溶液,___________ ,最后加入5mL0.1mol/L草酸溶液。

(1)利用实验Ⅰ探究锌与1mol/L硫酸和4mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项即可):
(2)利用实验Ⅱ探究浓度对化学平衡的影响。
已知:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+ 推测B试管中实验现象为
(黄色)+2H+ 推测B试管中实验现象为(3)该小组同学继续用酸性KMnO4溶液和草酸(H2C2O4)溶液进行实验,实验操作及现象如下表:
| 编号 | 实验操作 | 实验现象 |
| ⅰ | 向一支试管中先加入5mL0.01mol/L酸性KMnO4溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅,30min后几乎变为无色 |
| ⅱ | 向另一支试管中先加入5mL0.01mol/L酸性KMnO4溶液,再加入10滴3mol/L硫酸,最后加入5mL0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
 + 5H2C2O4 +6H+ =2Mn2+ +10CO2↑+8H2O
+ 5H2C2O4 +6H+ =2Mn2+ +10CO2↑+8H2O① 由实验ⅰ、实验ⅱ可得出的结论是
② 关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组同学提出了猜想:反应中生成的Mn2+对反应有催化作用。利用下列提供的试剂设计实验ⅲ,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸, MnSO4固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入5mL0.01mol/L酸性KMnO4溶液,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】我国将力争2060年前实现碳中和。 的捕捉是减少碳排放的措施之一
的捕捉是减少碳排放的措施之一
(1)一种利用NaOH溶液捕捉回收 的过程如图所示。
的过程如图所示。
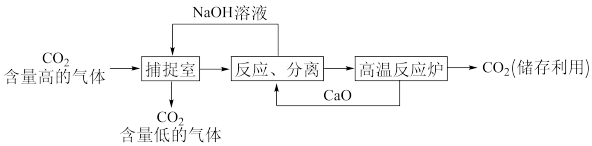
①捕捉室中NaOH溶液常喷成雾状,优点是_______ 。
②“反应分离”环节发生的复分解反应是_______ 。
③“反应分离”环节分离物质采用的方法是_______ 。
④ 用途广泛,写出一种用途:
用途广泛,写出一种用途:_______ 。
(2)CaO固体也可以捕捉回收 。研究表明
。研究表明 热分解制得的CaO疏松多孔,具有良好的
热分解制得的CaO疏松多孔,具有良好的 捕捉性能。取1.46g
捕捉性能。取1.46g 进行加热,固体质量随温度变化如图。
进行加热,固体质量随温度变化如图。
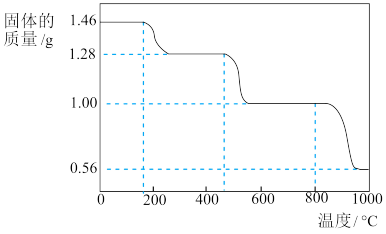
①写出400 ~600℃范围内分解反应的化学方程式:_______ ( 的相对分子质量:146)。
的相对分子质量:146)。
②据图分析,CaO捕捉 的反应温度应
的反应温度应_______ (填“高于”或“低于”)800℃。
 的捕捉是减少碳排放的措施之一
的捕捉是减少碳排放的措施之一(1)一种利用NaOH溶液捕捉回收
 的过程如图所示。
的过程如图所示。
①捕捉室中NaOH溶液常喷成雾状,优点是
②“反应分离”环节发生的复分解反应是
③“反应分离”环节分离物质采用的方法是
④
 用途广泛,写出一种用途:
用途广泛,写出一种用途:(2)CaO固体也可以捕捉回收
 。研究表明
。研究表明 热分解制得的CaO疏松多孔,具有良好的
热分解制得的CaO疏松多孔,具有良好的 捕捉性能。取1.46g
捕捉性能。取1.46g 进行加热,固体质量随温度变化如图。
进行加热,固体质量随温度变化如图。
①写出400 ~600℃范围内分解反应的化学方程式:
 的相对分子质量:146)。
的相对分子质量:146)。②据图分析,CaO捕捉
 的反应温度应
的反应温度应
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某实验探究小组用酸性 KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 KMnO4溶液的浓度可选择 0.010 mol·L-1、0.001 mol·L-1,催化剂的用量可选择 0.5 g、0 g,实验温度可选择 298K 、323K。每次实验酸性KMnO4溶液的用量均为 4 mL,H2C2O4溶液(0.100 mol·L-1)的用量均为2 mL。
(1)写出反应的离子方程式:_______ 。
(2)请完成实验设计表:
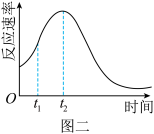
(3)图一通过测定一定时间内 CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物 MnSO4是该反应的催化剂;②_______ 。
(1)写出反应的离子方程式:
(2)请完成实验设计表:
| 编号 | T/K | 催化剂的用量/g | 酸性 KMnO4溶液的浓度/(mol·L-1) | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究 b.实验①和③探究 c.实验①和④探究催化剂对该反应速率的影响。 |
| ② | 298 | 0.5 | 0.001 | |
| ③ | 323 | 0.5 | 0.010 | |
| ④ | 0 |

(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物 MnSO4是该反应的催化剂;②

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】一名同学把4.48 L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8 mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
实验结束后发现无水CuSO4变蓝,干燥管和洗气瓶共增重18 g,澄清石灰水变浑浊后又恰好变澄清。请根据实验回答下列问题:
(1)O2要过量的原因是:________________ 。
(2)若该有机物只含C、H两种元素,且不含任何官能团,也不含脂环,则该有机物的分子式为________ ,它可能属于________ (填序号)。
A.烷烃 B.苯的同系物 C.芳香烃 D.烃的衍生物
该物质可能的结构简式为_____________________ 。
(3)若该有机物分子中含有一个氧原子,则它可能是哪几类物质?请各举一例,填写在下表中:

实验结束后发现无水CuSO4变蓝,干燥管和洗气瓶共增重18 g,澄清石灰水变浑浊后又恰好变澄清。请根据实验回答下列问题:
(1)O2要过量的原因是:
(2)若该有机物只含C、H两种元素,且不含任何官能团,也不含脂环,则该有机物的分子式为
A.烷烃 B.苯的同系物 C.芳香烃 D.烃的衍生物
该物质可能的结构简式为
(3)若该有机物分子中含有一个氧原子,则它可能是哪几类物质?请各举一例,填写在下表中:
| 物质种类 | 实例(写结构简式) |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】Ⅰ.某有机化合物的蒸汽对氢气的相对密度为30,其分子中含碳40%,含氢6.7%,其余为氧。该有机物的分子式为___________ ;若该物质能与 溶液反应放出
溶液反应放出 ,则该物质的结构简式为
,则该物质的结构简式为___________ 。
Ⅱ.某烃M的相对分子质量为84。
①烃M的分子式为___________ 。
②下列物质与烃M以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是___________ (填字母序号,下同);若总质量一定,充分燃烧消耗氧气的量不变的是___________ 。
A.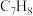 B.
B.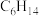 C.
C.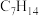 D.
D.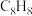
③若烃M为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则烃M的结构简式为___________ 。
 溶液反应放出
溶液反应放出 ,则该物质的结构简式为
,则该物质的结构简式为Ⅱ.某烃M的相对分子质量为84。
①烃M的分子式为
②下列物质与烃M以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是
A.
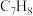 B.
B.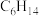 C.
C.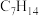 D.
D.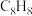
③若烃M为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则烃M的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】某种手液中含有PCMX,对革兰氏阳性和阴性菌及霉菌具有极好的杀灭效果。
(1)PCMX分子中含有苯环,相对分子质量为156.5,该有机物含有碳、氢、氧、氯四种元素,其中氯和氧元素的质量比为35.5︰16,则有机物的分子式是_______ 。
(2)PCMX分子的苯环上含有四个取代基,其中相同的两个取代基处于间位,另外两个不同的取代基处于对位;该有机物在一定条件下能跟浓溴水发生苯环上的取代反应,且PCMX与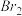 的物质的量之比为1︰2。PCMX结构简式是
的物质的量之比为1︰2。PCMX结构简式是__________ ,其中含氧官能团名称是_________ 。
(3)PCMX在光照的条件下,跟氯气反应生成一氯代物的化学方程式是__________ 。
(4)已知

 ,PCMX与
,PCMX与 反应的化学方程式是
反应的化学方程式是__________ ;
(5)PCMX的同分异构体中,有两个取代基,且能跟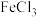 溶液发生显色反应的有
溶液发生显色反应的有________ 种,写出其中两种的结构简式__________ ,__________ 。
(1)PCMX分子中含有苯环,相对分子质量为156.5,该有机物含有碳、氢、氧、氯四种元素,其中氯和氧元素的质量比为35.5︰16,则有机物的分子式是
(2)PCMX分子的苯环上含有四个取代基,其中相同的两个取代基处于间位,另外两个不同的取代基处于对位;该有机物在一定条件下能跟浓溴水发生苯环上的取代反应,且PCMX与
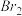 的物质的量之比为1︰2。PCMX结构简式是
的物质的量之比为1︰2。PCMX结构简式是(3)PCMX在光照的条件下,跟氯气反应生成一氯代物的化学方程式是
(4)已知


 ,PCMX与
,PCMX与 反应的化学方程式是
反应的化学方程式是(5)PCMX的同分异构体中,有两个取代基,且能跟
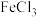 溶液发生显色反应的有
溶液发生显色反应的有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】看你有些听累了,白风这才拍了拍脑袋:“要不你先去休息下?我还有命题任务呢xwx”
“当然啦,毕竟是我约你出来玩的,如果乐意的话你也可以和我一起哦~”
面对白风的邀请,你怎么可能拒绝呢?
只不过,当你看到白风的命题群里正在讨论的问题是,一股不好的感觉忽然涌上心头……
白风:你们说,如果向等体积等浓度的两瓶溶液:【成分分别是Na2CO3和NaHCO3】中倒入过量但不等量的稀硫酸,有没有一种方法能区分出来他们两个原来的化学成分呢?
(1)看着大家都在想办法,白风转头朝你眨了眨眼:“你能给出一种可行的方案吗?_________________________ 。
看你想出来了白风很满意:“不愧是你,想到的这么快~”
“不过,这些仪器你认识嘛~”
(2)写出下列装置的完整名称:
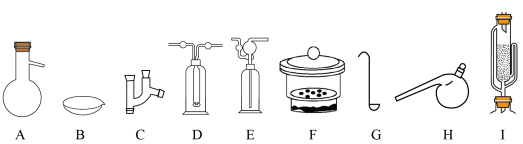
A___________ ,B___________ ,C___________ ,D___________ ,E___________ ,
F___________ ,G___________ ,H___________ ,I___________ 。
“当然啦,毕竟是我约你出来玩的,如果乐意的话你也可以和我一起哦~”
面对白风的邀请,你怎么可能拒绝呢?
只不过,当你看到白风的命题群里正在讨论的问题是,一股不好的感觉忽然涌上心头……
白风:你们说,如果向等体积等浓度的两瓶溶液:【成分分别是Na2CO3和NaHCO3】中倒入过量但不等量的稀硫酸,有没有一种方法能区分出来他们两个原来的化学成分呢?
(1)看着大家都在想办法,白风转头朝你眨了眨眼:“你能给出一种可行的方案吗?
看你想出来了白风很满意:“不愧是你,想到的这么快~”
“不过,这些仪器你认识嘛~”
(2)写出下列装置的完整名称:

A
F
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某研究小组为了准确检测香菇中添加剂亚硫酸盐的含量,设计实验如下(夹持装置省略):

①向三颈烧瓶中加入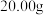 香菇样品和
香菇样品和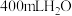 。
。
②向锥形瓶中加入 、
、 淀粉溶液和
淀粉溶液和 的碘标准溶液,充分搅拌。
的碘标准溶液,充分搅拌。
③以 流速通入
流速通入 ,然后加入过量浓
,然后加入过量浓 ,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了
,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了 碘标准溶液。
碘标准溶液。
④做空白实验,消耗了 碘标准溶液。
碘标准溶液。
回答下列问题:
(1)装置图中仪器a的进水方向_______ (填“m”或“n”)。
(2)装置图中仪器b的名称为_______ 。
(3)通入 的目的是
的目的是_______ 。
(4)利用平衡移动原理解释加入 能够生成
能够生成 的原因
的原因_______ *。
(5)下列操作会使测定结果偏大的是_______ 。
A.未用标准液润洗滴定管
B.滴定前滴定管尖嘴部分有气泡,滴定后无气泡
C.起始读数时平视,终点读数时俯视
(6)滴定终点时的现象为_______ ,该样品中亚硫酸盐含量(以 计)为
计)为_______ 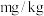 。
。

①向三颈烧瓶中加入
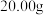 香菇样品和
香菇样品和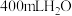 。
。②向锥形瓶中加入
 、
、 淀粉溶液和
淀粉溶液和 的碘标准溶液,充分搅拌。
的碘标准溶液,充分搅拌。③以
 流速通入
流速通入 ,然后加入过量浓
,然后加入过量浓 ,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了
,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了 碘标准溶液。
碘标准溶液。④做空白实验,消耗了
 碘标准溶液。
碘标准溶液。回答下列问题:
(1)装置图中仪器a的进水方向
(2)装置图中仪器b的名称为
(3)通入
 的目的是
的目的是(4)利用平衡移动原理解释加入
 能够生成
能够生成 的原因
的原因(5)下列操作会使测定结果偏大的是
A.未用标准液润洗滴定管
B.滴定前滴定管尖嘴部分有气泡,滴定后无气泡
C.起始读数时平视,终点读数时俯视
(6)滴定终点时的现象为
 计)为
计)为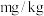 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(CH3COO)2Mn·4H2O主要用于纺织染色催化剂和分析试剂,其制备过程如图。回答下列问题:
步骤一:以MnO2为原料制备MnSO4
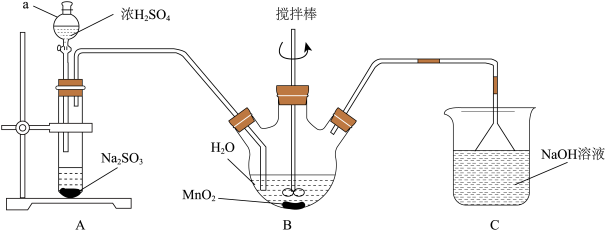
(1)仪器a的名称是___ ,C装置中NaOH溶液的作用是___________ 。
(2)B装置中发生反应的化学方程式是___________ 。
步骤二:制备MnCO3沉淀
充分反应后将B装置中的混合物过滤,向滤液中加入饱和NH4HCO3溶液,反应生成MnCO3沉淀。过滤,洗涤,干燥。
(3)①生成MnCO3的离子方程式_____________ 。
②判断沉淀已洗净的操作和现象是___________ 。
步骤三:制备(CH3COO)2Mn·4H2O固体
向11.5 g MnCO3固体中加入醋酸水溶液,反应一段时间后,过滤、洗涤,控制温度不超过55℃干燥,得(CH3COO)2Mn·4H2O固体。探究生成(CH3COO)2Mn·4H2O最佳实验条件的数据如下:
(4)产品干燥温度不宜超过55℃的原因可能是___________ 。
(5)上述实验探究了___________ 和___________ 对产品质量的影响,实验l中(CH3COO)2Mn·4H2O产率为___________ 。
步骤一:以MnO2为原料制备MnSO4

(1)仪器a的名称是
(2)B装置中发生反应的化学方程式是
步骤二:制备MnCO3沉淀
充分反应后将B装置中的混合物过滤,向滤液中加入饱和NH4HCO3溶液,反应生成MnCO3沉淀。过滤,洗涤,干燥。
(3)①生成MnCO3的离子方程式
②判断沉淀已洗净的操作和现象是
步骤三:制备(CH3COO)2Mn·4H2O固体
向11.5 g MnCO3固体中加入醋酸水溶液,反应一段时间后,过滤、洗涤,控制温度不超过55℃干燥,得(CH3COO)2Mn·4H2O固体。探究生成(CH3COO)2Mn·4H2O最佳实验条件的数据如下:
| 实验组别 | 醋酸质量分数 | 温度/℃ | 产品质量/g |
| 1 | 3% | 50 | 22.05 |
| 2 | 3% | 60 | 22.24 |
| 3 | 4% | 50 | 22.13 |
| 4 | 4$ | 60 | 23.27 |
(5)上述实验探究了
您最近一年使用:0次



