人类利用化学反应不仅可以创造新物质,还可以实现不同形式能量之间的转化,化学反应所提供的能量大大促进了社会的发展。与研究化学反应中的物质变化一样,研究化学反应中的能量变化同样具有重要意义。热化学方程式是一种化学用语,它表示的是一个化学反应中的反应焓变和物质变化。
(1)下列反应中,生成物总能量低于反应物总能量的是___________。
| A.碳酸钙受热分解 | B.八水合氢氧化钡与氯化铵的反应 |
| C.金属与酸与水的反应 | D.煤与高温下的水蒸气反应 |
(2)下列说法错误的是___________。
| A.在同一反应中,焓变和反应热的数值不相等 |
| B.有化学键破坏的一定是化学反应,且一定伴随着能量的变化 |
C.一个化学反应中,反应物的焓小于生成物的焓时, |
| D.反应体系向环境中释放能量,反应体系的焓会减小 |
(3)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的一种反应原理如下:
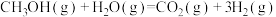
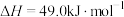 ,下列说法正确的是___________。
,下列说法正确的是___________。A.1L 蒸汽与1L水蒸气反应生成1L 蒸汽与1L水蒸气反应生成1L 气体与3L氢气吸收热量49.0kJ 气体与3L氢气吸收热量49.0kJ |
B.1个 分子与1个水分子反应生成1个 分子与1个水分子反应生成1个 分子与3个 分子与3个 分子吸收热量49.0kJ 分子吸收热量49.0kJ |
C.1mol 气体与1mol液态水反应生成1mol 气体与1mol液态水反应生成1mol 气体与3mol氢气吸收的热量小于49.0kJ 气体与3mol氢气吸收的热量小于49.0kJ |
D.相同条件下1mol 与1mol 与1mol 的能量总和小于1mol 的能量总和小于1mol 与3mol 与3mol 的能量总和 的能量总和 |
(4)氢气是一种清洁能源,如图是
 和
和 反应生成
反应生成 的能量变化示意图,由图可知___________。
的能量变化示意图,由图可知___________。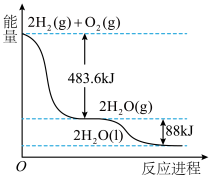
A. ,断键吸收的能量小于成键释放的能量 ,断键吸收的能量小于成键释放的能量 |
B.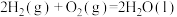  |
C. 和 和 具有的总能量比 具有的总能量比 所具有的总能量高 所具有的总能量高 |
D.生成2mol 需要吸收483.6kJ的能量 需要吸收483.6kJ的能量 |
(5)根据碘与氢气反应的热化学方程式
(ⅰ)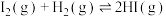
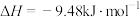
(ⅱ)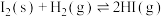
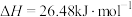
下列判断正确的是___________。
A.254g 中通入2g 中通入2g ,反应放热9.48kJ ,反应放热9.48kJ |
| B.1mol固态碘与1mol气态碘所含的能量相差17.00kJ |
| C.反应(ⅰ)的产物比反应(ⅱ)的产物稳定 |
| D.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
(6)能表示反应
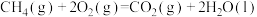 的示意图是
的示意图是A. 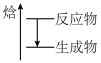 B.
B. 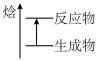 C.
C. 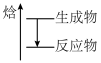 D.
D.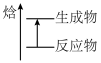
已知:常温常压下,8g甲烷气体在足量氧气中充分燃烧生成液态水和二氧化碳气体时放出445kJ热量,写出甲烷气体的燃烧热的热化学方程式:
(7)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为
 )。回答问题:
)。回答问题:| 化学键 | H―H | H―Cl |
| 键能 | 436 | 431 |
①下列关于键能的叙述正确的是
A.每生成1mol H―Cl吸收431kJ能量 B.每生成1mol H―Cl放出431kJ能量
C.每拆开1mol H―H放出436kJ能量 D.每拆开1mol H―H吸收436kJ能量
②已知热化学方程式: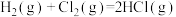
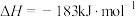 。则
。则 的键能为
的键能为 。
。
相似题推荐
 O2(g)=H2O(g),反应过程中能量变化如图,问:
O2(g)=H2O(g),反应过程中能量变化如图,问: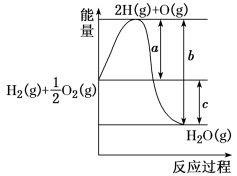
(1)a、b、c分别代表什么意义?
a
(2)该反应是放热反应还是吸热反应?
(3)a、b、c的关系式为
| 物质 | 炭粉(C) | 一氧化碳(CO) | 氢气(H2) | 甲烷(CH4) | 乙醇(C2H5OH) |
| 状态 | 固体 | 气体 | 气体 | 气体 | 液体 |
| 热量(kJ) | 392.8 | 282.6 | 285.8 | 890.3 | 1367 |
(2)写出管道煤气中的一氧化碳燃烧的热化学方程式
(3)充分燃烧 1mol 表中各种燃料,排放出二氧化碳的量最多的是
(4)矿物燃料储量有限,而且在燃烧过程中会产生污染。根据能源多样化的发展战略,我国开发利用的绿色能源有氢能、
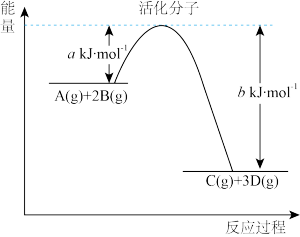
II.在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能 发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用 kJ·mol-1表示。请认真观察下图,然后回答问题:
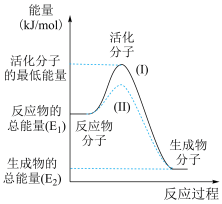
(5)图中所示反应是
(6)下列 4 个反应中符合示意图描述的反应的是___________(填代号)。
| A.水蒸气与炭反应 | B.用水稀释氢氧化钠溶液 | C.铝粉与四氧化三铁反应 | D.灼热的炭与 CO2反应 |
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是
①CO2(g)+H2(g)=CO(g)+H2O(g) △H1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) △H2=-90kJ•mol-1
(1)总反应的△H=
(2)下列示意图中能体现上述反应能量变化的是
A.
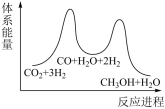 B.
B.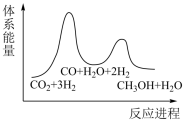 C.
C.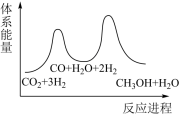
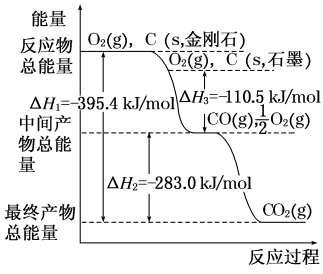
(1)等量金刚石和石墨完全燃烧
(2)在通常状况下,
(Ⅱ)已知热化学反应方程式:
Zn(s)+
 O2(g)=ZnO(s);ΔH=-351.5kJ·mol-1
O2(g)=ZnO(s);ΔH=-351.5kJ·mol-1Hg(l)+
 O2(g)=HgO(s);ΔH=-90.84kJ·mol-1
O2(g)=HgO(s);ΔH=-90.84kJ·mol-1则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的ΔH=
(1)25 ℃、1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
(3)已知:C(s,石墨)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l)ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g) ΔH=
 ,是导致汽车尾气中含有NO的原因之一。已知断裂某些共价键需要的能量如下表:
,是导致汽车尾气中含有NO的原因之一。已知断裂某些共价键需要的能量如下表:断裂的共价键 | O=O |
| N—O |
需要的能量 | 495 | 945 | 630 |
(1)机动车内燃机工作时会引发
 和
和 的反应,该反应是
的反应,该反应是 与1 mol
与1 mol  的总能量比2 mol NO的总能量
的总能量比2 mol NO的总能量(2)
 与
与 合成NO的热化学方程式可以表示为
合成NO的热化学方程式可以表示为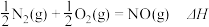 ,则
,则  =
=(3)NO与CO反应的热化学方程式可以表示
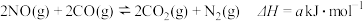 ,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,
,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后, =
=(1)某反应过程中的能量变化如下图所示:
①该反应的ΔH
②加入催化剂,b
③该反应的热化学方程式为
(2)已知: ① 2C(s)+O2(g)=2CO(g) ΔH=-221kJ/mol
② C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
则表示CO的燃烧热的热化学方程式为