回答下列问题:
(1)NaClO中Cl的化合价为_______ ,NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)9.03×1023个CO2的物质的量是_______ ,在标准状况下的体积为_______ 。
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为_______ ,所含氧原子数之比为_______ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO )=
)=_______ 。
(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为_______ 。
(6)FeCl2溶液通入氯气的反应,用离子方程式表示为_______ 。
(7)铜丝与浓硫酸反应的化学方程式为_______ ,若1molCu完全反应,则被还原的硫酸物质的量是_______ 。
(1)NaClO中Cl的化合价为
(2)9.03×1023个CO2的物质的量是
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO )=
)=(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为
(6)FeCl2溶液通入氯气的反应,用离子方程式表示为
(7)铜丝与浓硫酸反应的化学方程式为
更新时间:2024-04-01 10:47:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)18.6gNa2X含有0.6molNa+,则X的相对原子质量为___ 。
(2)标准状况下,1.6g某气态氧化物RO2体积为0.56L,RO2的摩尔质量为___ 。
(3)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,其中NH3的体积分数为___ 。
(4)相同条件下,H2和O2的质量比为m∶n的混合气体,其平均相对分子质量是___ 。
(5)同温同压下,等质量的O2和CO2,体积之比为___ 。
(6)某物质A在一定条件下加热完全分解,产物都是气体。分解方程式为4A B+2C+3D,测得生成的混合气体对甲烷的相对密度为
B+2C+3D,测得生成的混合气体对甲烷的相对密度为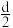 ,则A的相对分子质量为
,则A的相对分子质量为___ 。
(7)将标准状况下4.48LHCl气体通入0.5L水中(水的密度为1g/cm3),HCl完全溶解得到的盐酸溶液的密度为1.1g/cm3,该盐酸的物质的量浓度为____ mol·L-1(保留到小数点后一位小数)。
(8)将20.0g氢氧化钠固体溶于水配成100mL溶液,其密度为1.25g·mL-1。从该溶液中取出10mL,将其加水稀释到100mL,稀释后溶液中氢氧化钠的物质的量浓度为___ 。将一定体积的原溶液和稀释后的溶液按1:4的体积比混合(忽略混合时溶液体积变化),所得混合溶液中氢氧化钠的物质的量浓度为___ 。
(1)18.6gNa2X含有0.6molNa+,则X的相对原子质量为
(2)标准状况下,1.6g某气态氧化物RO2体积为0.56L,RO2的摩尔质量为
(3)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,其中NH3的体积分数为
(4)相同条件下,H2和O2的质量比为m∶n的混合气体,其平均相对分子质量是
(5)同温同压下,等质量的O2和CO2,体积之比为
(6)某物质A在一定条件下加热完全分解,产物都是气体。分解方程式为4A
 B+2C+3D,测得生成的混合气体对甲烷的相对密度为
B+2C+3D,测得生成的混合气体对甲烷的相对密度为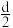 ,则A的相对分子质量为
,则A的相对分子质量为(7)将标准状况下4.48LHCl气体通入0.5L水中(水的密度为1g/cm3),HCl完全溶解得到的盐酸溶液的密度为1.1g/cm3,该盐酸的物质的量浓度为
(8)将20.0g氢氧化钠固体溶于水配成100mL溶液,其密度为1.25g·mL-1。从该溶液中取出10mL,将其加水稀释到100mL,稀释后溶液中氢氧化钠的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】室温下,某容积固定的密闭容器被可移动的活塞隔成A、B两室(假设活塞质量和与容器的摩擦忽略不计),A中充入了一定量 、
、 的混合气体,混合气体的质量为34g;B中充入了
的混合气体,混合气体的质量为34g;B中充入了 ,此时活塞的位置如图所示。
,此时活塞的位置如图所示。
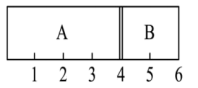
(1)A室混合气体所含分子总数为________ 。
(2)混合气体的密度是同温同压下条件下氢气密度的_____ 倍。
(3)若将A室 、
、 的混合气体点燃引爆,回复原温度后,最终活塞停留的位置在
的混合气体点燃引爆,回复原温度后,最终活塞停留的位置在_____ 刻度处,容器内气体压强与反应前气体压强之比为_____ 。
 、
、 的混合气体,混合气体的质量为34g;B中充入了
的混合气体,混合气体的质量为34g;B中充入了 ,此时活塞的位置如图所示。
,此时活塞的位置如图所示。
(1)A室混合气体所含分子总数为
(2)混合气体的密度是同温同压下条件下氢气密度的
(3)若将A室
 、
、 的混合气体点燃引爆,回复原温度后,最终活塞停留的位置在
的混合气体点燃引爆,回复原温度后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)有以下物质①石墨;②钠;③酒精;④氨气;⑤液态氯化氢;⑥氯化钠固体;⑦氢氧化钡溶液。
其中能导电的是___________ ;属于非电解质的是___________ 。
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是___________ 。
(3)写出亚硫酸氢钾在水溶液中的电离方程式___________ 。
(4)室温下,某容积固定的密闭容器由可移动的薄片活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在___________ 刻度处。
(1)有以下物质①石墨;②钠;③酒精;④氨气;⑤液态氯化氢;⑥氯化钠固体;⑦氢氧化钡溶液。
其中能导电的是
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(3)写出亚硫酸氢钾在水溶液中的电离方程式
(4)室温下,某容积固定的密闭容器由可移动的薄片活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+ 11O2 2Fe2O3+ 8SO2
2Fe2O3+ 8SO2
该反应中氧化剂和氧化产物之比为______________ ;标准状态下得到4.48升SO2 时,一共转移了________ mol e-。
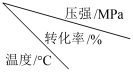
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的最佳反应条件是_________ 。
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 kJ,写出该反应的热化学方程式:____________________________________ 。若在该条件下将2 mol SO2放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 kJ,则此时SO2的转化率为____________ (用含Q1、Q2代数式表示)。
(4)市售浓硫酸的密度是1.84 g/cm3、质量分数为98 % ,若用H2SO4·XH2O来表示这种浓硫酸,则X为_________ 。
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+ 11O2
 2Fe2O3+ 8SO2
2Fe2O3+ 8SO2该反应中氧化剂和氧化产物之比为
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的最佳反应条件是
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| A.400-500℃ 0.1 MPa | B.400℃ 10 MPa |
| C.500℃ 10 MPa | D.400-500℃ 1 MPa |
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 kJ,写出该反应的热化学方程式:
(4)市售浓硫酸的密度是1.84 g/cm3、质量分数为98 % ,若用H2SO4·XH2O来表示这种浓硫酸,则X为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上用 为原料制
为原料制 可简化为如下两步反应:
可简化为如下两步反应:
第一步: (条件略);第二步:
(条件略);第二步: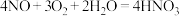 。
。
某同学用 与足量
与足量 和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气
和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气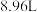 。请计算:
。请计算:
(1)消耗的 的物质的量为
的物质的量为___________  。
。
(2)整个过程转移电子的物质的量为___________  。
。
(3)理论上可获得质量分数为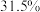 的硝酸(假设溶质不挥发)质量为
的硝酸(假设溶质不挥发)质量为___________  。
。
 为原料制
为原料制 可简化为如下两步反应:
可简化为如下两步反应:第一步:
 (条件略);第二步:
(条件略);第二步: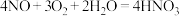 。
。某同学用
 与足量
与足量 和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气
和水为原料,在一定条件下模拟了上述生产过程,共消耗了标准状况下氨气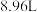 。请计算:
。请计算:(1)消耗的
 的物质的量为
的物质的量为 。
。(2)整个过程转移电子的物质的量为
 。
。(3)理论上可获得质量分数为
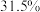 的硝酸(假设溶质不挥发)质量为
的硝酸(假设溶质不挥发)质量为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学工业为疫情防控提供了强有力的物质支撑。
(I)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________ (填序号)。
A Cl2 B H2O2 C ClO2 D O3
(II)一氯胺(NH2Cl)在中性或酸性环境中会发生强烈水解,生成具有强烈杀菌作用的HClO,是重要的水消毒剂。
(1)写出NH2Cl的电子式_______________
(2)写出NH2Cl水解的化学方程式______________________
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为__________
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_________ (用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:____________________
(I)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是
A Cl2 B H2O2 C ClO2 D O3
(II)一氯胺(NH2Cl)在中性或酸性环境中会发生强烈水解,生成具有强烈杀菌作用的HClO,是重要的水消毒剂。
(1)写出NH2Cl的电子式
(2)写出NH2Cl水解的化学方程式
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】离子反应是中学化学中重要的反应类型。回答下列问题:
(1)离子方程式是重要的化学用语。下列是有关离子方程式的一个错误观点:酸碱中和反应均可表示为 ,请用一个相应的“离子方程式”否定这个观点。
,请用一个相应的“离子方程式”否定这个观点。___________
(2)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“ ”来表示,请写出2个有关反应的化学方程式:
”来表示,请写出2个有关反应的化学方程式:
①___________ ;
②___________ 。
(3)实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:
方案一: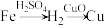
方案二:
写出上述两个方案每步转化的有关方程式。
方案一,化学方程式:___________ ;___________
方案二,离子方程式:___________ ;___________
(4)在常温下,将 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为___________ ,该漂白液的有效成分是___________ (填名称)。
(5)检验某溶液中是否含有 的方法是:
的方法是:___________ ,有关离子方程式是___________ 。
(1)离子方程式是重要的化学用语。下列是有关离子方程式的一个错误观点:酸碱中和反应均可表示为
 ,请用一个相应的“离子方程式”否定这个观点。
,请用一个相应的“离子方程式”否定这个观点。(2)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“
 ”来表示,请写出2个有关反应的化学方程式:
”来表示,请写出2个有关反应的化学方程式:①
②
(3)实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:
方案一:
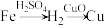
方案二:

写出上述两个方案每步转化的有关方程式。
方案一,化学方程式:
方案二,离子方程式:
(4)在常温下,将
 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为(5)检验某溶液中是否含有
 的方法是:
的方法是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碱式次氯酸镁[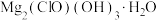 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
(1)工业上利用 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式_______ 。
(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是_______ ,阴极电极反应方程式为_______ 。
(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是_______ (用离子方程式表示)。
(4)碱式次氯酸镁( )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量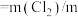 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为_______ 。
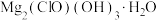 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:(1)工业上利用
 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、
 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是
(4)碱式次氯酸镁(
 )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量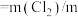 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】概念辨析(括号内画“√”或“×”,正确的横线处不填,错误的说明原因)
(1)浓H2SO4与Cu、C的反应中,都体现了H2SO4的酸性和强氧化性。(___)____ 。
(2)放热反应不需要加热就能反应,吸热反应不加热就不能反应。(___)_____ 。
(3)铵盐加热均易分解且产生NH3。(___)_____ 。
(4)伴有能量变化的物质变化都是化学变化。(___)____ 。
(1)浓H2SO4与Cu、C的反应中,都体现了H2SO4的酸性和强氧化性。(___)
(2)放热反应不需要加热就能反应,吸热反应不加热就不能反应。(___)
(3)铵盐加热均易分解且产生NH3。(___)
(4)伴有能量变化的物质变化都是化学变化。(___)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请写出下列相关反应的化学方程式。
(1)漂白粉的漂白原理:
(2)氯碱工业:
(3)工业制硫酸时高温煅烧硫铁矿:
(4)工业制硫酸时接触室中的反应:
(5)金属铜与浓硫酸反应:
(6)过氧化钠作呼吸面具的供氧剂(2个):
您最近一年使用:0次



