短周期主族元素X、Y、Z、Q、W的原子序数依次增大,其中X基态原子最外层2p轨道有两个未成对电子,Q的电负性为4.0,Z与W同主族且五种元素可形成如图所示的阴离子,下列说法正确的是
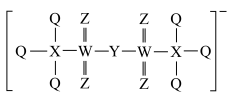
| A.Z、W可形成多种化合物且均为非极性分子 |
B.第一电离能: |
| C.X和Y分别形成氢化物的沸点:前者低于后者 |
| D.上述阴离子中,Y原子价层电子对数为4 |
更新时间:2024-04-01 10:53:51
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】我国发明的陶瓷荧光材料 能有效解决色漂移、蓝光溢出等问题
能有效解决色漂移、蓝光溢出等问题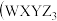 中仅Z元素为负价
中仅Z元素为负价 ,Z、X、Y、W是原子序数依次增大且均不大于20的主族元素,X、Y同周期且相邻,Y原子最外层电子数是次外层的
,Z、X、Y、W是原子序数依次增大且均不大于20的主族元素,X、Y同周期且相邻,Y原子最外层电子数是次外层的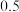 倍,W和Y的主族序数之和是X主族序数的2倍。下列说法正确的是
倍,W和Y的主族序数之和是X主族序数的2倍。下列说法正确的是
 能有效解决色漂移、蓝光溢出等问题
能有效解决色漂移、蓝光溢出等问题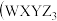 中仅Z元素为负价
中仅Z元素为负价 ,Z、X、Y、W是原子序数依次增大且均不大于20的主族元素,X、Y同周期且相邻,Y原子最外层电子数是次外层的
,Z、X、Y、W是原子序数依次增大且均不大于20的主族元素,X、Y同周期且相邻,Y原子最外层电子数是次外层的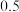 倍,W和Y的主族序数之和是X主族序数的2倍。下列说法正确的是
倍,W和Y的主族序数之和是X主族序数的2倍。下列说法正确的是A.原子半径: |
B.最高价氧化物的水化物的酸性: |
| C.X的氧化物可用于制造光导纤维 |
| D.工业上用电解熔融的氧化物来制取Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】M、W、X、Y、Z是原子序数依次增大的同周期主族元素,基态X原子2p能级上仅有2个电子,Y元素原子的价层电子数是W的两倍,由五种元素组成的某电极材料的结构如图所示。下列说法正确的是
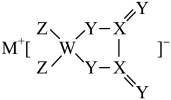
| A.氢化物沸点:X<Y |
| B.该化合物中必然存在配位键 |
| C.由M单质和Y单质反应生成的化合物中存在共价键 |
| D.基态原子未成对电子数:W<X<Y<Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】Xn+、Ym+、Zp-为3种短周期元素的离子,其中X、Y属于金属元素,Z为非金属元素,它们各自带有的电荷数p<n<m=3,且Zp-的电子层数比Xn+、Ym+多1,比较X、Y、Z及其化合物,则下列说法正确的是
| A.X、Y、Z的最高价氧化物对应的水化物中,Y(OH)m是一种两性氢氧化物,其碱性比X(OH)n弱,其酸性也比Z的最高价含氧酸弱 |
| B.原子半径Z>X>Y |
| C.单质的还原性Y>X |
| D.Xn+、Ym+、Zp-的半径:Xn+>Ym+>Zp- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】如图三条曲线分别表示 、
、 和
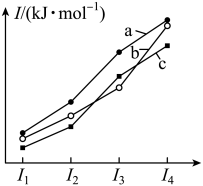
和 元素的前四级电离能变化趋势。下列说法正确的是
元素的前四级电离能变化趋势。下列说法正确的是
 、
、 和
和 元素的前四级电离能变化趋势。下列说法正确的是
元素的前四级电离能变化趋势。下列说法正确的是
A.元素电负性: |
B.简单氢化物的稳定性: |
C.简单氢化物的相对分子质量: |
D.对应最高价氧化物的水化物的酸性强弱: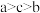 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】居里夫妇用α粒子( )轰击某金属原子
)轰击某金属原子 得到
得到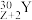 ,基态Y原子3p能级半充满。
,基态Y原子3p能级半充满。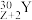 具有放射性,很快衰变为
具有放射性,很快衰变为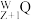 :
: ,
,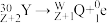 。下列说法正确的是
。下列说法正确的是
 )轰击某金属原子
)轰击某金属原子 得到
得到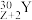 ,基态Y原子3p能级半充满。
,基态Y原子3p能级半充满。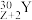 具有放射性,很快衰变为
具有放射性,很快衰变为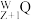 :
: ,
,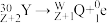 。下列说法正确的是
。下列说法正确的是| A.第一电离能:X<Q<Y |
| B.自然界不存在Y4分子,因其化学键不稳定 |
| C.X原子核内中子数与质子数之比为13:14 |
| D.简单氢化物的热稳定性:Y<Q |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】SO3和O3的混合气体经光解作用可生成一种新分子,结构简式如下所示,下列说法正确的是
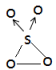

| A.O3的键角为10928 |
| B.SO3与O3均为非极性分子 |
| C.SO3 的空间结构为平面三角形 |
| D.SO3中心原子为sp3杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】通常状况下,NCl3是一种油状液体,下列对NCl3的有关叙述正确的是
| A.CCl4中C—Cl键键长比NCl3中N—Cl键键长短 |
| B.分子中的N原子无孤电子对 |
| C.NCl3分子的空间构型为三角锥型 |
| D.NCl3稳定性弱于NF3,因为N—Cl的键能比N—F的键能大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于物质结构的命题中,错误的项数有( )
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期ⅣA族,核外电子排布式为 [Ar]4s24p2,属于p区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2、NaHSO4晶体中的阴、阳离子个数比均为1 :2
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑧可燃冰中甲烷分子与水分子之间存在氢键
⑨在碘的CCl4的溶液中加入少量浓KI溶液,振荡试管,溶液颜色变浅
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期ⅣA族,核外电子排布式为 [Ar]4s24p2,属于p区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2、NaHSO4晶体中的阴、阳离子个数比均为1 :2
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“···”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为:
⑧可燃冰中甲烷分子与水分子之间存在氢键
⑨在碘的CCl4的溶液中加入少量浓KI溶液,振荡试管,溶液颜色变浅
| A.7项 | B.6项 | C.5项 | D.4项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】PH3的分子构型与NH3的分子构型相似。下列关于PH3和NH3的说法正确的是
| A.P-H键的极性大于N-H键的极性,PH3和NH3均为极性分子 |
| B.PH3的沸点高于NH3的沸点 |
| C.PH3与NH3均为三角锥形 |
| D.PH3中,P-H键的键长大于N-H键的键长,其键角也大于BF3分子中的键角 |
您最近一年使用:0次
【推荐3】铜是生命必须的元素,也是人类最早使用的金属之一、铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分Cu2S)可以用于制铜,反应方程式为 ,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是
,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是

 ,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是
,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是
| A.Cu+转化为基态Cu,得到的电子填充在3d轨道上 |
| B.O2和SO2都是非极性分子 |
| C.Cu2S晶胞中S2-位置如图所示,则一个晶胞中含有8个Cu+ |
| D.标准状况下,每有22.4 LO2参与反应,转移电子4 mol |
您最近一年使用:0次


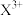
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是 中硅的价层电子对数为0.4
中硅的价层电子对数为0.4


