名校
解题方法
1 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)SO2分子构型为“折线型”,则SO2是___________ (选填“极性”、“非极性”)分子,从结构的角度解释原因:___________ ;其在水中的溶解度比氯气___________ (选填“大”、“小”、“一样”)。
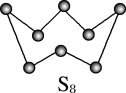
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是___________ ;下图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因是___________ 。
| H2S | S8 | MnS | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >1600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)SO2分子构型为“折线型”,则SO2是
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
您最近半年使用:0次
解题方法
2 . 氧化二氯(Cl2O)是净化饮用水的一种有效的净水剂,制备反应为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A.Cl2O的结构式为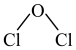 | B.键角 |
C. 中心原子的杂化方式为 中心原子的杂化方式为 | D.Cl2的电子云轮廓图为 |
您最近半年使用:0次
3 . 高效率和高选择性地将 转化为
转化为 是
是 资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原
资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原 提供了一种可行的转化方案,其原理如图所示,设
提供了一种可行的转化方案,其原理如图所示,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 转化为
转化为 是
是 资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原
资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原 提供了一种可行的转化方案,其原理如图所示,设
提供了一种可行的转化方案,其原理如图所示,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是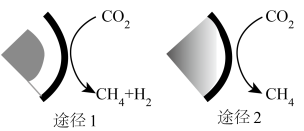
A.44g 中中心原子C的价层电子对数为 中中心原子C的价层电子对数为 |
B.1  中所含中子数一定为10 中所含中子数一定为10 |
C.途径2生成标准状况下22.4L ,反应转移电子数为8 ,反应转移电子数为8 |
D.若利用电解原理实现途径1, 在阳极放电 在阳极放电 |
您最近半年使用:0次
解题方法
4 . 下列表示不正确的是
A.HF分子中 键的形成示意图为 键的形成示意图为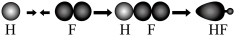 |
B.基态Cr原子的价层电子轨道表示式为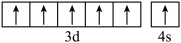 |
C. 分子的VSEPR模型: 分子的VSEPR模型: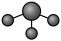 |
D.2,4,6—三硝基甲苯的结构简式: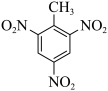 |
您最近半年使用:0次
名校
5 . S2Cl2常用于制作橡胶的粘结剂,S2Cl2与水反应的化学方程式为2 S2Cl2+2H2O=SO2↑+3S↓+4HCl。设NA表示阿伏加德罗常数的值。下列说法错误的是
| A.32gS2与32gS8均含有NA个硫原子 |
| B.0.1molS2Cl2含有6.6NA个质子 |
| C.标准状况下,2.24LSO2中S原子的孤电子对数为0.1NA |
| D.若有4molHCl生成,则该反应中转移的电子数为6NA |
您最近半年使用:0次
2024-04-19更新
|
275次组卷
|
2卷引用:湖南省长沙市长郡中学2024届高三高考适应性考试(二)化学试题
名校
解题方法
6 . 设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A. 金刚石含碳碳单键的数目为 金刚石含碳碳单键的数目为 |
B.标准状况下,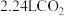 中的 中的 键数目为 键数目为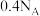 |
C.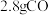 和 和 的混合气体中含有的孤电子对数为 的混合气体中含有的孤电子对数为 |
D. 冰中有 冰中有 个氢键 个氢键 |
您最近半年使用:0次
名校
解题方法
7 . 下列化学用语书写正确的是
A.基态Mg原子的价电子排布图: | B.p-p π键电子云模型: 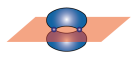 |
| C.As原子的简化电子排布式:[Ar]4s24p3 | D.SO3的VSEPR模型: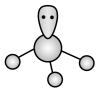 |
您最近半年使用:0次
8 . NA为阿伏加德罗常数的值。下列说法错误的是
| A.0.5molXeF4中氙的价层电子对数为2NA |
B.2.0gH218O与D216O 混合物中含有的中子数为NA 混合物中含有的中子数为NA |
| C.40g SiC晶体中含有的Si-C键数目为4NA |
| D.标准状况下,22.4L乙炔中π键数为2NA |
您最近半年使用:0次
9 . 下列说法正确的是
| A.利用红外光谱可以测定分子的相对分子质量 |
B.苹果酸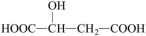 含有1个手性碳原子 含有1个手性碳原子 |
| C.AsH3分子的中心原子上的孤电子对数为3 |
| D.基态S原子核外电子的运动状态有9种 |
您最近半年使用:0次
名校
10 . 沼气是一种混合气体,成分及其含量为55%~70% 、30%~45%
、30%~45% 气体,下列说法正确的是
气体,下列说法正确的是
 、30%~45%
、30%~45% 气体,下列说法正确的是
气体,下列说法正确的是A.最高正化合价: |
B. 中心原子价层电子对数为3 中心原子价层电子对数为3 |
C. 分子中 分子中 键与 键与 键的数目之比为2∶1 键的数目之比为2∶1 |
D.通过红外光谱仪可测定 的相对分子质量 的相对分子质量 |
您最近半年使用:0次



