水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法错误的是
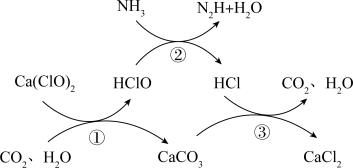

| A.反应①为非氧化还原反应 |
| B.反应②每生成1 mol N2,转移6 mol电子 |
| C.22.4 L二氧化碳所含的共用电子对数目为4NA |
| D.CO2在该反应中能够循环利用 |
更新时间:2024-04-02 15:34:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】用NA表示阿伏伽德罗常数的值,下列说法正确的是
| A.标准状况下,11.2L 1H2和2H2组成的混合气体中含质子数为NA |
| B.标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA |
| C.铁在高温下与水蒸气反应,每消耗56g Fe,转移电子数为3NA |
| D.浓度为1mol/L的K2SO4溶液中所含K+数目为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏伽德罗常数的数值。下列有关说法中正确的有
①1L0.1 mol·L-1 FeCl3溶液中含Fe3+数目为0.1NA
②5.6g铁粉与3.2g硫粉混合隔绝空气加热,充分反应后,转移电子数为0.2NA
③0.lmol乙醇与0.lmol乙酸在浓硫酸催化并加热下,生成乙酸乙酯分子数为0.1NA
④60gSiO2中含有的Si-O键和12g金刚石中含有的C-C键的数目均为NA
⑤体积为11.2L的氯气中含有氯原子数约为6.02×1025个
⑥92g的NO2和N2O4混合气体含有的原子数为6NA
⑦10g46%甲酸( HCOOH)水溶液中所含的氧原子数为0.5NA
⑧7.8gNa2O2与足量的水(H218O)反应生成的氧气中所含的中子数为0.5NA
①1L0.1 mol·L-1 FeCl3溶液中含Fe3+数目为0.1NA
②5.6g铁粉与3.2g硫粉混合隔绝空气加热,充分反应后,转移电子数为0.2NA
③0.lmol乙醇与0.lmol乙酸在浓硫酸催化并加热下,生成乙酸乙酯分子数为0.1NA
④60gSiO2中含有的Si-O键和12g金刚石中含有的C-C键的数目均为NA
⑤体积为11.2L的氯气中含有氯原子数约为6.02×1025个
⑥92g的NO2和N2O4混合气体含有的原子数为6NA
⑦10g46%甲酸( HCOOH)水溶液中所含的氧原子数为0.5NA
⑧7.8gNa2O2与足量的水(H218O)反应生成的氧气中所含的中子数为0.5NA
| A.四种 | B.三种 | C.五种 | D.两种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,往 溶液中滴加少量酸性
溶液中滴加少量酸性 溶液,可发生如下两个反应:①
溶液,可发生如下两个反应:① ;②
;② 。下列说法正确的是
。下列说法正确的是
 溶液中滴加少量酸性
溶液中滴加少量酸性 溶液,可发生如下两个反应:①
溶液,可发生如下两个反应:① ;②
;② 。下列说法正确的是
。下列说法正确的是A. 的氧化性比 的氧化性比 强,其还原性比 强,其还原性比 弱 弱 |
B. 的分解过程中,溶液的酸性逐渐增强 的分解过程中,溶液的酸性逐渐增强 |
C. 分解的总方程式为 分解的总方程式为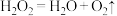 |
D. 生产过程要严格避免混入 生产过程要严格避免混入 |
您最近一年使用:0次
【推荐2】关于反应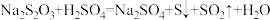 ,下列说法正确的是
,下列说法正确的是
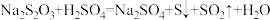 ,下列说法正确的是
,下列说法正确的是| A.H2SO4是还原剂 |
| B.氧化产物与还原产物的物质的量之比为2∶1 |
| C.0.5mol Na2S2O3发生反应,转移1mol电子 |
| D.Na2S2O3与稀硝酸也能发生类似反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式正确的是( )
| A.漂白粉露置在空气中失效:ClO-+CO2+H2O===HClO+HCO3- |
| B.向银氨溶液中加入足量的HCl:[Ag(NH3)2]++OH-+3H+===Ag++2NH4++H2O |
| C.过量的CO2通入水玻璃中:SiO32-+2CO2+2H2O===H2SiO3↓+2HCO3- |
| D.NH4Al(SO4)2溶液中加入过量Ba(OH)2溶液:NH4++Al3++5OH-===NH3·H2O+AlO2-+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学与社会、生活密切相关。对下列现象或事实的解释正确的是
| 选项 | 现象或事实 | 解 释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接和油污反应 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C | Ca(OH)2溶液能溶解难溶的杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)浸出K+ | 氢氧根离子与镁离子结合,使平衡向右移动 |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,在反应过程中测得Fe3+、
、H+和H2O六种粒子,在反应过程中测得Fe3+、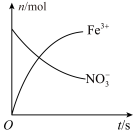
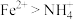
 )是分子晶体,推测
)是分子晶体,推测 也是分子晶体
也是分子晶体 与
与 与
与 ,推测
,推测 反应生成
反应生成 与
与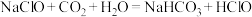 ,推测
,推测 溶液中通入过量
溶液中通入过量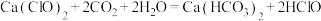
 加热可制取HCl,推测
加热可制取HCl,推测 与浓
与浓


