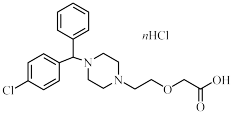
盐酸左西替利嗪是一种用于治疗荨麻疹的药物。其部分说明书如下:
(1)在左西替利嗪中添加盐酸的目的是___________ ;药品成分中n的值为___________ 。
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是___________ 。请在下图中用:“·”标出具有手性的碳原子。___________
| 盐酸左西替利嗪说明书 【成分】本品为西替利嗪的R型对映体,在过量盐酸中结晶制得。 【性状】本品外观是白色或类白色的片剂,易溶于水。
|
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是

| A.西替利嗪中,有9个碳原子与氮原子的杂化方式相同 |
| B.将西替利嗪溶于水,形成内盐 |
| C.两个苯环上的12个碳原子共平面 |
| D.分子内含有羧基和酯基 |
更新时间:2024-04-12 10:05:57
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】非金属元素碳能形成多种化合物,请回答以下与碳的化合物相关的问题:
(1)CO2分子中σ键与π键的个数比为__________________ 。
(2)C2H6的二溴代物中__________________ (填“有”或“无”)手性分子。
(3)已知邻羟基苯甲酸 与对羟基苯甲酸
与对羟基苯甲酸 的沸点相差较大,根据结构分析,前者的沸点
的沸点相差较大,根据结构分析,前者的沸点_________ 后者(填“高于”或“低于”)并解释原因___________________ 。
(1)CO2分子中σ键与π键的个数比为
(2)C2H6的二溴代物中
(3)已知邻羟基苯甲酸
 与对羟基苯甲酸
与对羟基苯甲酸 的沸点相差较大,根据结构分析,前者的沸点
的沸点相差较大,根据结构分析,前者的沸点
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】已知反应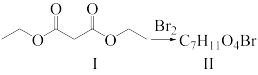 ,回答下列问题:
,回答下列问题:
(1)已知化合物II的核磁共振氢谱有三组峰,且峰面积之比为6∶4∶1,则其结构简式为________ 。
(2)已知X的相对分子质量比化合物I少14,且 X能与足量
X能与足量 溶液反应放出
溶液反应放出
 。符合上述条件的X共有
。符合上述条件的X共有________ 种(不考虑立体异构),写出含有手性碳原子的所有可能的结构简式,并用*标出手性碳原子的位置(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)________ 。
 ,回答下列问题:
,回答下列问题:(1)已知化合物II的核磁共振氢谱有三组峰,且峰面积之比为6∶4∶1,则其结构简式为
(2)已知X的相对分子质量比化合物I少14,且
 X能与足量
X能与足量 溶液反应放出
溶液反应放出
 。符合上述条件的X共有
。符合上述条件的X共有
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】化合物(A)是治疗慢性或习惯性便秘,调节结肠的生理节律的药物。它是由单糖(B)和单糖(C)经甙(苷)键结合成的一个双糖。

请回答以下问题:
(1)写出(B)糖和(C)糖的名称:_______ 、_______ 。
(2)写出(C)糖的费歇尔(Fischer)投影式,用*标出(C)糖中的手性碳原子,并标出手性碳原子的R或S构型_________ 。同时指出(C)糖的构型_______ 。
(3)指出(B)糖和(C)糖是通过何种甙(苷)键结合成(A)糖的_______ 。
(4)用系统命名法命名(A)糖________ 。

请回答以下问题:
(1)写出(B)糖和(C)糖的名称:
(2)写出(C)糖的费歇尔(Fischer)投影式,用*标出(C)糖中的手性碳原子,并标出手性碳原子的R或S构型
(3)指出(B)糖和(C)糖是通过何种甙(苷)键结合成(A)糖的
(4)用系统命名法命名(A)糖
您最近一年使用:0次
【推荐1】催化剂(Fe,Al)/MIL-53可直接选择性氧化甲烷制甲醇,节省能耗。

(1)(Fe,Al)/MIL-53制备方法如下:Al(NO3)3•9H2O +Al/MIL-53
+Al/MIL-53 (Fe,Al)/MIL-53。
(Fe,Al)/MIL-53。
①对苯二甲酸的结构简式为_______ ,该分子中最多_______ 个原子共平面。
②生成(Fe,Al)/MIL-53过程中溶液pH_______ (填“变大”或“变小”)。
③(Fe,Al)/MIL-53中Fe3+位于O原子形成的_______ 空隙中,1个对苯二甲酸根离子最多能形成_______ 个配位键。
(2)(Fe,Al)/MIL-53催化CH4制CH3OH的机理如图,其中虚线表示吸附状态。

①ii转化为iii的过程中,破坏的微粒间作用力有_______ (填标号)。
A.σ键 B.配位键 C.离子键 D.极性键 E.非极性键
②该催化循环中铁元素价态有_______ 种。
(3)用FeCl3•6H2O和对苯二甲酸合成Fe/MIL-53。两种催化剂在上述催化过程中相对能量的变化情况如图。

①Fe/MIL-53催化过程中决速步骤为_______ (化学键变化角度答题)。
②(Fe,Al)/MIL-53催化效果更佳的原因是_______ 。

(1)(Fe,Al)/MIL-53制备方法如下:Al(NO3)3•9H2O
 +Al/MIL-53
+Al/MIL-53 (Fe,Al)/MIL-53。
(Fe,Al)/MIL-53。①对苯二甲酸的结构简式为
②生成(Fe,Al)/MIL-53过程中溶液pH
③(Fe,Al)/MIL-53中Fe3+位于O原子形成的
(2)(Fe,Al)/MIL-53催化CH4制CH3OH的机理如图,其中虚线表示吸附状态。

①ii转化为iii的过程中,破坏的微粒间作用力有
A.σ键 B.配位键 C.离子键 D.极性键 E.非极性键
②该催化循环中铁元素价态有
(3)用FeCl3•6H2O和对苯二甲酸合成Fe/MIL-53。两种催化剂在上述催化过程中相对能量的变化情况如图。

①Fe/MIL-53催化过程中决速步骤为
②(Fe,Al)/MIL-53催化效果更佳的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】按要求回答下列问题:
(1) 的分子式为
的分子式为______ ,所含官能团的名称为_____ 。
(2)CH3-C≡C-CH=CHCH3分子中有_____ 个碳原子共平面,最多有_____ 个原子共平面。
(3)一定条件下,某些不饱和烃分子可以进行自身加成反应,例如:
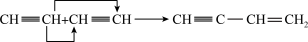
有机物甲的结构简式为 ,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长碳链仍为5个碳原子,丙是甲的同分异构体。则乙的结构简式是
,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长碳链仍为5个碳原子,丙是甲的同分异构体。则乙的结构简式是______ ,丙的结构简式是_____ 。
(1)
 的分子式为
的分子式为(2)CH3-C≡C-CH=CHCH3分子中有
(3)一定条件下,某些不饱和烃分子可以进行自身加成反应,例如:

有机物甲的结构简式为
 ,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长碳链仍为5个碳原子,丙是甲的同分异构体。则乙的结构简式是
,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的。在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长碳链仍为5个碳原子,丙是甲的同分异构体。则乙的结构简式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】按要求填空
(1)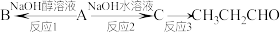
①反应1的反应类型___________ 。
②物质B的名称___________ 。
③反应3的条件___________ 。
(2)某有机物结构如下图所示,分子中处于同一直线的碳原子最多有___________ 个, 该烃与氢气反应最多消耗
该烃与氢气反应最多消耗___________ mol氢气。 ,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:
,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:___________ 。
(4)分子式为 且属于芳香族化合物的同分异构体有
且属于芳香族化合物的同分异构体有___________ 种。
(5)BN晶体的晶胞如下图,已知B原子半径为 ,N原子半径为
,N原子半径为 ,BN属于
,BN属于___________ 晶体,试表示BN晶体的空间利用率计算式___________ 。
(1)
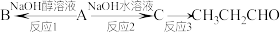
①反应1的反应类型
②物质B的名称
③反应3的条件
(2)某有机物结构如下图所示,分子中处于同一直线的碳原子最多有
 该烃与氢气反应最多消耗
该烃与氢气反应最多消耗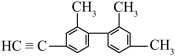
 ,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:
,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:(4)分子式为
 且属于芳香族化合物的同分异构体有
且属于芳香族化合物的同分异构体有(5)BN晶体的晶胞如下图,已知B原子半径为
 ,N原子半径为
,N原子半径为 ,BN属于
,BN属于
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】根据元素周期表回答下列问题:
(1)写出元素Cu的基态原子的电子排布式:____________________ 。
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有________ 对。此元素A原子与O的第一电离能的相对大小为:A________ O(填“<”“>”或“=”)。
(3)元素C形成的最高价氧化物中含有________ 个π键。C和Cl形成化合物的电子式为_____________ ,此化合物中C的杂化方式为________ 。
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是________ ,假设晶胞的边长为d cm、密度为ρ g·cm-3,则元素钒的相对原子质量为_____________ (NA为阿伏伽德罗常数)。

(1)写出元素Cu的基态原子的电子排布式:
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有
(3)元素C形成的最高价氧化物中含有
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】铜的配合物在自然界中广泛存在,请回答下列问题:
(1)基态29Cu的核外电子排布式为____ 。
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子____ (填化学式),配体中提供孤电子对的原子是____ (填元素符号)。
②H2O、SO 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为____ 、____ 。
(3)同学甲设计如图制备铜的配合物的实验:

已知:铜离子的配位数通常为4。
①结合化学平衡原理解释试管c中浑浊液转变为深蓝色溶液的原因____ 。
②由上述实验可得出以下结论:结论1:配合物的形成与____ 、____ 有关。
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:____>____(填化学式)。____
(1)基态29Cu的核外电子排布式为
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子
②H2O、SO
 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为(3)同学甲设计如图制备铜的配合物的实验:

已知:铜离子的配位数通常为4。
①结合化学平衡原理解释试管c中浑浊液转变为深蓝色溶液的原因
②由上述实验可得出以下结论:结论1:配合物的形成与
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:____>____(填化学式)。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】选考【化学——选修3:物质结构与性质】四种常见元素的性质或结构信息如F表所示,请问答下列问题。
(1)R的基态原子价层电子排布式为________ ,这四种元素的第一电离能由大到小的顺序为________________ (写元素符号)。
(2)
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中 键之比为
键之比为________ ,已知有下列两种数据:
请解释键能大小与两种氧化物熔点、沸点高低差异过大的原因________ 。
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为________ 。

(5)A元素能形成组成为Pt(AH3)2Cl2的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是________ (填“极性”或“非极性”)分子,
②P的结构简式为________ (AH3配体作为一个整体写)。
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3 个能级且最高能级上有3 个电子 | B的单质是最常 见半导体材料 | 位于第四周期 IB族 | 是非金属元素,其形成的 某种单质是电的良导体, 有的分子形状似足球 |
(2)
| A.B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为_______,任意写出一种中心原子存在sp3、sp2两种杂化类型的物质的结构简式________,与A的常见单质互为等电子体的上述元素的氧化物是________。 |
 键之比为
键之比为| 键能(kJ/mol) | 熔点(K) | 沸点(K) | |
| BO2 | B-O:452 | 1923 | 2503 |
| DO2 | D=O:615 D-O:348 | 216 | 195 |
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为

(5)A元素能形成组成为Pt(AH3)2Cl2的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是
②P的结构简式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】已知苯胺( )与甲基吡啶(
)与甲基吡啶( )互为芳香同分异构体。E(
)互为芳香同分异构体。E( )的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有
)的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有_______ 种,其中,芳香环上为二取代的结构简式为_______ 。
 )与甲基吡啶(
)与甲基吡啶( )互为芳香同分异构体。E(
)互为芳香同分异构体。E( )的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有
)的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有
您最近一年使用:0次