元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),与中学常见的长式元素周期表相比,第一到第十八可看成族,⑩为Fe元素。由扇形周期表的填充规律,下列有关已填入的元素说法不正确的是
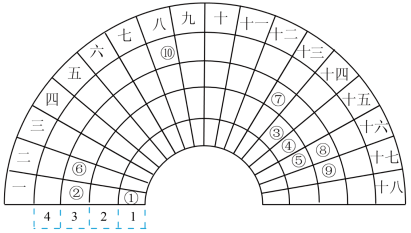
| A.⑤处于长式周期表第二周期第VIA族 |
| B.②最高价氧化物水化物能与⑦的最高价氧化物反应 |
| C.①与③均可形成既含极性键又含非极性键的化合物 |
| D.⑩单质能与CO形成两种稳定配合物Fe(CO)5和Fe(CO)6 |
更新时间:2024-04-12 12:36:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质中,既能与强酸反应,又能与强碱反应的是
① ②Al③
②Al③ ④
④ ⑤
⑤
①
 ②Al③
②Al③ ④
④ ⑤
⑤
| A.①②③ | B.②③④ | C.③④⑤ | D.①②③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应的离子方程式正确的是
A.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO 沉淀完全:2Al3++3SO 沉淀完全:2Al3++3SO +3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓ +3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓ |
B.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO +2HClO +2HClO |
C.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO +3Cl-+H2O+4H+ +3Cl-+H2O+4H+ |
| D.氯化铜溶液中通入H2S:Cu2++H2S=CuS↓+2H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下图为元素周期表短周期的一部分。关于A~G 七种元素的叙述正确的是
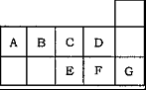

| A.E、F、G形成的单质中都含有共价键 |
| B.形成的简单阴离子半径:E > C > D |
| C.B、C、D三种元素的氢化物的稳定性依次减弱 |
| D.A、B、E的氢化物都能跟HNO3发生化合反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是
四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是
 四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是
四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是| X | Y | |||
| W | Z | |||
A.四种元素中原子半径最大为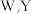 元素没有最高正价 元素没有最高正价 | B.四种元素最高价氧化物的水化物都是酸 |
C.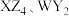 中所含化学键类型相同,熔点都很高 中所含化学键类型相同,熔点都很高 | D.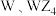 都是重要的半导体材料 都是重要的半导体材料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】W、X、Y、Z为短周期主族元素,原子序数依次增大.W与Y同族,Z的族序数等于X和Y的族序数之和.A、B、C、D、E、F分别是由上述四种元素中的一种或两种组成,相互转化关系如图所示.化合物G的焰色实验呈黄色,下列说法错误的是


A.简单离子半径: |
| B.Z形成的含氧酸一定是强酸 |
| C.Y形成的常见氧化物中阳离子与阴离子个数之比都为2∶1 |
| D.W与X形成的一种二元化合物中,可能只有极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】药物利托那韦治疗新型冠状病毒肺炎临床研究进展顺利。如图是利托那韦的结构,有关利托那韦的说法错误的是
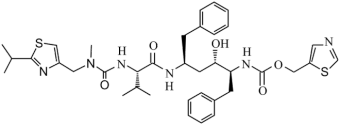

| A.分子式为C37H48N6O5S2 |
| B.分子中既含有σ键又含有π键 |
| C.分子中含有极性较强的化学键,化学性质比较活泼 |
| D.分子中含有苯环,属于芳香烃 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值,下列说法错误的是
| A.标准状况下,2.24L丙烯中含有的σ键数目为0.8NA |
| B.6.0gSiO2与足量HF溶液充分反应,生成SiF4的数目为0.1NA |
C.1.2gNaHSO4晶体中含有的 数目为0.01NA 数目为0.01NA |
| D.5.6gFe与3.55g氯气充分反应后转移的电子数目为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 可用作杀虫剂,其制备步骤如下。
可用作杀虫剂,其制备步骤如下。
步骤1:向足量铜粉与一定量稀 的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
步骤2:向步骤1所得滤液中边搅拌边滴加氨水,沉淀先增加后减少。当沉淀完全溶解时,停止滴加氨水。
步骤3:向步骤2所得溶液中加入95%乙醇,析出深蓝色 晶体。
晶体。
下列说法正确的是
 可用作杀虫剂,其制备步骤如下。
可用作杀虫剂,其制备步骤如下。步骤1:向足量铜粉与一定量稀
 的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。步骤2:向步骤1所得滤液中边搅拌边滴加氨水,沉淀先增加后减少。当沉淀完全溶解时,停止滴加氨水。
步骤3:向步骤2所得溶液中加入95%乙醇,析出深蓝色
 晶体。
晶体。下列说法正确的是
A.步骤1发生反应的离子方程式为 |
B.步骤2所得溶液中大量存在的离子有 、 、 、 、 、 、 |
C.步骤3加入95%乙醇的目的是降低 的溶解量 的溶解量 |
D. 中有12个配位键 中有12个配位键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】碱性溶液中, 可与缩二脲形成下图所示的紫色配离子。有关说法正确的是
可与缩二脲形成下图所示的紫色配离子。有关说法正确的是

 可与缩二脲形成下图所示的紫色配离子。有关说法正确的是
可与缩二脲形成下图所示的紫色配离子。有关说法正确的是
| A.该离子中,只有C、N和O原子可以和水分子形成氢键 |
B.基态Cu原子的价电子排布式是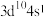 ,该配离子中 ,该配离子中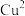 的配位数为4 的配位数为4 |
| C.该离子涉及的元素的电负性顺序为Cu<C<H<N<O |
| D.已知铜氨配离子为平面正方形结构,则图中离子也是平面型结构(均不考虑H原子) |
您最近一年使用:0次

 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼
转化为肼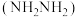 ,其反应历程如下所示。
,其反应历程如下所示。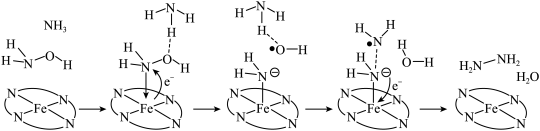
 均为非极性分子
均为非极性分子 ,反应可得
,反应可得


