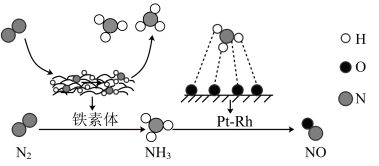
下列说法正确的是
A. 的第一电离能高于 的第一电离能高于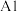 ,则 ,则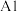 的金属性强于 的金属性强于 |
B. 是非极性分子,则 是非极性分子,则 也是非极性分子 也是非极性分子 |
| C.分子晶体中分子间作用力越大,对应的物质越稳定 |
| D.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
更新时间:2024-04-15 09:09:39
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关性质的比较中,正确的是
| A.微粒半径:O2-<F-<Na+<Li+ |
| B.第一电离能:He<Ne<Ar |
| C.共价键的键能:C-C<C=C<C≡C |
| D.分子中的键角:CH4>H2O>CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法正确的是( )
| A.C、N、O三种元素电负性从大到小的顺序是N>O>C |
| B.第二周期基态原子第一电离能处于B和O之间的元素有1种 |
| C.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| D.基态Ti原子的价电子排布式是4s23d2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
| A.H2O的沸点比H2S的高与氢键无关 |
B. 中价电子对互斥理论模型名称与离子的立体构型名称不一致 中价电子对互斥理论模型名称与离子的立体构型名称不一致 |
C.由于乳酸(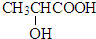 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体 |
| D.冰和固体碘晶体中相互作用力类型相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.用价层电子对互斥理论预测H2S、BF3的立体结构分别为V形、平面正三角形 |
| B.分子晶体中一定存在分子间作用力,不一定存在共价键 |
| C.1 mol晶体硅中含有4 mol Si-Si键 |
| D.仅含极性共价键的分子可以是极性分子,也可以是非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关物质结构与性质的表述结构正确的是
A.N-H键的极性大于C-H键的极性, 分子的极性小于 分子的极性小于 |
B. 易溶于 易溶于 ,可从 ,可从 和 和 都是非极性分子的角度解释 都是非极性分子的角度解释 |
C. 中的氢键数量比 中的氢键数量比 少,可推断 少,可推断 的稳定性比 的稳定性比 差 差 |
| D.超分子是两种或两种以上的分子(包括离子)通过化学键形成的分子聚集体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】光气(COCl2)是一种重要的有机中间体,其制备原理为: 。下列叙述正确的是
。下列叙述正确的是
 。下列叙述正确的是
。下列叙述正确的是| A.CHCl3是含有极性共价键的非极性分子 | B.H2O2中氧原子的杂化方式为sp2杂化 |
| C.COCl2的VSEPR模型为三角锥形 | D.HCl的沸点是同族氢化物中最低的 |
您最近一年使用:0次

 、
、 的说法正确的是
的说法正确的是 形成的
形成的 中,由
中,由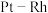 ”作用下发生转化的过程如图所示,下列分析合理的是
”作用下发生转化的过程如图所示,下列分析合理的是