回答下列问题。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)___________ ;
ⅱ.属于电解质的是___________ ;
ⅲ.属于非电解质的是___________ ;
ⅳ.既不是电解质又不是非电解质的是___________ 。
(2)ⅰ.配平下列离子方程式:___________ 。___________ 。
_____Fe(NO3)3+_______NaOH+______Cl2=____Na2FeO4+_____NaNO3+____NaCl+_____H2O
反应中___________ 元素被氧化,氧化剂与氧化产物的个数比为___________ 。
(1)今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸。其中:
ⅰ.能导电的是(填序号,下同)
ⅱ.属于电解质的是
ⅲ.属于非电解质的是
ⅳ.既不是电解质又不是非电解质的是
(2)ⅰ.配平下列离子方程式:
______MnO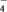 +_____H++______Cl-=_____Mn2++_____Cl2↑+_____H2O
+_____H++______Cl-=_____Mn2++_____Cl2↑+_____H2O
_____Fe(NO3)3+_______NaOH+______Cl2=____Na2FeO4+_____NaNO3+____NaCl+_____H2O
反应中
更新时间:2024-04-29 19:53:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(Ⅰ)现有下列物质。
①酒精②硫酸③ ④
④ 溶液⑤铁⑥小苏打⑦
溶液⑤铁⑥小苏打⑦ 胶体
胶体
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)⑥在水中的电离方程式为___________ 。
(3)向⑦中逐滴滴加②的溶液至过量,观察到的现象为___________ 。
(Ⅱ)在两份相同的 溶液中,分别滴入浓度相等的
溶液中,分别滴入浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

(4)图中曲线①代表滴加___________ 溶液的过程,曲线②中B点之前发生反应的离子方程式为___________ 。
(5)A、D点对应的溶液均显___________ (填“酸性”“中性”或“碱性”)
①酒精②硫酸③
 ④
④ 溶液⑤铁⑥小苏打⑦
溶液⑤铁⑥小苏打⑦ 胶体
胶体(1)属于电解质的是
(2)⑥在水中的电离方程式为
(3)向⑦中逐滴滴加②的溶液至过量,观察到的现象为
(Ⅱ)在两份相同的
 溶液中,分别滴入浓度相等的
溶液中,分别滴入浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
(4)图中曲线①代表滴加
(5)A、D点对应的溶液均显
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】观察氧化物和酸碱盐的关系:
回答下列问题:
(1)横向从价态的视角,发现氧化物的中心元素价态越高,往往___________ 性越强; 元素有
元素有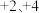 两种常见化合价,则对应氧化物碱性更强的是
两种常见化合价,则对应氧化物碱性更强的是___________ (填化学式)。
(2)纵向从对应酸碱盐的视角,发现氧化物与酸或碱反应生成盐时,酸性氧化物提供盐中___________ (填字母,下同),碱性氧化物提供盐中___________ 。
A.金属阳离子 B.氢离子 C.含氧酸根离子 D.氯离子
(3)已知 为紫红色。将
为紫红色。将 放入
放入 溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性: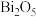
___________ ,
___________ 。
(4)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是___________ 。
②上述物质中既不是电解质也不是非电解质的是___________ 。
(5)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来。

①加水的烧杯为___________ (填字母)。
② 是三元酸,能生成
是三元酸,能生成 、
、 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸(
一种正盐。磷还有一种含氧酸叫亚磷酸( )。已知:
)。已知: 与
与 反应只生成
反应只生成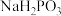 和
和 两种盐。那么
两种盐。那么 为
为___________ (填“正盐”或“酸式盐”);写出 (弱酸)与少量
(弱酸)与少量 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
| 氧化物 |  |  |  |  |  |  | 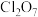 |
| 性质 | 强碱性 | 中强碱性 | 两性 | 弱酸性 | 中强酸性 | 强酸性 | 更强酸性 |
| 对应碱 |  |  |  | ||||
| 对应酸 | 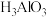 |  |  |  |  | ||
| 对应盐 |  |  | 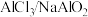 |  |  |  | 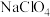 |
(1)横向从价态的视角,发现氧化物的中心元素价态越高,往往
 元素有
元素有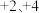 两种常见化合价,则对应氧化物碱性更强的是
两种常见化合价,则对应氧化物碱性更强的是(2)纵向从对应酸碱盐的视角,发现氧化物与酸或碱反应生成盐时,酸性氧化物提供盐中
A.金属阳离子 B.氢离子 C.含氧酸根离子 D.氯离子
(3)已知
 为紫红色。将
为紫红色。将 放入
放入 溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性: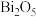

(4)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是
②上述物质中既不是电解质也不是非电解质的是
(5)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来。

①加水的烧杯为
②
 是三元酸,能生成
是三元酸,能生成 、
、 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸(
一种正盐。磷还有一种含氧酸叫亚磷酸( )。已知:
)。已知: 与
与 反应只生成
反应只生成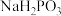 和
和 两种盐。那么
两种盐。那么 为
为 (弱酸)与少量
(弱酸)与少量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,下列物质括号内为厨卫物品的主要成分:①食盐 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液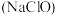 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:
(1)写出 在水中的电离方程式:
在水中的电离方程式:_______ 。
(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是_______ 。
(3)②③的主要成分可以归为一类物质,其分类的依据是_______ (填标号)。
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是_______ (用离子方程式表示)。
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:_______ (设有机酸化学式为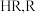 表示有机酸根)。
表示有机酸根)。
(6)欲用 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。
①用电子天平(精确度为 )称量
)称量 的质量为
的质量为_______ g,若配制过程中发现液面超过了刻度线,处理方法为_______ 。
②该“84”消毒液的物质的量浓度约为_______  (保留小数点后一位)。
(保留小数点后一位)。
 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液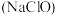 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:(1)写出
 在水中的电离方程式:
在水中的电离方程式:(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(3)②③的主要成分可以归为一类物质,其分类的依据是
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:
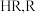 表示有机酸根)。
表示有机酸根)。(6)欲用
 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。①用电子天平(精确度为
 )称量
)称量 的质量为
的质量为②该“84”消毒液的物质的量浓度约为
 (保留小数点后一位)。
(保留小数点后一位)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)某兴趣小组做电解质导电实验,如图所示。
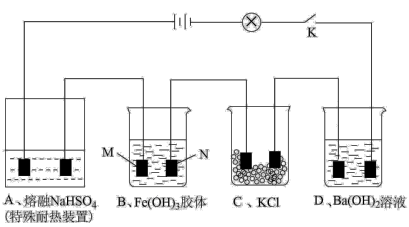
回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法___________ (写出一种方法即可)。
②装置A中电解质的电离方程式___________ ,在水溶液能与Fe反应生成氢气的离子方程式___________ 。
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是___________ (填①或②)。
②B点对应的溶液呈___________ (填“酸”、“碱”或“中”)性。
③起始点到D点之间发生反应的离子方程式为___________ 。
(1)某兴趣小组做电解质导电实验,如图所示。

回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法
②装置A中电解质的电离方程式
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是
②B点对应的溶液呈
③起始点到D点之间发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下为中学化学中常见的物质:
①熔融硝酸钾 ②HNO3 ③NaHSO4固体 ④SO3 ⑤铜 ⑥乙醇 ⑦CaCO3固体 ⑧烧碱,请按要求回答问题。
(1)以上物质中可以导电的是___________ ;属于电解质的是___________ 。
(2)属于酸的是___________ ;属于碱的是___________ ;属于盐的是___________ 。
(3)写出下列物质的电离方程式。
HNO3:___________ ;
NaHSO4:___________ ;
①熔融硝酸钾 ②HNO3 ③NaHSO4固体 ④SO3 ⑤铜 ⑥乙醇 ⑦CaCO3固体 ⑧烧碱,请按要求回答问题。
(1)以上物质中可以导电的是
(2)属于酸的是
(3)写出下列物质的电离方程式。
HNO3:
NaHSO4:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学源自生活和生产实践,并随着人类社会的进步而不断发展。根据所学知识,回答下列问题:
(1)分类是认识和研究物质及其变化的一种常用的科学方法,如图所示分类方法是__________ (选填“树状分类法”或“交叉分类法”)。
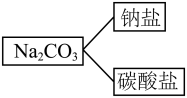
(2)下列物质:①液氯 ②盐酸 ③ ④硝酸钾固体 ⑤熔融
④硝酸钾固体 ⑤熔融 ⑥铜,其中属于电解质的是
⑥铜,其中属于电解质的是__________ (填序号,后同),能导电的是__________ ,④的电离方程式为__________ 。
(3) 所含化学键的类型
所含化学键的类型__________ 。
(4)氢化钠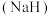 可在野外用作生氢剂,其原理为
可在野外用作生氢剂,其原理为 ,该反应的还原剂是
,该反应的还原剂是__________ (填化学式),生成 转移的电子数目为
转移的电子数目为__________ 。
(5)碳酸钠是一种重要的化工基本原料,俗称__________ ,向碳酸钠溶液中滴加少量稀盐酸,会生成 和
和__________ (填化学式)。除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法是__________ 。
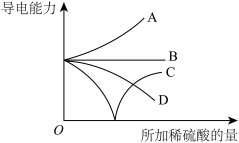
(6)向一定体积的 溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中
溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中__________ (填字母)所示。
(7)把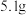 镁铝合金的粉末放入过量的盐酸中,充分反应后得到
镁铝合金的粉末放入过量的盐酸中,充分反应后得到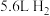 (标准状况),该合金中铝和镁的物质的量之比为
(标准状况),该合金中铝和镁的物质的量之比为__________ 。
(1)分类是认识和研究物质及其变化的一种常用的科学方法,如图所示分类方法是

(2)下列物质:①液氯 ②盐酸 ③
 ④硝酸钾固体 ⑤熔融
④硝酸钾固体 ⑤熔融 ⑥铜,其中属于电解质的是
⑥铜,其中属于电解质的是(3)
 所含化学键的类型
所含化学键的类型(4)氢化钠
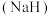 可在野外用作生氢剂,其原理为
可在野外用作生氢剂,其原理为 ,该反应的还原剂是
,该反应的还原剂是 转移的电子数目为
转移的电子数目为(5)碳酸钠是一种重要的化工基本原料,俗称
 和
和(6)向一定体积的
 溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中
溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中
(7)把
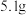 镁铝合金的粉末放入过量的盐酸中,充分反应后得到
镁铝合金的粉末放入过量的盐酸中,充分反应后得到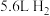 (标准状况),该合金中铝和镁的物质的量之比为
(标准状况),该合金中铝和镁的物质的量之比为
您最近一年使用:0次
【推荐1】根据反应NH3+Cl2=NH4Cl+N2回答下列问题。
(1)配平系数为___________ ,
(2)氧化剂___________ ,还原剂___________ ;
(3)1molNH3参与反应转移电子数是___________ (用 表示);
表示);
(4)当生成28gN2时,被氧化的物质的物质的量是___________ mol。
(1)配平系数为
(2)氧化剂
(3)1molNH3参与反应转移电子数是
 表示);
表示);氧化剂与氧化产物的质量比
(4)当生成28gN2时,被氧化的物质的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】海水中蕴含着丰富的资源,开发利用海水资源,可获得人类所需的物质。
(1)海水提盐后剩余的母液中含有较多 ,将母液用硫酸酸化后通入足量
,将母液用硫酸酸化后通入足量 ,可获得含
,可获得含 的海水,反应的离子方程式为
的海水,反应的离子方程式为_________ ,由此可知,氧化性
____________  (填“>”或“<”)。
(填“>”或“<”)。
(2)以上方法获得的含 的海水中
的海水中 的浓度较小,向其中通入
的浓度较小,向其中通入__________ 将 吹出并冷凝获得粗溴。
吹出并冷凝获得粗溴。
(3)向粗溴中通入 ,反应的化学方程式为
,反应的化学方程式为 ,该反应中氧化剂是
,该反应中氧化剂是________ (填化学式,下同),氧化产物是___________ 。若要消耗80g ,需要标准状况下
,需要标准状况下 的体积为
的体积为_______________ 。
(4)将贝壳煅烧成粉末,然后加入海水提盐后剩余的母液中,可获得 沉淀。然后将过滤出的沉淀溶于稀盐酸时,反应的化学方程式为
沉淀。然后将过滤出的沉淀溶于稀盐酸时,反应的化学方程式为_____________ 。
(1)海水提盐后剩余的母液中含有较多
 ,将母液用硫酸酸化后通入足量
,将母液用硫酸酸化后通入足量 ,可获得含
,可获得含 的海水,反应的离子方程式为
的海水,反应的离子方程式为
 (填“>”或“<”)。
(填“>”或“<”)。(2)以上方法获得的含
 的海水中
的海水中 的浓度较小,向其中通入
的浓度较小,向其中通入 吹出并冷凝获得粗溴。
吹出并冷凝获得粗溴。(3)向粗溴中通入
 ,反应的化学方程式为
,反应的化学方程式为 ,该反应中氧化剂是
,该反应中氧化剂是 ,需要标准状况下
,需要标准状况下 的体积为
的体积为(4)将贝壳煅烧成粉末,然后加入海水提盐后剩余的母液中,可获得
 沉淀。然后将过滤出的沉淀溶于稀盐酸时,反应的化学方程式为
沉淀。然后将过滤出的沉淀溶于稀盐酸时,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】配平下列方程式:
(1)____ P+____ Br2+____ H2O=____ H3PO4+____ HBr
(2)___ KMnO4+___ HCl(浓)=___ KCl+___ MnCl2+___ Cl2↑+___ H2O
(3)___ FeSO4 + ___ H2O + ___ O2 = ___ Fe2(SO4)3 + ___ Fe(OH)3
(1)
(2)
(3)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】HNO2是一种弱酸,且不稳定,易分解生成 NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成 Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有 Fe2+。若误食亚硝酸盐(如NaNO2 ),则导致血红蛋白中的 Fe2+转化为 Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_________ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将 Fe3+还原为 Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,能用来区分NaNO2和NaCl的是_____ (填序号)。
A.分别溶于水看溶解情况
B.在酸性条件下加入KI—淀粉溶液来区别
C.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和 HCl,请写出反应的离子方程式:____________________________________ 。
(4)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是______ (填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为 2∶1,试配平下列方程式:________________
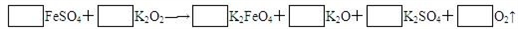 .
.
(1)人体正常的血红蛋白含有 Fe2+。若误食亚硝酸盐(如NaNO2 ),则导致血红蛋白中的 Fe2+转化为 Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将 Fe3+还原为 Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,能用来区分NaNO2和NaCl的是
A.分别溶于水看溶解情况
B.在酸性条件下加入KI—淀粉溶液来区别
C.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和 HCl,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为 2∶1,试配平下列方程式:
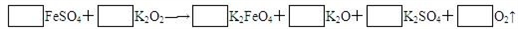 .
.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。
请回答下列问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: 。
。 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。
(1)物质(甲)为_______ (填化学式)。
(2)反应中若产生5molNO分子,则转移电子的数目是_______ 。
Ⅱ.亚硝酸钠( )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生如下反应:
会使人中毒。已知亚硝酸钠能发生如下反应: 。
。
(3)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为_______ 。
(4)自来水中的 对人类健康会产生危害碱性条件下Al粉还原
对人类健康会产生危害碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。_______
_______Al+_______ +_______
+_______ _______
_______ _______
_______ _______
_______
请回答下列问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 。
。 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。(1)物质(甲)为
(2)反应中若产生5molNO分子,则转移电子的数目是
Ⅱ.亚硝酸钠(
 )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生如下反应:
会使人中毒。已知亚硝酸钠能发生如下反应: 。
。(3)用双线桥法标出该反应中电子转移的方向及数目:
(4)自来水中的
 对人类健康会产生危害碱性条件下Al粉还原
对人类健康会产生危害碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。_______Al+_______
 +_______
+_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次

 MnCl2+Cl2↑+2H2O的反应中,用“双线桥法”表示氧化还原反应中电子转移情况
MnCl2+Cl2↑+2H2O的反应中,用“双线桥法”表示氧化还原反应中电子转移情况

