用可溶性 溶液生产纳米
溶液生产纳米 的一种工艺流程如下:
的一种工艺流程如下:
 溶液生产纳米
溶液生产纳米 的一种工艺流程如下:
的一种工艺流程如下: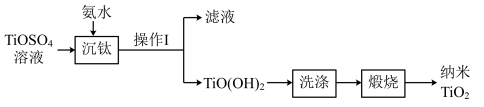
| A.实验室中进行“操作Ⅰ”时,需要的玻璃仪器有烧杯、玻璃棒、普通漏斗 |
B.“沉钛”时反应的离子方程式为: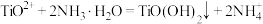 |
C.回收“滤液”中的 时,高温灼烧有利于提高其产率 时,高温灼烧有利于提高其产率 |
D.空气与纳米 所形成的分散系,可检测出有丁达尔效应 所形成的分散系,可检测出有丁达尔效应 |
更新时间:2024-04-30 10:51:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列概念或分类法正确的是
| A.含氧元素的化合物叫氧化物 |
| B.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| C.根据水溶液是否能够导电,将物质分为电解质和非电解质 |
| D.有电子转移的化学反应叫氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是
①向石灰水中逐渐通入过量CO2
②向Ca(ClO)2溶液中逐渐通入过量SO2
③向氢氧化铝胶体中逐滴滴入过量稀NaOH溶液
④向氯化钡溶液中逐渐通入过量二氧化硫
⑤向AgNO3溶液中逐滴滴入过量稀氨水
⑥向饱和碳酸钠溶液中逐渐通入过量二氧化碳
①向石灰水中逐渐通入过量CO2
②向Ca(ClO)2溶液中逐渐通入过量SO2
③向氢氧化铝胶体中逐滴滴入过量稀NaOH溶液
④向氯化钡溶液中逐渐通入过量二氧化硫
⑤向AgNO3溶液中逐滴滴入过量稀氨水
⑥向饱和碳酸钠溶液中逐渐通入过量二氧化碳
| A.①②⑥ | B.①③⑤ | C.②④⑥ | D.③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列相关离子方程式书写正确的是
| A.泡沫灭火器工作原理:2A13++3CO32-+3H2O=2Al(OH)3↓+3CO2↑ |
| B.Fe(OH)3溶于HI溶液:Fe(OH)3+3H+=Fe3++3H2O |
| C.往Ba(OH)2溶液中滴加KHSO4溶液至溶液呈中性: Ba2++OH-+H++SO42-=BaSO4+H2O |
| D.酸性高锰酸钾溶液与草酸溶液混合:2MnO4-+5H2C2O42-+6H+=2Mn2++10CO2↑+8H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列离子方程式正确的是
| A.足量的CO2通入饱和碳酸钠溶液中: CO2+CO32-+H2O=2HCO3- |
| B.FeSO4溶液在空气中变质:4Fe2++O2+2H2O=4Fe3++4OH- |
| C.次氯酸钙溶液中通入足量二氧化硫:Ca2++ClO-+SO2+H2O=CaSO4↓+Cl-+2H+ |
| D.碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO3-+2Ca2++4OH— =2CaCO3↓+ Mg(OH)2↓+ 2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列实验操作以及现象能得到正确实验结论的是
实验操作及现象 | 实验结论 | |
A | 用 |
|
B | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了取代反应 |
C | 将 | 证明 |
D | 将 | 分解产物中一定不含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.CO2的水溶液能导电,所以CO2是电解质 |
| B.氧化剂在反应中得到的电子越多,氧化能力越强 |
| C.用加热法可分离I2和NH4HCO3两种固体 |
| D.氧化性:Cl2>I2,还原性:I->Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
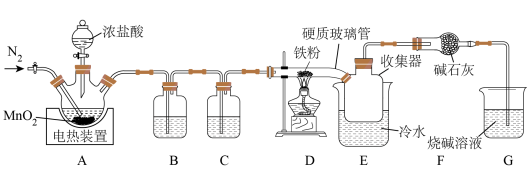
【推荐1】某实验小组采用下图装置模拟干法制备 。已知
。已知 在空气中易潮解,受热易升华。下列说法错误的是
在空气中易潮解,受热易升华。下列说法错误的是
 。已知
。已知 在空气中易潮解,受热易升华。下列说法错误的是
在空气中易潮解,受热易升华。下列说法错误的是
| A.装置A中浓盐酸体现酸性和还原性 |
| B.装置B、C中分别盛放饱和食盐水和浓硫酸 |
C.装置D、E直接相连可防止生成的 冷凝后造成堵塞 冷凝后造成堵塞 |
D.装置F的主要作用是防止 排放到空气中,造成环境污染 排放到空气中,造成环境污染 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知氯气和空气按体积比1∶3混合通入潮湿的碳酸钠中能生成Cl2O,且反应放热;不含Cl2的Cl2O易与水反应生成HClO;Cl2O在42℃以上会分解生成Cl2和O2。设计如图装置(部分夹持装置略)制备HClO,每个虚线框表示一个装置单元,其中存在错误的是
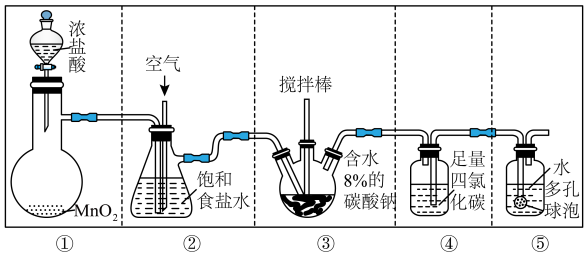

| A.②③⑤ | B.①④⑤ | C.①②④ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列用氯气氧化K2MnO4制备KMnO4,氧化过程中会产生MnO2杂质。实验原理和装置不能达到实验目的的是
A.制取Cl2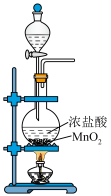 | B.除去Cl2中的少量HCl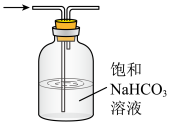 |
C.制备 KMnO4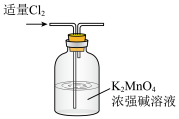 | D.分离 MnO2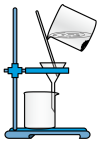 |
您最近一年使用:0次

 溶液中加入H2S:
溶液中加入H2S:
 H2+Cl2↑+2OH-
H2+Cl2↑+2OH-
 [CuCl4]2-+4H2O
[CuCl4]2-+4H2O 试纸测得
试纸测得 溶液的
溶液的 溶液的
溶液的 电离出
电离出 的能力比
的能力比 的强
的强 气体通入浓度均为
气体通入浓度均为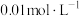 的
的 和
和 溶液中,只出现
溶液中,只出现 黑色沉淀
黑色沉淀
 受热分解产生的气体通入
受热分解产生的气体通入 溶液,产生白色沉淀
溶液,产生白色沉淀



