除去废水中Cr( )的方法有多种。请按要求回答下列问题。
)的方法有多种。请按要求回答下列问题。
(1)NaHSO3与熟石灰除Cr( )法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
①实验中NaHSO3的作用是___________ 。
②Cr( )在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(
)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr( )去除率下降的原因可用离子方程式表示为
)去除率下降的原因可用离子方程式表示为___________ 。
用硫酸盐还原菌(SRB)处理含Cr( )的废水时,Cr(
)的废水时,Cr( )去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是
)去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是___________ 。
①“酸浸、还原”时,反应的化学方程式为___________ 。
该步骤若pH过低,则消耗Na2S2O5的量比理论值高出许多,其原因是___________ (文字叙述)。
②“沉铬”时所发生反应的离子方程式为___________ 。能不能将纯碱改为足量NaOH溶液?___________ 。(给出结论,并结合离子方程式给出理由)
 )的方法有多种。请按要求回答下列问题。
)的方法有多种。请按要求回答下列问题。(1)NaHSO3与熟石灰除Cr(
 )法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。
)法:向酸性废水中加入NaHSO3,再加入熟石灰,使Cr3+沉淀。①实验中NaHSO3的作用是
②Cr(
 )在水溶液中的存在形态分布如图1所示。当pH>12时,Cr(
)在水溶液中的存在形态分布如图1所示。当pH>12时,Cr( )去除率下降的原因可用离子方程式表示为
)去除率下降的原因可用离子方程式表示为
用硫酸盐还原菌(SRB)处理含Cr(
 )的废水时,Cr(
)的废水时,Cr( )去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是
)去除率随温度的变化如图2所示。55 ℃时,Cr(Ⅵ)去除率很低的原因是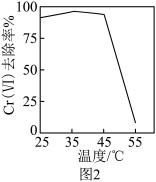

①“酸浸、还原”时,反应的化学方程式为
该步骤若pH过低,则消耗Na2S2O5的量比理论值高出许多,其原因是
②“沉铬”时所发生反应的离子方程式为
2024高三·全国·专题练习 查看更多[1]
(已下线)FHgkyldyjhx02
更新时间:2024-05-02 15:13:40
|
相似题推荐
【推荐1】按要求填空。
(1)配平氧化还原离子方程式:____Cu+_____NO +_____H+ =_____NO↑+____Cu2++_____H2O
+_____H+ =_____NO↑+____Cu2++_____H2O ___________
(2)已知KMnO4 与浓盐酸室温下可发生如下反应:2KMnO4 +16HCl浓=2KCl+2MnCl2 +5Cl2 +8H2O
①用“双线桥法”标出上述反应的电子转移情况。__________ 2KMnO4 +16HCl浓=2KCl+2MnCl2 +5Cl2 +8H2O
②该反应的离子反应方程式为___________ ,此反应体现 HCl的___________ 性和___________ 性,氧化剂与还原剂个数比为___________ , 生成 71gCl2 时消耗的还原剂的质量为___________ g
③若分别用①KMnO4(还原产物是 Mn2+);②MnO2+(还原产物是 Mn2+)氧化浓盐酸制备氯气,当浓盐酸足量且消耗 KMnO4 和 MnO2+这两种氧化剂的数目相同时,生成氯气分子的数目之比是___________ 。
(1)配平氧化还原离子方程式:____Cu+_____NO
 +_____H+ =_____NO↑+____Cu2++_____H2O
+_____H+ =_____NO↑+____Cu2++_____H2O (2)已知KMnO4 与浓盐酸室温下可发生如下反应:2KMnO4 +16HCl浓=2KCl+2MnCl2 +5Cl2 +8H2O
①用“双线桥法”标出上述反应的电子转移情况。
②该反应的离子反应方程式为
③若分别用①KMnO4(还原产物是 Mn2+);②MnO2+(还原产物是 Mn2+)氧化浓盐酸制备氯气,当浓盐酸足量且消耗 KMnO4 和 MnO2+这两种氧化剂的数目相同时,生成氯气分子的数目之比是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)五氧化铬又称过氧化铬,其中Cr元素的化合价为+6价,则每个 分子中存在过氧键的数目为
分子中存在过氧键的数目为_______ 个。
(2)过氧化尿素[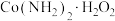 ]是一种白色晶体,可用于漂白、消毒和增氧剂,在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5),重铬酸钾与
]是一种白色晶体,可用于漂白、消毒和增氧剂,在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5),重铬酸钾与 反应的离子方程式为
反应的离子方程式为_______ ,上述反应_______ (填“是”或“不是”)氧化还原反应。
(1)五氧化铬又称过氧化铬,其中Cr元素的化合价为+6价,则每个
 分子中存在过氧键的数目为
分子中存在过氧键的数目为(2)过氧化尿素[
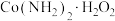 ]是一种白色晶体,可用于漂白、消毒和增氧剂,在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5),重铬酸钾与
]是一种白色晶体,可用于漂白、消毒和增氧剂,在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5),重铬酸钾与 反应的离子方程式为
反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学与生产、生活、环境息息相关。从化学视角回答下列问题:
(1)我国科学家研发了一种室温下“可呼吸”的Na—CO2充电电池。电池的总反应为:3CO2+4Na=2Na2CO3+C,该电池中不能存在水,否则可能引起电池爆炸,用离子方程式表示其原因_______ ;
(2)亚硝酸钠被称为工业盐,有毒,但在肉类制品加工中又可以加入极少量用作发色剂、防微生物剂、防腐剂,在漂白、电镀和金属处理等方面有应用。已知NaNO2能发生反应:_______NaNO2+_______HI→_______NO↑+_______I2+_______NaI+_______H2O
①配平并写出上述化学方程式_______ ;
②该反应中HI表现的性质是_______ ;氧化剂与还原剂的个数之比为_______ 。
(1)我国科学家研发了一种室温下“可呼吸”的Na—CO2充电电池。电池的总反应为:3CO2+4Na=2Na2CO3+C,该电池中不能存在水,否则可能引起电池爆炸,用离子方程式表示其原因
(2)亚硝酸钠被称为工业盐,有毒,但在肉类制品加工中又可以加入极少量用作发色剂、防微生物剂、防腐剂,在漂白、电镀和金属处理等方面有应用。已知NaNO2能发生反应:_______NaNO2+_______HI→_______NO↑+_______I2+_______NaI+_______H2O
①配平并写出上述化学方程式
②该反应中HI表现的性质是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】2021年是国际化学年十周年纪念,中国的宣传口号是“化学一我们的生活,我们的未来”。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
(2)工业上常用金属钠冶炼钛,是利用金属钠的强_______ 性。
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为_______ 。
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯_______ (填“I”或“II”)中澄清石灰水变浑浊。加热后试管中发生反应的化学方程式为_______ 。

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式_______ 。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
| A.晶体硅用于制作半导体材料 | B.硅在常温下化学性比较活泼 |
| C.玻璃属于硅酸盐材料 | D.玛瑙的主要成分是硅单质 |
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一定条件下,无机物可以转化为有机物。例如,干冰与液氨反应可生成氨基甲酸铵(NH2COONH4),氨基甲酸铵受热可转化为尿素[CO(NH2)2]。新近研究发现,海底热液中有CO2和H2等无机物,还有可能通过非生物途径形成CH4等烃类。请回答:
(1)干冰与液氨反应生成氨基甲酸铵的化学方程式____________ 。
(2)氨基甲酸铵受热转化为尿素的化学方程式______________ 。
(3)有人推测,海底热液中CH4由CO2和H2反应生成。请说明该推测的合理性______ 。
(4)也有人推测,海底热液中的CH4由海底矿物直接生成。热液条件(如50 MPa,300℃)下,矿物中NaHCO3、Fe与H2O反应生成CH4的化学方程式____________ 。
(1)干冰与液氨反应生成氨基甲酸铵的化学方程式
(2)氨基甲酸铵受热转化为尿素的化学方程式
(3)有人推测,海底热液中CH4由CO2和H2反应生成。请说明该推测的合理性
(4)也有人推测,海底热液中的CH4由海底矿物直接生成。热液条件(如50 MPa,300℃)下,矿物中NaHCO3、Fe与H2O反应生成CH4的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④氨气;⑤葡萄糖;⑥氯化镁;⑦ ;⑧氯水;⑨
;⑧氯水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有_______ ,属于非电解质的有_______ 。
(2)④的电子式为_______ 。
(3)用电子式表示⑥的形成过程_______ 。
(4)除去③中少量②的相应化学方程式为_______ 。
(5)⑦中含有的化学键为_______ 。
II.写出下列反应的离子方程式(已知还原性: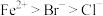 ):
):
(6)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)_______ ;
(7)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶_______ 。
 ;⑧氯水;⑨
;⑧氯水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
(4)除去③中少量②的相应化学方程式为
(5)⑦中含有的化学键为
II.写出下列反应的离子方程式(已知还原性:
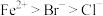 ):
):(6)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)(7)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学与生活息息相关,请用化学知识分析下列问题
(1)从鸡蛋白溶液中提取蛋白质的方法是________ 。
(2)误食重金属盐会中毒,这是因为________________________________________________________________________ 。
(3)浓HNO3溅在皮肤上,使皮肤呈现______ 色,这是由于浓HNO3和蛋白质发生了________ 反应。
(1)从鸡蛋白溶液中提取蛋白质的方法是
(2)误食重金属盐会中毒,这是因为
(3)浓HNO3溅在皮肤上,使皮肤呈现
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.生活中的有机物种类丰富,在衣、食、住、行等方面应用广泛。
(1)乙醇是无色有特殊香味的液体。乙醇官能团的名称为_______ 。
(2)工业上用乙烯与水在一定条件下反应可制得乙醇,该反应的化学方程式为_______ 。
(3)下列属于乙醇的同系物的是_______ ,属于乙醇的同分异构体的是_______ 。(填字母)
a.甲醇( ) b.
) b.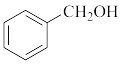 c.乙醚(
c.乙醚(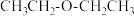 ) d.
) d.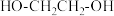 e.
e.
Ⅱ.糖尿病是由于体内胰岛素分泌紊乱导致的代谢紊乱综合征。长期摄入高热量食品和缺少运动都易导致糖尿病。
(4)木糖醇[ ]是一种天然甜味剂,在人体中的代谢不受胰岛素调节,可作为糖尿病人的热能源。请预测木糖醇的一种化学性质:
]是一种天然甜味剂,在人体中的代谢不受胰岛素调节,可作为糖尿病人的热能源。请预测木糖醇的一种化学性质:_______ 。
(5)糖尿病病人宜多吃蔬菜和豆类食品。蔬菜中富含纤维素,豆类食品中富含蛋白质。下列说法错误的是_______ 。(填字母)
a.蛋白质都属于天然有机高分子化合物,蛋白质都不溶于水
b.用灼烧闻气味的方法可以区别合成纤维和羊毛
c.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
d.紫外线、医用酒精能杀菌消毒,是因为它们能使细菌的蛋白质变性
e.用天然彩棉制成贴身衣物可减少染料对人体的副作用
(1)乙醇是无色有特殊香味的液体。乙醇官能团的名称为
(2)工业上用乙烯与水在一定条件下反应可制得乙醇,该反应的化学方程式为
(3)下列属于乙醇的同系物的是
a.甲醇(
 ) b.
) b. c.乙醚(
c.乙醚(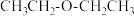 ) d.
) d.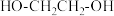 e.
e.
Ⅱ.糖尿病是由于体内胰岛素分泌紊乱导致的代谢紊乱综合征。长期摄入高热量食品和缺少运动都易导致糖尿病。
(4)木糖醇[
 ]是一种天然甜味剂,在人体中的代谢不受胰岛素调节,可作为糖尿病人的热能源。请预测木糖醇的一种化学性质:
]是一种天然甜味剂,在人体中的代谢不受胰岛素调节,可作为糖尿病人的热能源。请预测木糖醇的一种化学性质:(5)糖尿病病人宜多吃蔬菜和豆类食品。蔬菜中富含纤维素,豆类食品中富含蛋白质。下列说法错误的是
a.蛋白质都属于天然有机高分子化合物,蛋白质都不溶于水
b.用灼烧闻气味的方法可以区别合成纤维和羊毛
c.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
d.紫外线、医用酒精能杀菌消毒,是因为它们能使细菌的蛋白质变性
e.用天然彩棉制成贴身衣物可减少染料对人体的副作用
您最近半年使用:0次
【推荐3】糖类、油脂和蛋白质都是生命中重要的有机物质。
(1)淀粉在硫酸作用下可发生水解反应,检验淀粉未完全水解的试剂为__ 。
(2)韩国出现中东呼吸综合征疫情的,防疫人员用84消毒液对地铁进行消毒,这是利用了蛋白质的___ (填序号)性质。
a.两性 b.水解 c.变性 d.盐析
(3)某油脂A的结构简式为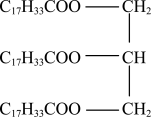 。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是__ (写结构简式)。
(4)聚丙烯酸钠、涤纶的结构简式如图:
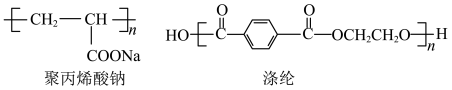
合成聚丙烯酸钠的单体的结构简式是__ ,合成聚丙烯酸钠的反应类型是__ 。合成涤纶的单体有两种,其中能和Na2CO3反应的单体的结构简式是__ ;该单体核磁共振氢谱的峰面积之比是__ 。
(1)淀粉在硫酸作用下可发生水解反应,检验淀粉未完全水解的试剂为
(2)韩国出现中东呼吸综合征疫情的,防疫人员用84消毒液对地铁进行消毒,这是利用了蛋白质的
a.两性 b.水解 c.变性 d.盐析
(3)某油脂A的结构简式为
 。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是(4)聚丙烯酸钠、涤纶的结构简式如图:

合成聚丙烯酸钠的单体的结构简式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)柚皮精油可采用水蒸气蒸馏法提取,它是利用__________ 将__________ 较强的柚皮精油携带出来,形成油水混合物。在油水混合物中,加入__________ 可使油水出现明显分层;分离得到的油层应加入__________ 进行除水。
(2)水蒸气蒸馏易使柚皮精油有效成分部分水解,为避免此缺点,可采用__________ 法提取柚皮精油。为提高出油率,需先对柚皮进行的处理是__________ ,以分解果胶。
(3)青蒿素易溶于有机溶剂,60℃以上易分解,宜采用萃取法提取。现有四氯化碳(沸点76.5℃)和乙醚(沸点34.5℃)两种溶剂,应选用__________ 作为萃取剂,不选用另外一种的理由是__________ 。
(1)柚皮精油可采用水蒸气蒸馏法提取,它是利用
(2)水蒸气蒸馏易使柚皮精油有效成分部分水解,为避免此缺点,可采用
(3)青蒿素易溶于有机溶剂,60℃以上易分解,宜采用萃取法提取。现有四氯化碳(沸点76.5℃)和乙醚(沸点34.5℃)两种溶剂,应选用
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】8.34g FeSO4·7H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。回答下列问题:
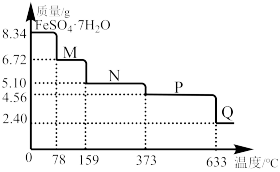
(1)试确定200℃时固体物质N的化学式___________ 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式___________ 。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
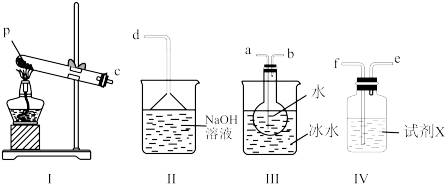
①试剂X的名称是___________ 。
②按气流方向连接仪器,用字母表示接口的连接顺序:c→___________ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为___________ g.(填计算式)

(1)试确定200℃时固体物质N的化学式
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。

①试剂X的名称是
②按气流方向连接仪器,用字母表示接口的连接顺序:c→
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空:
(1)有机物C常用于食品行业。已知9.0gC在足量 中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为
中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为 。
。
①C分子的质谱图如图所示,则C的分子式是_______ 。

②C能与 溶液发生反应,C一定含有的官能团名称是
溶液发生反应,C一定含有的官能团名称是_______ 。
③C分子的核磁共振氢谱有4组峰,峰面积之比是1:1:1:3,则C的结构简式是_______ 。
④0.2molC与足量Na反应,在标准状况下产生 的体积是
的体积是_______ L。
(2)国际化学年中国宣传口号是“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。Na2CO3和NaHCO3是日常生活中经常遇到的物质。请填空:
①甲组同学为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将20g样品加热至质量不再发生变化,其质量变为16.9g,则该Na2CO3样品的纯度(质量分数)是_______ 。
②混合样品中碳酸钠的质量分数,也可通过加热分解得到的CO2质量进行计算,乙组同学设计的实验装置示意图如下,则下列说法正确的是_______ 。

A.X气体可以是空气,反应前和反应后均需通一段时间空气
B.没有a装置会导致所测碳酸钠的质量分数偏高
C.装置B、C之间缺少CO2的干燥装置
D.a装置内应装碱石灰,目的是为了尾气处理
(1)有机物C常用于食品行业。已知9.0gC在足量
 中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为
中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为 。
。①C分子的质谱图如图所示,则C的分子式是

②C能与
 溶液发生反应,C一定含有的官能团名称是
溶液发生反应,C一定含有的官能团名称是③C分子的核磁共振氢谱有4组峰,峰面积之比是1:1:1:3,则C的结构简式是
④0.2molC与足量Na反应,在标准状况下产生
 的体积是
的体积是(2)国际化学年中国宣传口号是“化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。Na2CO3和NaHCO3是日常生活中经常遇到的物质。请填空:
①甲组同学为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将20g样品加热至质量不再发生变化,其质量变为16.9g,则该Na2CO3样品的纯度(质量分数)是
②混合样品中碳酸钠的质量分数,也可通过加热分解得到的CO2质量进行计算,乙组同学设计的实验装置示意图如下,则下列说法正确的是

A.X气体可以是空气,反应前和反应后均需通一段时间空气
B.没有a装置会导致所测碳酸钠的质量分数偏高
C.装置B、C之间缺少CO2的干燥装置
D.a装置内应装碱石灰,目的是为了尾气处理
您最近半年使用:0次



