8.34g FeSO4·7H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。回答下列问题:
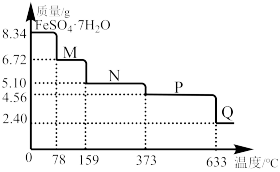
(1)试确定200℃时固体物质N的化学式___________ 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式___________ 。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
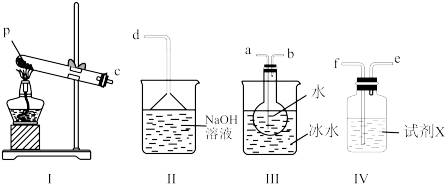
①试剂X的名称是___________ 。
②按气流方向连接仪器,用字母表示接口的连接顺序:c→___________ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为___________ g.(填计算式)

(1)试确定200℃时固体物质N的化学式
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。

①试剂X的名称是
②按气流方向连接仪器,用字母表示接口的连接顺序:c→
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为
21-22高三上·辽宁大连·阶段练习 查看更多[2]
更新时间:2021-10-19 00:37:11
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室有一瓶敞口放置一段时间的氢氧化钠固体,为测定该瓶样品中氢氧化钠的质量分数,现取17.3g该样品溶于足量的水中(固体完全溶解),向所得溶液中逐滴加入200g一定溶质质量分数的稀盐酸,实验过程如图所示(不考虑碳酸钠的分步反应)。
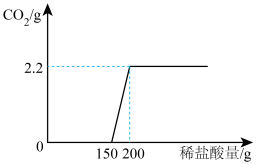
(1)经分析,该氢氧化钠固体_______ (填“部分”或“完全”)变质,恰好完全反应时,产生气体的质量为_______ g。
(2)计算样品中氢氧化钠的质量_______ (写出计算过程)。

(1)经分析,该氢氧化钠固体
(2)计算样品中氢氧化钠的质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧气是支持生命活动的一种重要物质,回答下列问题:
(1)氧气的摩尔质量为_______ 。
(2)现有0.5molO2,含氧原子物质的量为_______ 含氧分子数为_______ 个,其体积(标准状况)为_______ ,其质量为_______ 。
(3)氧气与炭在一定条件下发生反应可以生成 CO和CO2。在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:
①CO2和CO的物质的量之比是_______ 。
②CO2和CO的体积之比是_______ 。
③CO2和CO的质量之比是_______ 。
(1)氧气的摩尔质量为
(2)现有0.5molO2,含氧原子物质的量为
(3)氧气与炭在一定条件下发生反应可以生成 CO和CO2。在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:
①CO2和CO的物质的量之比是
②CO2和CO的体积之比是
③CO2和CO的质量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列填空。
(1)将3.22g芒硝(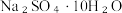 )溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为___________ 。
(2)写出工业制备漂白粉的化学反应方程式___________
(3)碳酸氢钠受热分解的化学反应方程式___________
(4)写出过氧化钠与水反应的化学方程式___________
(5)写出向饱和碳酸钠溶液中通入二氧化碳反应的化学方程式___________
(6)写出钠与硫酸铜溶液反应的化学方程式___________
(7)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体的物质的量为___________ ;
②实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在___________ 刻度处。
(1)将3.22g芒硝(
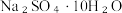 )溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为(2)写出工业制备漂白粉的化学反应方程式
(3)碳酸氢钠受热分解的化学反应方程式
(4)写出过氧化钠与水反应的化学方程式
(5)写出向饱和碳酸钠溶液中通入二氧化碳反应的化学方程式
(6)写出钠与硫酸铜溶液反应的化学方程式
(7)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体的物质的量为
②实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)写出以下反应的化学反应方程式
①三氧化二铁与稀硫酸反应:______
②氢氧化铝药物治疗胃酸(主要成分为盐酸)过多:______
③氢氧化钠溶液吸收少量二氧化硫气体:______
(2)已知CO和CO2的混合气体18.0g在标准状况下所占的体积为11.2L。则该混合气体中,CO2的物质的量为____ mol。
(3)在同温同压下,若A容器中的O2和B容器中的SO2所含的氧原子总数 相等,则A容器和B容器的体积比是____ 。
①三氧化二铁与稀硫酸反应:
②氢氧化铝药物治疗胃酸(主要成分为盐酸)过多:
③氢氧化钠溶液吸收少量二氧化硫气体:
(2)已知CO和CO2的混合气体18.0g在标准状况下所占的体积为11.2L。则该混合气体中,CO2的物质的量为
(3)在同温同压下,若A容器中的O2和B容器中的SO2所含的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: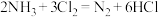 。当
。当 过量时,会发生反应
过量时,会发生反应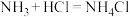 ,产生白烟,因此当
,产生白烟,因此当 和
和 比例不同时,产物有差异。
比例不同时,产物有差异。
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳比例为
的最佳比例为_______ 。该反应可用于检验化工生产中氯气是否泄漏。若氯气有少量泄漏,用氨气检验时有明显现象,此过程中发生反应的 和
和 的体积比范围为
的体积比范围为_______ 。
(2)体积为 ,质量为
,质量为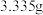 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为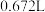 (其中
(其中 体积分数为50%)。两位同学想要根据这些数据计算被氧化的
体积分数为50%)。两位同学想要根据这些数据计算被氧化的 的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: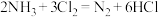 。当
。当 过量时,会发生反应
过量时,会发生反应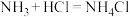 ,产生白烟,因此当
,产生白烟,因此当 和
和 比例不同时,产物有差异。
比例不同时,产物有差异。(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
 和
和 的最佳比例为
的最佳比例为 和
和 的体积比范围为
的体积比范围为(2)体积为
 ,质量为
,质量为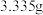 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为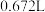 (其中
(其中 体积分数为50%)。两位同学想要根据这些数据计算被氧化的
体积分数为50%)。两位同学想要根据这些数据计算被氧化的 的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)| 学生编号 | 所列第一步算式 | 未知数X表示的意义 |
| 甲 | 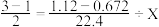 | |
| 乙 | 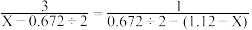 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。
(1)已知Na2S2O5中O元素的化合价为-2,则S元素的化合价为_______ 。Na2S2O5在酸性条件下会放出SO2,其反应的离子方程式为_______ 。
(2)Na2S2O5是一种食品添加剂、Na2S2O5晶体中常含有 。
。
①Na2S2O5作脱氧剂时的反应原理为 ,用单线桥法标出该反应中电子转移的数目和方向:
,用单线桥法标出该反应中电子转移的数目和方向:_______ 。
②检验其中含有 的方法是
的方法是_______ 。
(3)葡萄酒中常加入Na2S2O5作抗氧化剂。测定某葡萄酒中Na2S2O5残留量的实验方法如下:取20.00mL葡萄酒样品,慢慢滴加5.00mL0.010mol/LI2标准液恰好反应(以淀粉溶液作指示剂)。已知实验过程中发生的反应为 。计算该葡萄酒中Na2S2O5的残留量为
。计算该葡萄酒中Na2S2O5的残留量为_______ mol/L。
(1)已知Na2S2O5中O元素的化合价为-2,则S元素的化合价为
(2)Na2S2O5是一种食品添加剂、Na2S2O5晶体中常含有
 。
。①Na2S2O5作脱氧剂时的反应原理为
 ,用单线桥法标出该反应中电子转移的数目和方向:
,用单线桥法标出该反应中电子转移的数目和方向:②检验其中含有
 的方法是
的方法是(3)葡萄酒中常加入Na2S2O5作抗氧化剂。测定某葡萄酒中Na2S2O5残留量的实验方法如下:取20.00mL葡萄酒样品,慢慢滴加5.00mL0.010mol/LI2标准液恰好反应(以淀粉溶液作指示剂)。已知实验过程中发生的反应为
 。计算该葡萄酒中Na2S2O5的残留量为
。计算该葡萄酒中Na2S2O5的残留量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______  填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
 是强氧化性的盐
是强氧化性的盐
 固体保存需要防潮
固体保存需要防潮
 其消毒和净化水的原理相同
其消毒和净化水的原理相同
 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:_______
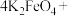 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个 时,转移的电子数为
时,转移的电子数为_______ 个
(5)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______  。
。
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈 的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附 性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5 mg K2FeO4即可达到卫生标准 ... ... |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是 是强氧化性的盐
是强氧化性的盐 固体保存需要防潮
固体保存需要防潮 其消毒和净化水的原理相同
其消毒和净化水的原理相同 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味(4)将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整: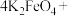 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个
 时,转移的电子数为
时,转移的电子数为(5)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象_____ 。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测,写出Mg与NO2反应的化学方程式_____ 。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)。
资料信息:2NO2+2NaOH=NaNO3+NaNO2+H2O。

①装置A中的试剂是_____ 。
②干燥管和装置B的作用分别是_____ 、_____ 。
③实验开始时正确的操作步骤是_____ 。
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红棕色气体后,关闭弹簧夹
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测,写出Mg与NO2反应的化学方程式
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)。
资料信息:2NO2+2NaOH=NaNO3+NaNO2+H2O。

①装置A中的试剂是
②干燥管和装置B的作用分别是
③实验开始时正确的操作步骤是
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红棕色气体后,关闭弹簧夹
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测定。
第一组,取刚降到地面的酸雨水样,进行了如下实验:
①将一片红色的玫瑰花瓣浸在一份水样中;②向雨水试样中滴加氯化钡溶液,有白色浑浊出现;③每隔一定时间测定其pH,数据如表Ⅰ所示。
表Ⅰ 不同时间酸雨的pH
(1)一段时间后,观察到红色变浅,可能的原因_______ 。
(2)生成白色浑浊的离子方程式_______ 。
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示)_______ 。
第一组,取刚降到地面的酸雨水样,进行了如下实验:
①将一片红色的玫瑰花瓣浸在一份水样中;②向雨水试样中滴加氯化钡溶液,有白色浑浊出现;③每隔一定时间测定其pH,数据如表Ⅰ所示。
表Ⅰ 不同时间酸雨的pH
| 测定时间/小时 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(1)一段时间后,观察到红色变浅,可能的原因
(2)生成白色浑浊的离子方程式
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某实验小组设计实验证明某碳酸钠粉末中混有硫酸钠和氯化钠,请完成下列空白:
| 实验步骤 | 实验现象 | 有关化学方程式 |
| ⑴取少量样品于试管中,加蒸馏水配成溶液。在溶液中先加足量的HNO3溶液 | 有气泡产生 | |
| ⑵再向(1)的溶液中加入过量的 | 产生白色沉淀 | |
| ⑶取(2)静置后的上层清液少许,滴加AgNO3溶液 | ||
| 结论:碳酸钠粉末中混有硫酸钠和氯化钠 | ||
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】已知某一种燃料含碳、氢和氧三种元素,为测定该燃料的组成:将该燃料放入到足量氧气中燃烧,并使产生的CO2与H2O蒸气以及剩余的O2全部通过如下图所示的装置,得到如下表所列出的实验数据(假设生成的气体是全部被吸收)。
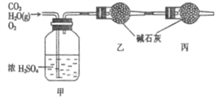
根据实验数据填空:
(1)该燃料分子中碳、氢原子的数目比为_______ 。
(2)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为________________ 。

| 实验前 | 实验后 | |
| 甲的质量 / g | 101.1 | 103.8 |
| 乙的质量 / g | 82.0 | 86.4 |
根据实验数据填空:
(1)该燃料分子中碳、氢原子的数目比为
(2)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度 2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:

(1) 写出本题中由乙醇制备1,2-二溴乙烷的两个化学反应方程式:
①____________________________________________ ,反应类型为________________ 。
②____________________________________________ ,反应类型为________________ 。
(2)装置b可以充当安全瓶,防止倒吸,例如:若装置a、b上方气体压强减小,则装置b中的现象为________________________________________________________________ 。
(3)容器c中NaOH溶液的作用是:________________________________ ;若无c装置,则d中发生副反应 的离子方程式为________________________________________ 。
(4)在做此实验时,应使a装置中的液体温度迅速升高到所需温度,请用化学方程式表示其原因_____________________________________________________________ 。

(1) 写出本题中由乙醇制备1,2-二溴乙烷的两个化学反应方程式:
①
②
(2)装置b可以充当安全瓶,防止倒吸,例如:若装置a、b上方气体压强减小,则装置b中的现象为
(3)容器c中NaOH溶液的作用是:
(4)在做此实验时,应使a装置中的液体温度迅速升高到所需温度,请用化学方程式表示其原因
您最近一年使用:0次



