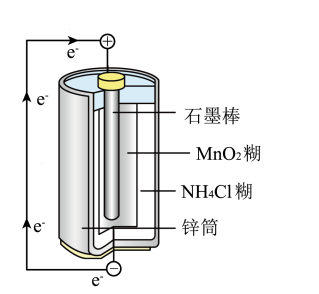
化学反应同时伴随着能量变化,是人类获取能量的重要途径。以下是常见的化学反应。
a.镁与盐酸反应;b.氢氧化钠与盐酸反应;c.盐酸与碳酸氢钠反应;d.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
(1)反应d的化学方程式是___________ 。
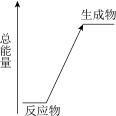
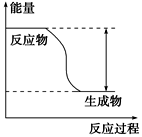
(2)以上化学反应中能用下图表示其能量变化的是___________ (填字母),此类反应中有能量变化的原因是:断开反应物的化学键吸收的总能量___________ (填“>”或“<”)形成生成物的化学键释放的总能量。
①将下图原电池装置补充完整。___________ ___________ 。
③正极的电极反应式是___________ 。
a.镁与盐酸反应;b.氢氧化钠与盐酸反应;c.盐酸与碳酸氢钠反应;d.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
(1)反应d的化学方程式是
(2)以上化学反应中能用下图表示其能量变化的是
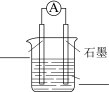
①将下图原电池装置补充完整。
③正极的电极反应式是
更新时间:2024-05-04 17:29:08
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】在下列事实中,各是什么因素影响了化学反应速率。
(1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:____ ;
(2)黄铁矿煅烧时要粉碎成矿粒:________ ;
(3)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体 :____ ;
(4)同样大小的石灰石分别与0.1 mol·L-1盐酸和1 mol·L-1盐酸反应,速率不同:__________ 。
(5)夏天食品容易变质,而冬天不易发生该现象:_______________ 。
(6)从能量的角度看,断开化学键要______ 能量(填吸收或放出,下同),形成化学键要_____ 能量。当反应物的总能量高于生成物时,该反应为_______ 反应(填吸热或放热,下同);当反应物的总能量低于生成物时,该反应为__________ 反应。
(7)由铜、锌和稀硫酸组成的原电池中,正极是_______ (填名称),发生_______ 反应;负极是_______ (填名称),发生________ 反应,总反应的化学方程式是______________________ 。
(1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:
(2)黄铁矿煅烧时要粉碎成矿粒:
(3)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体 :
(4)同样大小的石灰石分别与0.1 mol·L-1盐酸和1 mol·L-1盐酸反应,速率不同:
(5)夏天食品容易变质,而冬天不易发生该现象:
(6)从能量的角度看,断开化学键要
(7)由铜、锌和稀硫酸组成的原电池中,正极是
您最近一年使用:0次
【推荐2】研究化学反应中的能量变化有利于更好的开发和使用化学能源。
(1)已知 、CO、
、CO、 的燃烧热分别为285.8
的燃烧热分别为285.8 、283.0
、283.0 、890.3
、890.3 。
。
①相同条件下,等质量的 、CO、
、CO、 分别完全燃烧,放出热量最多的是
分别完全燃烧,放出热量最多的是_______ 。
②

_______  。
。
③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a_______ 途径b(填“>”、“<”或“=”)
途径a: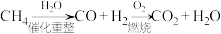
途径b: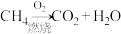
(2)已知白磷( )和
)和 的分子结构和部分化学键的键能分别如图、表所示:
的分子结构和部分化学键的键能分别如图、表所示:

①写出白磷与氧气反应生成 固体的热化学方程式:
固体的热化学方程式:_______ 。
②已知
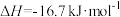 。比较稳定的是
。比较稳定的是_______ 。等质量的白磷、红磷分别完全燃烧,放出热量更多的是_______ 。
(1)已知
 、CO、
、CO、 的燃烧热分别为285.8
的燃烧热分别为285.8 、283.0
、283.0 、890.3
、890.3 。
。①相同条件下,等质量的
 、CO、
、CO、 分别完全燃烧,放出热量最多的是
分别完全燃烧,放出热量最多的是②


 。
。③等质量的甲烷按a、b两种途径完全转化,放出的热量:途径a
途径a:
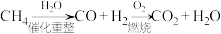
途径b:
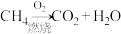
(2)已知白磷(
 )和
)和 的分子结构和部分化学键的键能分别如图、表所示:
的分子结构和部分化学键的键能分别如图、表所示:
| 化学键 | P-P | O=O | P-O |
键能( ) ) | a | b | c |
①写出白磷与氧气反应生成
 固体的热化学方程式:
固体的热化学方程式:②已知

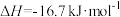 。比较稳定的是
。比较稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知:氢气和氧气的混合气体遇火星即发生爆炸,生成水;水在1 000 ℃以上持续加热分解为氢气和氧气;水电解生成氢气和氧气。试回答下列问题:
(1)氢气和氧气反应生成水的反应是__________ (填“放热”或“吸热”)反应,2mol氢气和1mol氧气的总能量__________ (填“大于”或“小于”) 2mol水的总能量,此反应中化学能转化为_________ 能。
(2)水在高温下分解的反应为______ (填“放热”或“吸热”)反应,反应中热能转化为__________ 能。电解水的过程是__________ 能转化为__________ 能的过程。
(3)下列正确的是:__________
①需要加热才能发生的反应一定是吸热反应;
②放热反应在常温下一定很容易发生;
③Na2O2中既含有离子键也含有非极性键
④有的吸热反应在常温下也能发生
⑤浓硫酸溶于水是放热反应
⑥含有离子键的化合物一定是离子化合物,含有共价键的一定是共价化合物。
(4)下列物质中:①Na2O2 ②He ③NaOH ④N2 ⑤MgCl2 ⑥NH3 ⑦H2O ⑧Cl2 ⑨NaF
是离子化合物的是_____________________ ,是共价化合物的是______________________ 。
(1)氢气和氧气反应生成水的反应是
(2)水在高温下分解的反应为
(3)下列正确的是:
①需要加热才能发生的反应一定是吸热反应;
②放热反应在常温下一定很容易发生;
③Na2O2中既含有离子键也含有非极性键
④有的吸热反应在常温下也能发生
⑤浓硫酸溶于水是放热反应
⑥含有离子键的化合物一定是离子化合物,含有共价键的一定是共价化合物。
(4)下列物质中:①Na2O2 ②He ③NaOH ④N2 ⑤MgCl2 ⑥NH3 ⑦H2O ⑧Cl2 ⑨NaF
是离子化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)下列过程中属于吸热反应的是___________ 。
①灼热的木炭中通入CO2②碘升华③石灰石受热分解④水蒸气液化⑤Mg+2HCl=MgCl2+H2↑⑥CH4+2O2 CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋
CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋
(2)汽车发动机工作时会引发N2和O2反应,生成NOX等污染大气,其中生成NO的能量变化如图所示,则图中三种分子最稳定的是___________ 。若反应生成2molNO气体(“吸收”或“放出”)___________ 热量。

(3)如果将燃料燃烧设计成燃料电池就可避免NOX的生成,某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①使用时,空气从___________ 口通入(填“A"或“B");当外电路通过0.4mol的电子时,消耗O2的体积___________ L(标况下)。
②假设使用的“燃料”是甲烷(CH4),a极的电极反应式为___________ 。
(1)下列过程中属于吸热反应的是
①灼热的木炭中通入CO2②碘升华③石灰石受热分解④水蒸气液化⑤Mg+2HCl=MgCl2+H2↑⑥CH4+2O2
 CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋
CO2+2H2O⑦HCl+NaHCO3=NaCl+H2O+CO2↑⑧Na2CO3·10H2O与NH4NO3反应制作冷敷袋(2)汽车发动机工作时会引发N2和O2反应,生成NOX等污染大气,其中生成NO的能量变化如图所示,则图中三种分子最稳定的是

(3)如果将燃料燃烧设计成燃料电池就可避免NOX的生成,某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲烷(CH4),a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在下列化合物中:H2O2 、Na2O、、I2 、、NaCl、、CO2、NH4Cl、Na2O2,用化学式回答下列问题:
①只由非金属组成的离子化合物是__________ ,
②只有极性共价键的共价化合物是_________ ,
③只含有非极性共价键的是______ ,
④既有离子键又有非极性键的化合物是______________ 。
(2)以下反应:①木炭与水制备水煤气 ②氯酸钾分解 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥ Ba(OH)2·8H2O与NH4Cl,属于放热反应_________ (填序号),写出反应⑥的化学方程式___________ 。
①只由非金属组成的离子化合物是
②只有极性共价键的共价化合物是
③只含有非极性共价键的是
④既有离子键又有非极性键的化合物是
(2)以下反应:①木炭与水制备水煤气 ②氯酸钾分解 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥ Ba(OH)2·8H2O与NH4Cl,属于放热反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】
(1)甲醇是一种重要的化工产品,可利用甲醇催化脱氢制备甲醛。甲醛与气态甲醇转化的能量关系如图所示。
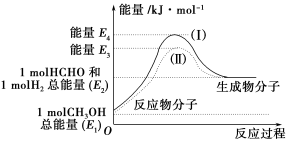
反应过程中的能量关系
①甲醇催化脱氢转化为甲醛的反应是________ (填“吸热”或“放热”)反应。
②过程Ⅰ与过程Ⅱ的反应热是否相同?____________ 原因是_______________ 。
③写出甲醇催化脱氢转化为甲醛的热化学反应方程式_________________________________ 。
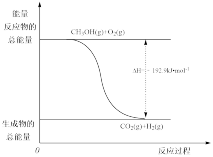
(2)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列说法正确的是________。
(1)甲醇是一种重要的化工产品,可利用甲醇催化脱氢制备甲醛。甲醛与气态甲醇转化的能量关系如图所示。

反应过程中的能量关系
①甲醇催化脱氢转化为甲醛的反应是
②过程Ⅰ与过程Ⅱ的反应热是否相同?
③写出甲醇催化脱氢转化为甲醛的热化学反应方程式
(2)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1下列说法正确的是________。

| A.CH3OH转变成H2的过程一定要吸收能量 |
| B.①反应中,反应物的总能量高于生成物的总能量 |
C.根据②推知反应:CH3OH(l)+ O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 |
| D.反应②的能量变化如图所示 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2的转换在生产、生活中具有重要的应用。
Ⅰ.CO2的低碳转型对抵御气候变化具有重要意义。
(1)海洋是地球上碳元素的最大“吸收池”。
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为____________ 。
②在海洋碳循环中,可通过下图所示的途径固碳。写出钙化作用的离子方程式:_____________ 。
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 2Na2CO3+C。放电时,在正极得电子的物质为
2Na2CO3+C。放电时,在正极得电子的物质为______ ;充电时,阳极的反应式为_____ 。
Ⅱ.环境中的有害物质常通过转化为CO2来降低污染。
(3)TiO2是一种性能优良的半导体光催化剂,能有效地将有机污染物转化为CO2等小分子物质。下图为在TiO2的催化下,O3降解CH3CHO的示意图,则该反应的化学方程式为____ 。
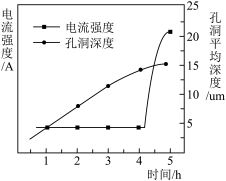
(4)用新型钛基纳米PbO2作电极可将苯、酚类等降解为CO2和H2O。该电极可通过下面过程制备:将钛基板用丙酮浸泡后再用水冲洗,在钛板上镀上一层铝膜。用它做阳极在草酸溶液中电解,一段时间后,铝被氧化为氧化铝并同时形成孔洞。再用Pb(NO3)2溶液处理得纳米PbO2,除去多余的氧化铝,获得钛基纳米PbO2电极。
①用丙酮浸泡的目的是______ 。
②电解时,电流强度和基板孔洞深度随时间变化如图所示,氧化的终点电流突然增加的原因是______ 。
Ⅰ.CO2的低碳转型对抵御气候变化具有重要意义。
(1)海洋是地球上碳元素的最大“吸收池”。
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为
②在海洋碳循环中,可通过下图所示的途径固碳。写出钙化作用的离子方程式:

(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2
 2Na2CO3+C。放电时,在正极得电子的物质为
2Na2CO3+C。放电时,在正极得电子的物质为Ⅱ.环境中的有害物质常通过转化为CO2来降低污染。
(3)TiO2是一种性能优良的半导体光催化剂,能有效地将有机污染物转化为CO2等小分子物质。下图为在TiO2的催化下,O3降解CH3CHO的示意图,则该反应的化学方程式为

(4)用新型钛基纳米PbO2作电极可将苯、酚类等降解为CO2和H2O。该电极可通过下面过程制备:将钛基板用丙酮浸泡后再用水冲洗,在钛板上镀上一层铝膜。用它做阳极在草酸溶液中电解,一段时间后,铝被氧化为氧化铝并同时形成孔洞。再用Pb(NO3)2溶液处理得纳米PbO2,除去多余的氧化铝,获得钛基纳米PbO2电极。
①用丙酮浸泡的目的是
②电解时,电流强度和基板孔洞深度随时间变化如图所示,氧化的终点电流突然增加的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(Ⅰ)将下列物质进行分类:
① 与
与 ②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
(1)互为同位素的是__________________ (填编号、下同);
(2)互为同素异形体的是___________________ ;
(3)互为同分异构体的是__________________ ;
(Ⅱ)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
(1)该反应为________ 反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是________ (填字母)。
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______ (填“正”或“负”)极。该极上发生的电极反应为_____________________ ,外电路中电子由______ 极(填“正”或“负”,下同)向______ 极移动。
①
 与
与 ②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石(1)互为同位素的是

(2)互为同素异形体的是
(3)互为同分异构体的是
(Ⅱ)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某课外小组分别用下图所示装置对原电池和电解原理进行实验探究。
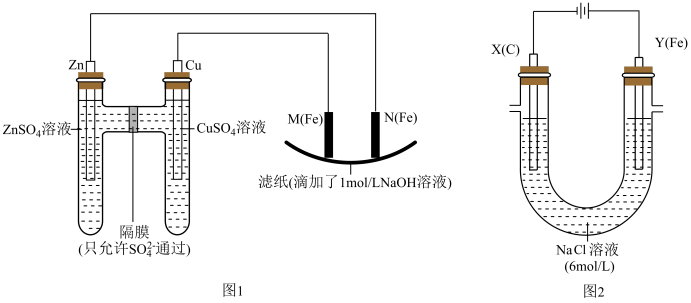
请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是_________ (填字母序号)。
(2)N极发生反应的电极反应式为____________________ 。
(3)实验过程中,SO42-_________ (填“从左向右”、“从右向左”或“不”)移动;
滤纸上能观察到的现象有___________________ 。
Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH___________ (填“增大” 、“减小”或“不变”)。电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O 和_______________ 。
(5)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________ g。

请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
| A.铝 | B.石墨 | C.银 | D.铂 |
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
滤纸上能观察到的现象有
Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH
(5)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题。
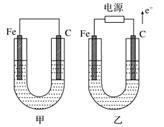
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的___________ 棒,乙池中的________ 棒。
②乙池中阳极的电极反应式是:_________________ 。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式:____________________ 。
②甲池中碳极的电极反应式是:______________ ,乙池中碳极的电极反应属于_______ (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙池中碳极附近,发现试纸变蓝,过一段时间后又发现蓝色褪去,这是因为过量的Cl2又将生成的I2氧化。若反应的Cl2和I2物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为:__________________ 。

(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的
②乙池中阳极的电极反应式是:
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式:
②甲池中碳极的电极反应式是:
③将湿润的淀粉KI试纸放在乙池中碳极附近,发现试纸变蓝,过一段时间后又发现蓝色褪去,这是因为过量的Cl2又将生成的I2氧化。若反应的Cl2和I2物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有反应:①Ba(OH)2∙8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O②Fe+H2SO4=FeSO4+H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是_______ (填序号,下同),能设计成原电池的是_______ 。
(2)Fe-Cu原电池的装置如图所示。
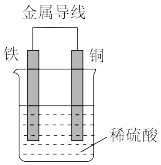
①铁作_______ (填“正极”或“负极”),溶液中H+向_______ (填“铁”或“铜”)电极方向移动。
②正极的现象是_______ ,负极的电极反应式为_______ 。
(1)两反应中属于吸热反应的是
(2)Fe-Cu原电池的装置如图所示。

①铁作
②正极的现象是
您最近一年使用:0次