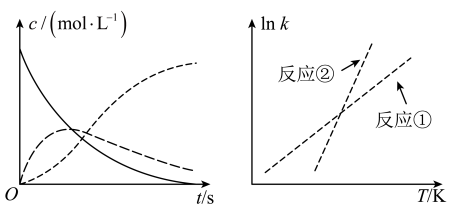
某实验小组用0.1 KMnO4溶液和0.1
KMnO4溶液和0.1 H2C2O4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是
H2C2O4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是
已知:
 KMnO4溶液和0.1
KMnO4溶液和0.1 H2C2O4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是
H2C2O4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。下列说法错误的是已知:

| 实验序号 | 温度 | KMnO4溶液 | H2C2O4溶液 |  | 溶液褪色所需的时间 |
| I | 10℃ | 2 | 5 | 10 | 10s |
| Ⅱ | 10℃ | 2 | 10 | a | 8s |
| Ⅲ | 10℃ | 2 | 7 | 8 |  s s |
| Ⅳ | 30℃ | 2 | 5 | 10 | 3s |
A.实验Ⅱ中 |
B.实验Ⅲ中 |
| C.对比实验I、Ⅳ可得:浓度保持不变时,升高温度,化学反应速率增大 |
| D.对比实验I、Ⅱ、Ⅲ可得:温度相同时,增大反应物浓度,化学反应速率增大 |
更新时间:2024-05-05 22:45:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案正确且能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别红棕色气体是 | 用湿润的淀粉-KI试纸检验 |
| B | 探究浓度对化学反应速率的影响 | 室温时取大小、形状和质量均相同的Fe片分别投入 的稀硝酸和 的稀硝酸和 的浓硝酸中 的浓硝酸中 |
| C | 比较C和 的非金属性强弱 的非金属性强弱 | 高温下,碳与 反应 反应 |
| D | 验证某无色溶液中含有 | 取样,向溶液中加入浓NaOH溶液并加热,并用湿润的红色石蕊试纸检验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某恒容密闭容器中进行反应:SO2(g)+NO2(g) SO3(g)+NO(g) ΔH=akJ·mol-1;某科研小组通过实验测出SO2的转化率(SO2、NO起始量一定)随条件P的变化情况如图所示,下列说法中正确的是
SO3(g)+NO(g) ΔH=akJ·mol-1;某科研小组通过实验测出SO2的转化率(SO2、NO起始量一定)随条件P的变化情况如图所示,下列说法中正确的是

 SO3(g)+NO(g) ΔH=akJ·mol-1;某科研小组通过实验测出SO2的转化率(SO2、NO起始量一定)随条件P的变化情况如图所示,下列说法中正确的是
SO3(g)+NO(g) ΔH=akJ·mol-1;某科研小组通过实验测出SO2的转化率(SO2、NO起始量一定)随条件P的变化情况如图所示,下列说法中正确的是
| A.10~15min内反应速率小于15~20min的反应速率,P为升高温度 |
| B.10~20min内反应速率小于20~40min的反应速率,P为减小SO3的浓度 |
| C.10~15min内反应速率大于40~50min的反应速率,P为减小压强 |
| D.该反应中,随着反应物浓度的减小,反应速率一直减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】现将2molA和1molB加入2L密闭容器中发生反应:2A(g)+B(g)  2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是
2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是
 2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是
2C(g),分别在Tl和T2时测得生成物C的物质的量随时间变化如图所示,下列说法正确的是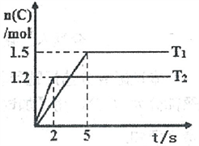
| A.T1<T2 |
| B.该反应在温度为T1时达到平衡时,容器中A与C的物质的量浓度相等 |
| C.温度为T2时,2s内B的平均速率为0.3mol·L-1·s-l |
| D.温度为T1时,达平衡时反应物A的转化率为60% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 溶液在不同温度下均可被过量
溶液在不同温度下均可被过量 氧化,当
氧化,当 完全消耗即有
完全消耗即有 析出,依据
析出,依据 析出所需时间可以求得
析出所需时间可以求得 的反应速率。将浓度均为0.020
的反应速率。将浓度均为0.020 的
的 溶液(含少量淀粉)10.0
溶液(含少量淀粉)10.0 、
、 (过量)酸性溶液40.0
(过量)酸性溶液40.0 混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是

 溶液在不同温度下均可被过量
溶液在不同温度下均可被过量 氧化,当
氧化,当 完全消耗即有
完全消耗即有 析出,依据
析出,依据 析出所需时间可以求得
析出所需时间可以求得 的反应速率。将浓度均为0.020
的反应速率。将浓度均为0.020 的
的 溶液(含少量淀粉)10.0
溶液(含少量淀粉)10.0 、
、 (过量)酸性溶液40.0
(过量)酸性溶液40.0 混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
| A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 |
B.图中N、P两点对应的 反应速率相等 反应速率相等 |
C.图中M点对应的 反应速率为 反应速率为 |
D.55℃时未观察到溶液变蓝,说明 没有完全消耗 没有完全消耗 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】CO2通入BaCl2溶液中并不产生沉淀,在下图右侧的Y形管中放置合适的药品,进行合理操作,在BaCl2溶液中可以看到白色沉淀.右侧Y形管中放的药品是( )


| A.Cu和浓硝酸 | B.CaO和浓氮水 |
| C.Na2SO3和较浓硫酸 | D.KMnO4溶液和浓盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室可利用硫酸厂废渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),聚铁的化学式可表示为[Fe2(OH)n(SO4)3-0.5n]m,主要工艺流程如下:

下列说法错误的是

下列说法错误的是
| A.炉渣中FeS与稀硫酸和氧气反应的离子方程式为:4FeS+3O2+12H+=4Fe3++4S↓+6H2O |
| B.气体M的成分是SO2,通入H2O2溶液得到硫酸,可循环使用 |
| C.向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸干即得绿矾 |
| D.溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】实验小组探究溶液酸碱性对含锰化合物和 氧化还原反应的影响。
氧化还原反应的影响。
资料: .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。
 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。
 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。
 .
. 为微溶物。
为微溶物。
已知:实验 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是
 氧化还原反应的影响。
氧化还原反应的影响。资料:
 .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。 .
. 为微溶物。
为微溶物。| 实验 | 序号 | 试剂 | 现象 |
| i.先加试剂a ii.再加试剂b
|  | a:10滴3mol/LH2SO4溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液紫色变浅至接近无色,静置一段时间后出现乳白色浑浊 |
 | a:10滴蒸馏水 b:20滴0.002mol/LNa2S2O3溶液 | 产生棕黑色沉淀 | |
 | a:x滴6mol/LNaOH溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液变为绿色,无沉淀生成;静置5min,绿色变浅,有棕黑色沉淀生成 |
 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是A.实验 中出现乳白色浑浊发生反应:S2O 中出现乳白色浑浊发生反应:S2O +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
B.实验 所得溶液中 所得溶液中 的检验:取少量溶液加入足量 的检验:取少量溶液加入足量 ,若有白色沉淀生成,则说明有 ,若有白色沉淀生成,则说明有 |
| C.x=10 |
D.实验 产生棕黑色沉淀可能原因是 产生棕黑色沉淀可能原因是 碱性减弱后不稳定生成 碱性减弱后不稳定生成 棕黑色沉淀 棕黑色沉淀 |
您最近一年使用:0次

 固体与稀盐酸反应制取
固体与稀盐酸反应制取 ,生成
,生成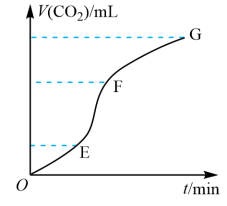
 最少
最少 Y(g);②Y(g)
Y(g);②Y(g)