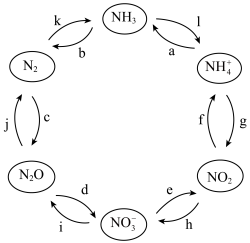
一定条件下,含氮元素的物质可发生如图所示的循环转化。
(1)图中属于“氮的固定”的反应是_______ (填字母);
(2)若“反应i”是在酸性条件下由 与Zn的作用实现,则该反应的离子方程式为
与Zn的作用实现,则该反应的离子方程式为_______ ;
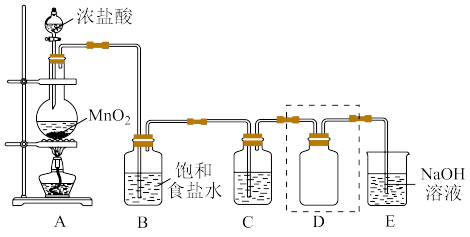
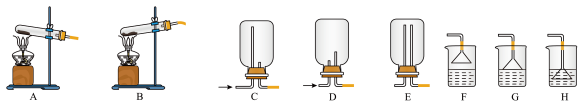
(3)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为_______ (填字母);_______ g;实验室还可以用其他方法快速制氨气,你认为合理的方案有:_______ (填字母);
A. 加热氯化铵固体 B.将浓氨水滴入氢氧化钠固体中
C. 加热浓氨水 D.将氢氧化钠固体加入浓氨水中
(4)实验室现有一白色未知固体,试通过实验证明其为铵盐:_______ 。
(1)图中属于“氮的固定”的反应是
(2)若“反应i”是在酸性条件下由
 与Zn的作用实现,则该反应的离子方程式为
与Zn的作用实现,则该反应的离子方程式为(3)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为
A. 加热氯化铵固体 B.将浓氨水滴入氢氧化钠固体中
C. 加热浓氨水 D.将氢氧化钠固体加入浓氨水中
(4)实验室现有一白色未知固体,试通过实验证明其为铵盐:
更新时间:2024/05/06 11:00:24
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
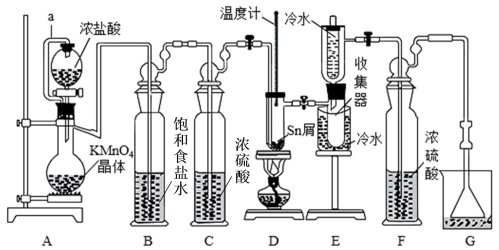
【推荐1】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点232℃,金属活动性比H好)与Cl2反应制备SnCl4,装置如图。
已知:①SnCl2、SnCl4有关物理性质:
② SnCl4极易水解生成SnO2·H2O
(1)导管a的作用是___________ ,装置A中发生反应的离子方程式为___________
(2)当观察到装置F液面上方___________ 时才开始点燃D处酒精灯,待锡熔化后,为防止产品带入过多的SnCl2,可使用的温度范围是___________
(3)若缺少装置B,则D处可能发生的反应为___________ (化学方程式),装置F的作用为___________
(4)装置G中发生反应的离子方程式为__________

已知:①SnCl2、SnCl4有关物理性质:
| 物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
| SnCl2 | 无色晶体 | 246 | 652 |
| SnCl4 | 无色晶体 | -33 | 114 |
(1)导管a的作用是
(2)当观察到装置F液面上方
(3)若缺少装置B,则D处可能发生的反应为
(4)装置G中发生反应的离子方程式为
您最近一年使用:0次
【推荐2】人类利用化学反应不仅可以创造新物质,还可以获取能量或实现不同形式能量之间的转化。回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。制作冷敷袋可以利用___________ (填标号)。
a.吸热的物理变化 b.放热的物理变化 c.吸热的化学变化 d.放热的化学变化
(2)氨气是重要的化工原料,工业合成氨反应: 。已知在25℃、
。已知在25℃、 时,拆开
时,拆开 键、
键、 键和
键和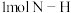 键所需能量分别为
键所需能量分别为 和
和 。
。
①根据上述数据判断,合成氨的反应是___________ 反应(填“吸热”或“放热”)。
②每消耗 ,反应放出或吸收的热量
,反应放出或吸收的热量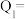
___________  。
。
③将 和
和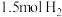 充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为
充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为 ,则
,则
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
(3)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 。补充完整下列化学方程式
。补充完整下列化学方程式_______ 。
___________ ___________
___________ ___________
___________ ___________+___________
___________+___________ ___________
___________
(4)从旧CPU中回收金部分流程如下。 、氯金酸、金元素的化合价为
、氯金酸、金元素的化合价为 )
)
若用 粉将溶液中的
粉将溶液中的 完全还原,则参加反应的
完全还原,则参加反应的 的物质的量是
的物质的量是___________ 。
(5)明矾 可用于净水。往明矾溶液中逐滴滴加
可用于净水。往明矾溶液中逐滴滴加 溶液,若使
溶液,若使 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为___________ 。
(6)彩漂剂的主要成分是双氧水,使用时会释放出一种无色无味的气体,使污垢活化,易于洗涤。但是不能长期存放,会降低彩漂效果,则发生的反应的还原产物为___________ (写化学式)。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。制作冷敷袋可以利用
a.吸热的物理变化 b.放热的物理变化 c.吸热的化学变化 d.放热的化学变化
(2)氨气是重要的化工原料,工业合成氨反应:
 。已知在25℃、
。已知在25℃、 时,拆开
时,拆开 键、
键、 键和
键和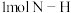 键所需能量分别为
键所需能量分别为 和
和 。
。①根据上述数据判断,合成氨的反应是
②每消耗
 ,反应放出或吸收的热量
,反应放出或吸收的热量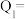
 。
。③将
 和
和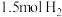 充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为
充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为 ,则
,则
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是(3)饮用水中的
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 。补充完整下列化学方程式
。补充完整下列化学方程式___________
 ___________
___________ ___________
___________ ___________+___________
___________+___________ ___________
___________
(4)从旧CPU中回收金部分流程如下。

 、氯金酸、金元素的化合价为
、氯金酸、金元素的化合价为 )
)若用
 粉将溶液中的
粉将溶液中的 完全还原,则参加反应的
完全还原,则参加反应的 的物质的量是
的物质的量是(5)明矾
 可用于净水。往明矾溶液中逐滴滴加
可用于净水。往明矾溶液中逐滴滴加 溶液,若使
溶液,若使 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为(6)彩漂剂的主要成分是双氧水,使用时会释放出一种无色无味的气体,使污垢活化,易于洗涤。但是不能长期存放,会降低彩漂效果,则发生的反应的还原产物为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】氮是生物体的重要组成元素,也是维持高等动植物生命活动的必需元素,研究氮的循环和转化对生产和生活有重要的价值。
Ⅰ.细菌可以促使铁、氮两种元素发生氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。___________ (填标号)。
a. b.
b. c.
c.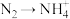 d.
d.
(2)硝化和反硝化过程均为氧化还原反应,反硝化过程中,含氮物质发生___________ (填“氧化”或“还原”)反应。
(3)写出氨态氮与亚硝态氮在氨氧化细菌的作用下转化为氮气的离子方程式___________ 。
(4)土壤中的铁循环可用于水体脱氮。土壤中的铁循环脱除水体中硝态氮和氨态氮的原理分别为:① ②
②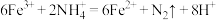 。若转移的电子数相等,则反应①②中生成
。若转移的电子数相等,则反应①②中生成 的物质的量之比为
的物质的量之比为___________ 。
Ⅱ.某实验小组用过量的氨气和氯气在常温下制备 。
。___________ 。
(6)利用装置B制取所需氯气,写出反应的离子方程式___________ 。
(7)为了使氨气和氯气在D中充分混合,各接口合理的连接顺序为___________ (提示:①氨气和氯气形成逆向流动更有利于两者充分混合。②用小写字母和箭头表示,箭头方向与气流方向一致)。
________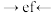 ___________。
___________。
Ⅰ.细菌可以促使铁、氮两种元素发生氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。

a.
 b.
b. c.
c.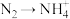 d.
d.
(2)硝化和反硝化过程均为氧化还原反应,反硝化过程中,含氮物质发生
(3)写出氨态氮与亚硝态氮在氨氧化细菌的作用下转化为氮气的离子方程式
(4)土壤中的铁循环可用于水体脱氮。土壤中的铁循环脱除水体中硝态氮和氨态氮的原理分别为:①
 ②
②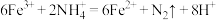 。若转移的电子数相等,则反应①②中生成
。若转移的电子数相等,则反应①②中生成 的物质的量之比为
的物质的量之比为Ⅱ.某实验小组用过量的氨气和氯气在常温下制备
 。
。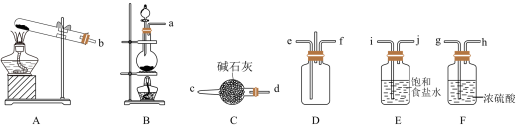
(6)利用装置B制取所需氯气,写出反应的离子方程式
(7)为了使氨气和氯气在D中充分混合,各接口合理的连接顺序为
________
 ___________。
___________。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】如图为制硝酸的流程图。
(1)工业生产中,物质A应选择_________ (填“空气”或“氧气”)。
(2)下列说法正确的是_________。
(3)以NO2为例,写出尾气处理装置中反应的化学方程式_________ 。
(4)写出足量氨气与光气(COCl2)反应生成尿素[CO(NH2)2]的化学方程式_________ 。
(5)向CuSO4溶液中依次加入氨水和乙醇可得[Cu(NH3)4]SO4⋅H2O晶体,设计实验证明该晶体中含有N元素(已知CuS不溶于氨水)_________ 。
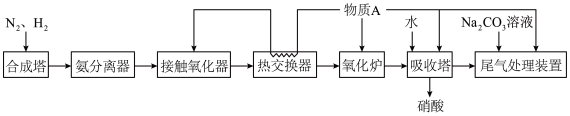
(1)工业生产中,物质A应选择
(2)下列说法正确的是_________。
| A.氨分离器得到的气体可循环使用 |
| B.热交换器可将接触氧化后的气体冷却并预热A |
| C.从氧化炉进入吸收塔的气体主要是NO |
| D.吸收塔中通入A可提高硝酸的产率 |
(3)以NO2为例,写出尾气处理装置中反应的化学方程式
(4)写出足量氨气与光气(COCl2)反应生成尿素[CO(NH2)2]的化学方程式
(5)向CuSO4溶液中依次加入氨水和乙醇可得[Cu(NH3)4]SO4⋅H2O晶体,设计实验证明该晶体中含有N元素(已知CuS不溶于氨水)
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】研究氮的循环和转化对生产、生活有重要的价值。
Ⅰ.氨是重要的化工原料。
某工厂用氨制硝酸的流程如图所示:
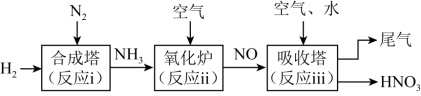
(1)上述转化中,属于氮的固定的是______ (填“i”“ii”或“iii”)。
(2)“合成塔”中发生反应N2+3H2 2NH3。已知断裂1mol相应化学键需要的能量如表:
2NH3。已知断裂1mol相应化学键需要的能量如表:
若反应生成2molNH3,可______ (填“吸收”或“放出”)热量______ kJ。
(3)写出“吸收塔”中反应的化学方程式2NO+O2=2NO2、______ 。
(4)“吸收塔”排出的尾气中含有NO、NO2等氮氧化物,可用NH3将其催化还原成不污染环境的气体,写出NH3与NO2反应的化学方程式______ 。
Ⅱ.含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如图:
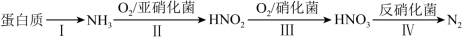
(5)过程Ⅲ发生反应的化学方程式为______ 。
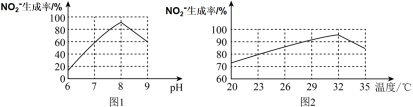
(6)根据图1和图2,判断使用亚硝化菌的最佳条件为______ 。
Ⅰ.氨是重要的化工原料。
某工厂用氨制硝酸的流程如图所示:

(1)上述转化中,属于氮的固定的是
(2)“合成塔”中发生反应N2+3H2
 2NH3。已知断裂1mol相应化学键需要的能量如表:
2NH3。已知断裂1mol相应化学键需要的能量如表:| 化学键 | H-H | N-H | N≡N |
| 能量 | 436kJ | 391kJ | 946kJ |
(3)写出“吸收塔”中反应的化学方程式2NO+O2=2NO2、
(4)“吸收塔”排出的尾气中含有NO、NO2等氮氧化物,可用NH3将其催化还原成不污染环境的气体,写出NH3与NO2反应的化学方程式
Ⅱ.含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如图:
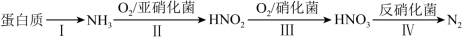
(5)过程Ⅲ发生反应的化学方程式为
(6)根据图1和图2,判断使用亚硝化菌的最佳条件为

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2.某同学在实验室中对NH3与NO2反应进行探究。回答下列问题:
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

(1)实验室制备氨气的化学方程式为___________ ;
(2)氨气的电子式:___________
(3)B中圆底烧瓶收集氨气时,请你选择氨气的进气口___________ (填“a”或“b”)。
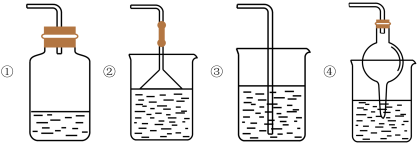
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)
(5)若观察到装置B中的烧瓶内产生了红色喷泉,你认为引发喷泉的操作应是___________ 。
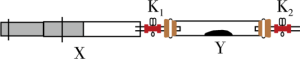
(6)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管中反应的化学方程式___________ 。
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

(1)实验室制备氨气的化学方程式为
(2)氨气的电子式:
(3)B中圆底烧瓶收集氨气时,请你选择氨气的进气口
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

(5)若观察到装置B中的烧瓶内产生了红色喷泉,你认为引发喷泉的操作应是
(6)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管中反应的化学方程式

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行探究。回答下列问题:
I.氨气的制备
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
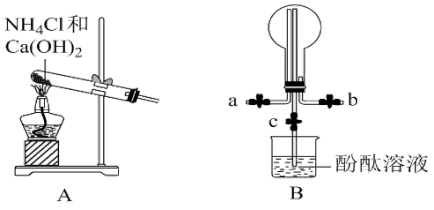
(1)实验室制备氨气的化学方程式为____ ;B中圆底烧瓶收集氨气时,请你选择氨气的进气口____ (填“a”或“b”)。
(2)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是____ (填序号)。
①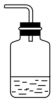 ②
②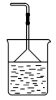 ③
③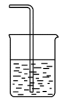 ④
④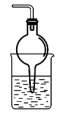
II.氨气与二氧化氮的反应
(3)铜和浓硝酸产生NO2的化学方程式是_____ 。
(4)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入(3)中产生的NO2(两端用夹子K1、K2夹好)。
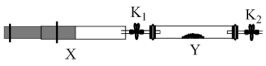
在一定温度下按图示装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管中实验现象是_____ ;反应的化学方程式_____ 。
I.氨气的制备
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

(1)实验室制备氨气的化学方程式为
(2)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是
①
 ②
② ③
③ ④
④
II.氨气与二氧化氮的反应
(3)铜和浓硝酸产生NO2的化学方程式是
(4)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入(3)中产生的NO2(两端用夹子K1、K2夹好)。

在一定温度下按图示装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管中实验现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某实验小组在实验室制备氨气并进行氨的催化氧化实验,装置如图所示。
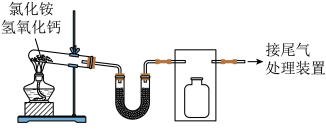
(1)U形管中的干燥剂可用_______ ,收集氨气应选择安装_______ (填“a”或“b”)。
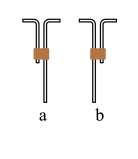
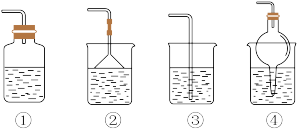
(2)为防止环境污染,图装置(盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。
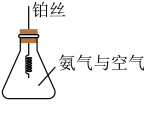
(3)如图所示,锥形瓶中是氨气与空气的混合气体,将灼热的铂丝插入锥形瓶中,观察到的现象为出现红棕色和白烟。写出氨催化氧化的化学方程式_______ 。
(4)氨气常用于检验化工生产中氯气是否泄漏,因为氯气有少量泄漏时用氨气检验会有白烟生成,同时生成一种对大气无污染的产物,试写出该反应的化学方程式_______ 。

(1)U形管中的干燥剂可用

(2)为防止环境污染,图装置(盛放的液体均为水)可用于吸收多余氨气的是

(3)如图所示,锥形瓶中是氨气与空气的混合气体,将灼热的铂丝插入锥形瓶中,观察到的现象为出现红棕色和白烟。写出氨催化氧化的化学方程式

(4)氨气常用于检验化工生产中氯气是否泄漏,因为氯气有少量泄漏时用氨气检验会有白烟生成,同时生成一种对大气无污染的产物,试写出该反应的化学方程式
您最近一年使用:0次

 。
。