黑火药的爆炸反应为S+2KNO3+3C=K2S+N2↑+3CO2↑。下列说法正确的是
| A.原子半径:r(K)>r(O)>r(C) |
| B.氢化物的沸点:CH4<H2O<H2S |
| C.元素最高价氧化物的水化物的酸性:N>C |
| D.硫单质、碳单质、干冰均为共价晶体 |
更新时间:2024-05-07 15:13:44
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列性质的比较,不能用元素周期律解释的是
| A.酸性:HClO4>H2SO4>H2SiO3 | B.熔点:SiO2>CO2 |
| C.热稳定性:H2O>H2S>SiH4 | D.非金属性:F>O>N |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如图所示。下列判断不合理的是
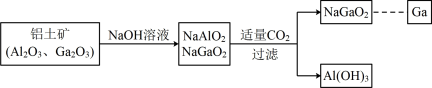

A.酸性: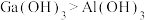 |
B.向 溶液中逐滴加入足量氨水,先生成沉淀,后沉淀溶解 溶液中逐滴加入足量氨水,先生成沉淀,后沉淀溶解 |
C.金属镓可与NaOH溶液反应生成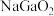 和氢气 和氢气 |
D. 可与盐酸反应生成 可与盐酸反应生成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】短周期元素X、Y、Z、W的原子序数依次增大,X2-与Y+具有相同的电子层结构,W的最高价氧化物对应的水化物是已知的最强无机含氧酸,X、W原子的核外电子数之和与Y、Z原子的核外电子数之和相等。下列叙述正确的是
| A.简单离子半径的大小顺序:W>Y>X |
| B.元素Z的简单气态氢化物的热稳定性比W的弱 |
| C.元素X和Y不可能形成含共价键的化合物 |
| D.工业上通过电解YW的水溶液制取Y单质 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列叙述中正确的是
①同周期元素中,ⅦA族元素的原子半径最大
②ⅥA族元素的原子,其半径越大,越容易得到电子
③同一周期中,碱金属元素的第一电离能最小
④当各轨道处于全满、半满、全空时原子较稳定
①同周期元素中,ⅦA族元素的原子半径最大
②ⅥA族元素的原子,其半径越大,越容易得到电子
③同一周期中,碱金属元素的第一电离能最小
④当各轨道处于全满、半满、全空时原子较稳定
| A.①② | B.②④ | C.①③ | D.③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】周期表中元素的位置、原子结构与元素的性质之间关系密切。下列说法正确的是
| A.Be(OH)2既可以和强酸反应,又可以和强碱反应 |
| B.①硫酸比次氯酸稳定;②S2-易被氯气氧化,均能说明氯元素的非金属性比硫元素强 |
| C.中学教材所附周期表中第15列元素的最高价氧化物对应水化物的化学式均为H3RO4 |
| D.HF的沸点比HCl 高,是因为H-F键比H-Cl键强 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】向 溶液中通入
溶液中通入 至过量,先生成蓝色沉淀,后沉淀溶解得到深蓝色的
至过量,先生成蓝色沉淀,后沉淀溶解得到深蓝色的 溶液。下列说法正确的是
溶液。下列说法正确的是
 溶液中通入
溶液中通入 至过量,先生成蓝色沉淀,后沉淀溶解得到深蓝色的
至过量,先生成蓝色沉淀,后沉淀溶解得到深蓝色的 溶液。下列说法正确的是
溶液。下列说法正确的是A.氢键的存在导致 热稳定性较强 热稳定性较强 | B.硫离子 的结构示意图: 的结构示意图: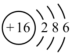 |
C.离子半径大小: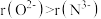 | D. 的空间结构为正四面体 的空间结构为正四面体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】正硼酸( )是一种层状结构白色晶体,层内的
)是一种层状结构白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的是
分子通过氢键相连(如图)。下列有关说法正确的是
 )是一种层状结构白色晶体,层内的
)是一种层状结构白色晶体,层内的 分子通过氢键相连(如图)。下列有关说法正确的是
分子通过氢键相连(如图)。下列有关说法正确的是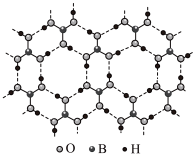
| A.正硼酸晶体属于共价晶体 | B. 分子的稳定性与氢键有关 分子的稳定性与氢键有关 |
C. 分子中B原子采用 分子中B原子采用 杂化 杂化 | D.含1mol 的晶体中有6mol氢键 的晶体中有6mol氢键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列晶体变成液态的过程中破坏的作用力与其他不同的是
| A.食盐 | B.冰醋酸 | C.蔗糖 | D.干冰 |
您最近一年使用:0次

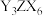 。下列说法正确的是
。下列说法正确的是



