Ⅰ.完成下列问题
(1) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
(2)实验室制备氢氧化铁胶体的化学方程式为___________ 。
Ⅱ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为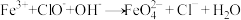
(3)高铁酸钠中铁元素化合价为___________ 。
(4)在该反应中被氧化的离子是(写离子符号,下同)___________ ;被还原的离子是___________ 。
(5)配平:_______
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ 。(依次写出计量数)
。(依次写出计量数)
Ⅲ.配制100mL1.00mol/LNaCl溶液,操作步骤如下:
(6)①溶解:将___________ g氯化钠放入小烧杯中,加适量蒸馏水溶解。
②转移:把①所得溶液小心转入100mL容量瓶中。
③洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
④定容:继续向容量瓶中加蒸馏水至液面距刻度线___________ 处,改用___________ 小心滴加蒸馏水至溶液凹液面底部与刻度线相切,
⑤摇匀:将容量瓶塞塞紧,充分摇匀。
(7)在溶解过程中若有少量液体溅出,配制所得的溶液浓度将___________ (填“偏高”、“偏低”或“无影响”)。
(1)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(2)实验室制备氢氧化铁胶体的化学方程式为
Ⅱ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠的一种方法对应的离子方程式为
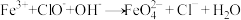
(3)高铁酸钠中铁元素化合价为
(4)在该反应中被氧化的离子是(写离子符号,下同)
(5)配平:
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ 。(依次写出计量数)
。(依次写出计量数) Ⅲ.配制100mL1.00mol/LNaCl溶液,操作步骤如下:
(6)①溶解:将
②转移:把①所得溶液小心转入100mL容量瓶中。
③洗涤:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
④定容:继续向容量瓶中加蒸馏水至液面距刻度线
⑤摇匀:将容量瓶塞塞紧,充分摇匀。
(7)在溶解过程中若有少量液体溅出,配制所得的溶液浓度将
更新时间:2024-05-09 08:17:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示表示钙及其化合物之间的转化关系:
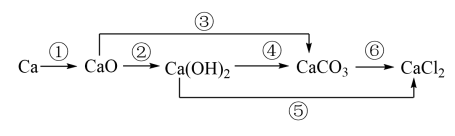
(1)Ca(OH)2是否属于电解质_______ (填“是”或者“否”)。
(2)写出Ca(OH)2在水溶液中的电离方程式_________ 。
(3)写出下列序号对应转化的化学方程式:
④:________ ;
⑥:_______ 。

(1)Ca(OH)2是否属于电解质
(2)写出Ca(OH)2在水溶液中的电离方程式
(3)写出下列序号对应转化的化学方程式:
④:
⑥:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】砷及其化合物用途非常广泛。回答下列问题:
(1)已知:砷(As)与磷位于同一主族相邻位置。画出砷的原子结构示意图:___________ 。
(2) (亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出
(亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出 。第一步电离方程式为
。第一步电离方程式为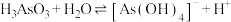 ,第二步的电离方程式为
,第二步的电离方程式为___________ 。
(3)古代《本草衍义》提纯砒霜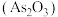 作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是
作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是___________ 。砷黄铁矿(FeAsS)制烧可生成砒霜和红棕色固体,该反应的化学方程式为___________ 。
(4)处理含砷废水的方法很多,在含高浓度 的酸性溶液中加入
的酸性溶液中加入 可将
可将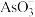 转化为
转化为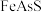 而脱除,该脱除砷的离子方程式为
而脱除,该脱除砷的离子方程式为___________ 。
(1)已知:砷(As)与磷位于同一主族相邻位置。画出砷的原子结构示意图:
(2)
 (亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出
(亚砷酸)是三元弱酸,第一步和第二步电离是通过和水中的氢氧根结合实现的,第三步则直接电离出 。第一步电离方程式为
。第一步电离方程式为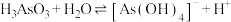 ,第二步的电离方程式为
,第二步的电离方程式为(3)古代《本草衍义》提纯砒霜
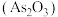 作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是
作如下叙述:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器,遂凝结,累然下垂如乳尖……”,该提纯用的基本操作是(4)处理含砷废水的方法很多,在含高浓度
 的酸性溶液中加入
的酸性溶液中加入 可将
可将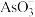 转化为
转化为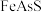 而脱除,该脱除砷的离子方程式为
而脱除,该脱除砷的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钙及其化合物间有如下相互转化关系,请按要求写出指定反应的化学方程式并完成填空。

(1)反应②___________
(2)反应⑤___________
(3)反应⑥___________
(4)在反应①~⑥中,属于化合反应的是___________ (填序号,下同),属于氧化还原反应的是___________
(5)写出下列物质的电离方程式
①NaHSO4在水溶液中的电离程式___________
②NaHSO4在熔融状态下的电离方程式___________
③NaHCO3在水溶液中的电离方程式___________

(1)反应②
(2)反应⑤
(3)反应⑥
(4)在反应①~⑥中,属于化合反应的是
(5)写出下列物质的电离方程式
①NaHSO4在水溶液中的电离程式
②NaHSO4在熔融状态下的电离方程式
③NaHCO3在水溶液中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角。
(1)在氧化还原反应中,氧化剂_______ 电子,发生_______ 反应。
(2)理论上,处于最低价态的元素通常具有_______ 性,在氧化还原反应中常作_______ 剂。
(3)下列物质在氧化还原反应中,常作还原剂的有_______ ;常作氧化剂的有_______ (均填序号)。
①KMnO4②铝③氯水④FeCl3⑤一氧化碳⑥Na2S
(4)钠与水反应的化学方程式为_______ 。铁与水反应的化学方程式为_______ ;在该反应中,若消耗3molFe,则转移的电子为_______ mol。事实证明,钠的还原性比铁的还原性(填“强”或“弱”)_______ 。
(1)在氧化还原反应中,氧化剂
(2)理论上,处于最低价态的元素通常具有
(3)下列物质在氧化还原反应中,常作还原剂的有
①KMnO4②铝③氯水④FeCl3⑤一氧化碳⑥Na2S
(4)钠与水反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。针对以下A—D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→NaCl+H2O2
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)上述反应中,H2O2仅体现氧化性的反应是____ (填字母,下同),H2O2仅体现还原性的反应是____ ,H2O2既体现氧化性又体现还原性的反应是____ 。
(2)请将D反应配平,并用单线桥标出D反应中电子转移的方向合数目:____ ,反应中氧化剂是____ ,被氧化的元素是____ ,氧化产物是____ 。
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO 、H2O、Fe2+、H+,则反应的离子方程式为
、H2O、Fe2+、H+,则反应的离子方程式为____ 。
A.Na2O2+HCl→NaCl+H2O2
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)上述反应中,H2O2仅体现氧化性的反应是
(2)请将D反应配平,并用单线桥标出D反应中电子转移的方向合数目:
(3)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO
 、H2O、Fe2+、H+,则反应的离子方程式为
、H2O、Fe2+、H+,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂,等物质的量的上述物质消毒效率(消毒效率是指单位物质的量消毒剂的得电子数目)最高的是__ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为__ ,H2O2被称为“绿色氧化剂”的理由是___ 。
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平),在该反应中,当有1molClO2生成时转移的电子个数约为___ 。
(4)“84”消毒液(主要成分是NaClO))和洁厕剂(主要成分是浓盐酸)不能混用,原因是__ (用化学方程式表示):利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:__ 。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂,等物质的量的上述物质消毒效率(消毒效率是指单位物质的量消毒剂的得电子数目)最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平),在该反应中,当有1molClO2生成时转移的电子个数约为
(4)“84”消毒液(主要成分是NaClO))和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
【推荐1】查资料得:HNO2是一种弱酸且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:________ 。
(4)Fe与过量稀硫酸反应可制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________ (填序号)。
A.Cl2 B.Fe C.H2O2 D.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
( ) FeSO4+( ) K2O2→( ) K2FeO4+( ) K2O+( ) K2SO4+( ) O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是___________________ 。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe C.H2O2 D.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂是__ 。(填化学式)
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:___ 。
②每生成2molFeO42-转移_______ mol电子,若反应过程中转移了0.5mol电子,则还原产物的物质的量为___ mol。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成2molFeO42-转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4,Fe为+6价)是一种高效水处理剂,具有氧化能力强、安全性好等优点。已知K2FeO4是紫色固体,可溶于水、微溶于浓KOH溶液,在0℃~5℃强碱性溶液中比较稳定。
(1)实验室可通过如下反应制取K2FeO4溶液:Fe(NO3)3+KClO+KOH——K2FeO4+KCl+KNO3+H2O(未配平)。
①配平反应的方程式,并用单线桥表示电子转移的方向和数目_______ 。
②反应结束后,为从溶液中获得K2FeO4晶体,可采取的实验操作是_______ 。
(2)将高铁酸钾固体投入水中时,会有Fe(OH)3胶体生成,同时有气泡产生。
①生成的气体是_______ (填化学式),每生成11.2L(标准状况下)该气体,转移电子_______ mol。
②检验有Fe(OH)3胶体生成的方法是_______ 。
(1)实验室可通过如下反应制取K2FeO4溶液:Fe(NO3)3+KClO+KOH——K2FeO4+KCl+KNO3+H2O(未配平)。
①配平反应的方程式,并用单线桥表示电子转移的方向和数目
②反应结束后,为从溶液中获得K2FeO4晶体,可采取的实验操作是
(2)将高铁酸钾固体投入水中时,会有Fe(OH)3胶体生成,同时有气泡产生。
①生成的气体是
②检验有Fe(OH)3胶体生成的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)明胶溶于水所形成的分散系和K2SO4溶液共同具备的性质是___ 。
a.都不稳定,密封放置沉淀 b.两者均有丁达尔现象 c.分散质粒子可通过滤纸
(2)现需配制0.50mol·L-1 K2SO4溶液480mL。
①配制溶液时必需的仪器有:托盘天平(精确到0.1g)、药匙、烧杯、玻璃棒、___ 、___ 、以及等质量的几片滤纸。
②配制该溶液需称取K2SO4晶体的质量为___ 。
③下列关于容量瓶的使用方法中,正确的是___ 。
A.容量瓶可长期存放溶液 B.在容量瓶中直接溶解固体
C.溶液未经冷却即注入容量瓶中 D.向容量瓶中转移溶液要用玻璃棒引流
④下列操作会使所配溶液浓度偏低的是___ 。
A.转移溶液时有液体溅出
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线
D.烧杯和玻璃棒未洗涤
(3)现有下列十种物质:①HCl;②NaHCO3;③K2SO4溶液;④CO2;⑤蔗糖晶体;⑥Ca(OH)2;⑦氢氧化铁胶体;⑧NH3·H2O;⑨空气;⑩Al2(SO4)3
(a)上述物质中属于电解质的有___ ,非电解质的有___ (填序号)。
(b)CO2属于酸性氧化物,SiO2也属于酸性氧化物,请写出SiO2和CaO反应的化学方程式:___ 。
(c)②在水溶液中的电离方程式为___ 。
(d)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式:___ ;如果病人同时患胃溃疡,为防胃壁穿孔,不宜服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:___ 。
(e)若⑦中混有少量的③,提纯的方法是:____ 。
A.蒸馏(分馏) B.萃取 C.渗析 D.分液
(1)明胶溶于水所形成的分散系和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀 b.两者均有丁达尔现象 c.分散质粒子可通过滤纸
(2)现需配制0.50mol·L-1 K2SO4溶液480mL。
①配制溶液时必需的仪器有:托盘天平(精确到0.1g)、药匙、烧杯、玻璃棒、
②配制该溶液需称取K2SO4晶体的质量为
③下列关于容量瓶的使用方法中,正确的是
A.容量瓶可长期存放溶液 B.在容量瓶中直接溶解固体
C.溶液未经冷却即注入容量瓶中 D.向容量瓶中转移溶液要用玻璃棒引流
④下列操作会使所配溶液浓度偏低的是
A.转移溶液时有液体溅出
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线
D.烧杯和玻璃棒未洗涤
(3)现有下列十种物质:①HCl;②NaHCO3;③K2SO4溶液;④CO2;⑤蔗糖晶体;⑥Ca(OH)2;⑦氢氧化铁胶体;⑧NH3·H2O;⑨空气;⑩Al2(SO4)3
(a)上述物质中属于电解质的有
(b)CO2属于酸性氧化物,SiO2也属于酸性氧化物,请写出SiO2和CaO反应的化学方程式:
(c)②在水溶液中的电离方程式为
(d)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式:
(e)若⑦中混有少量的③,提纯的方法是:
A.蒸馏(分馏) B.萃取 C.渗析 D.分液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】实验是学习化学的基础.某实验小组欲用 固体配制
固体配制 的
的 溶液.回答下列问题:
溶液.回答下列问题:
(1)本实验用到的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要___________________ .
(2)配制溶液时,一般可以分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却.正确的操作顺序为_________________ .
(3)某同学欲称量 的质量,他采用托盘天平称量,应称取
的质量,他采用托盘天平称量,应称取____________ 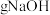 .
.
(4)某实验小组欲用 固体配制
固体配制 的
的 溶液.在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是
溶液.在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是____________ (填序号)
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面 ③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线 ⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
(5)取配制好的上述溶液 ,与足量的铝反应,可产生标准状况下氢气
,与足量的铝反应,可产生标准状况下氢气____________ L.(已知:氢氧化钠和铝会发生如下反应: )
)
 固体配制
固体配制 的
的 溶液.回答下列问题:
溶液.回答下列问题:(1)本实验用到的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
(2)配制溶液时,一般可以分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧冷却.正确的操作顺序为
(3)某同学欲称量
 的质量,他采用托盘天平称量,应称取
的质量,他采用托盘天平称量,应称取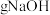 .
.(4)某实验小组欲用
 固体配制
固体配制 的
的 溶液.在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是
溶液.在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏高的是①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面 ③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线 ⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
(5)取配制好的上述溶液
 ,与足量的铝反应,可产生标准状况下氢气
,与足量的铝反应,可产生标准状况下氢气 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碳酸锂是生产锂离子电池的重要原料。
(1)碳酸锂制取锂的反应原理为:①Li2CO3 Li2O+CO2;②Li2O+C
Li2O+CO2;②Li2O+C CO+2Li。锂原子的电子排布式为
CO+2Li。锂原子的电子排布式为_____ ;CO2 的结构式为_____ ;反应②中涉及的化学键类型有_____ 。
(2)氢负离子(H﹣)与锂离子具有相同电子层结构,试比较两者微粒半径的大小,并用原子结构理论加以解释_____
(3)电池级碳酸锂对纯度要求很高,实验室测定Li2CO3产品纯度的方法如下:称取1.000g样品,溶于2.000 mol/L 10.00 mL 的硫酸,煮沸、冷却,加水定容至 100mL.取定容后的溶液 10.00 mL,加入 2 滴酚酞试液,用 0.100 mol/L标准NaOH溶液滴定过量的硫酸,消耗NaOH溶液13.00 mL。
①定容所需要玻璃仪器有烧杯、胶头滴管、_____ 和_____ 。
②滴定终点的判断依据为_____ 。
③样品的纯度为_____ 。
(1)碳酸锂制取锂的反应原理为:①Li2CO3
 Li2O+CO2;②Li2O+C
Li2O+CO2;②Li2O+C CO+2Li。锂原子的电子排布式为
CO+2Li。锂原子的电子排布式为(2)氢负离子(H﹣)与锂离子具有相同电子层结构,试比较两者微粒半径的大小,并用原子结构理论加以解释
(3)电池级碳酸锂对纯度要求很高,实验室测定Li2CO3产品纯度的方法如下:称取1.000g样品,溶于2.000 mol/L 10.00 mL 的硫酸,煮沸、冷却,加水定容至 100mL.取定容后的溶液 10.00 mL,加入 2 滴酚酞试液,用 0.100 mol/L标准NaOH溶液滴定过量的硫酸,消耗NaOH溶液13.00 mL。
①定容所需要玻璃仪器有烧杯、胶头滴管、
②滴定终点的判断依据为
③样品的纯度为
您最近一年使用:0次



