6.5g锌粉与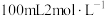 的稀硫酸反应,下列措施能加快反应速率且不改变生成的
的稀硫酸反应,下列措施能加快反应速率且不改变生成的 的物质的量的是
的物质的量的是
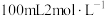 的稀硫酸反应,下列措施能加快反应速率且不改变生成的
的稀硫酸反应,下列措施能加快反应速率且不改变生成的 的物质的量的是
的物质的量的是A.改用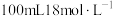 的浓硫酸参与反应 的浓硫酸参与反应 |
B.反应过程中加入适量 固体 固体 |
| C.适当升高反应体系温度 |
D.改用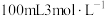 的盐酸参与反应 的盐酸参与反应 |
更新时间:2024-05-09 19:25:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述中正确的是
①在1 mol/L氨水中,NH3·H2O、NH 、NH3的物质的量浓度之和为1 mol/L
、NH3的物质的量浓度之和为1 mol/L
②水泥、玻璃、水晶饰物都是硅酸盐制品
③向铜与浓硫酸反应后的溶液中加水稀释,溶液变蓝,则证明产物有Cu2+生成
④ SiO2是酸性氧化物,它不能与任何酸发生反应
⑤铵盐受热分解一定都会产生氨气
⑥可用淀粉-KI试纸鉴别红棕色的Br2蒸气和NO2气体
⑦氨水和液氨不同,氨水是由多种粒子组成的,液氨的组成中只有氨分子
①在1 mol/L氨水中,NH3·H2O、NH
 、NH3的物质的量浓度之和为1 mol/L
、NH3的物质的量浓度之和为1 mol/L②水泥、玻璃、水晶饰物都是硅酸盐制品
③向铜与浓硫酸反应后的溶液中加水稀释,溶液变蓝,则证明产物有Cu2+生成
④ SiO2是酸性氧化物,它不能与任何酸发生反应
⑤铵盐受热分解一定都会产生氨气
⑥可用淀粉-KI试纸鉴别红棕色的Br2蒸气和NO2气体
⑦氨水和液氨不同,氨水是由多种粒子组成的,液氨的组成中只有氨分子
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述不合理的是
A. 可用作葡萄酒的防腐剂 可用作葡萄酒的防腐剂 |
B.浓硫酸与木炭反应的化学方程式为 ,在此反应中,浓硫酸既表现了强氧化性又表现了酸性 ,在此反应中,浓硫酸既表现了强氧化性又表现了酸性 |
| C.将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性 |
D.先将氨通入饱和食盐水,再通入 可生成碳酸氢钠沉淀 可生成碳酸氢钠沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】四个试管中都装有5mL0.1mol/LNa2SO3溶液,分别在不同温度下加入0.1mol/L硫酸和一定量水,最先出现浑浊的是
| A.20℃,4 mL硫酸,6 mL水 | B.20℃,5 mL硫酸,5 mL水 |
| C.30℃,5 mL硫酸,5 mL水 | D.30℃,4 mL硫酸,6 mL水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某同学为探究浓度对化学反应速率的影响,设计以下实验。
下列说法错误的是
| ① | ② | ③ | ④ | |
| 试剂a | 1mL0.01mol/L酸性高锰酸钾水溶液 | 1mL0.01mol/L酸性高锰酸钾水溶液 | 1mL0.01mol/L酸性高锰酸钾水溶液 | 1mL0.01mol/L酸性高锰酸钾水溶液 |
| 试剂b | 2mL0.1mol/LH2C2O4水溶液 | 2mL0.2mol/LH2C2O4水溶液 | 1mL0.2mol/LH2C2O4水溶液 | 1mL以浓盐酸为溶剂配制的0.2mol/LH2C2O4水溶液 |
| 褪色时间 | 690s | 677s | 600s |
| A.对比实验①、②可知,H2C2O4水溶液浓度增大,反应速率加快 |
| B.对比实验②、③可知,酸性高锰酸钾水溶液浓度增大,反应速率加快 |
| C.为验证H+浓度对反应速率的影响,设计实验④并与③对照 |
D.实验③的离子方程式为2 +6H++5H2C2O4=2Mn2++10CO2↑+8H2O +6H++5H2C2O4=2Mn2++10CO2↑+8H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在温度 和
和 时,分别将0.5 mol
时,分别将0.5 mol  和1.2 mol
和1.2 mol  充入体积为1 L的密闭容器中,发生反应:
充入体积为1 L的密闭容器中,发生反应: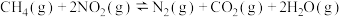 ,测得有关数据如表:
,测得有关数据如表:
下列说法正确的是
 和
和 时,分别将0.5 mol
时,分别将0.5 mol  和1.2 mol
和1.2 mol  充入体积为1 L的密闭容器中,发生反应:
充入体积为1 L的密闭容器中,发生反应: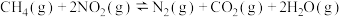 ,测得有关数据如表:
,测得有关数据如表:| 时间/min | 0 | 10 | 20 | 40 | 50 | |
 | 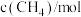 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
 | 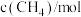 | 0.50 | 0.30 | 0.18 | a | 0.15 |
A.温度: |
B. 时0~10 min内 时0~10 min内 的平均反应速率为0.15 的平均反应速率为0.15  |
C.a=0.15,且该反应 |
D. 时保持其他条件不变,再充入0.5 mol 时保持其他条件不变,再充入0.5 mol  和1.2 mol 和1.2 mol  ,达新平衡时 ,达新平衡时 的浓度减小 的浓度减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在Mg和过量2 mol/L的稀H2SO4反应中,下列各措施能加快的速率,但又不影响H2的总量的是( )
| A.加入少量的CuSO4溶液 | B.将2 mol/L的稀硫酸改成98%的浓硫酸 |
| C.将镁粉改为镁条 | D.加热 |
您最近一年使用:0次




