富马酸亚铁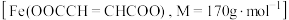 是一种治疗贫血的药物。其制备及纯度测定实验如下:
是一种治疗贫血的药物。其制备及纯度测定实验如下:
I.制备
步骤1:将 富马酸
富马酸 固体置于
固体置于 烧杯中,加水
烧杯中,加水 ,在加热搅拌下加入
,在加热搅拌下加入 溶液
溶液 ,使其
,使其 为
为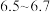 。
。
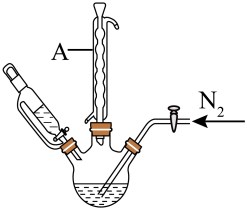
步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通 并加热一段时间后,维持温度100℃,缓慢滴加
并加热一段时间后,维持温度100℃,缓慢滴加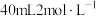 的
的 溶液,搅拌充分反应
溶液,搅拌充分反应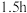 ;
; 。
。
Ⅱ.纯度测定
取 样品置于
样品置于 锥形瓶中,加入煮沸过的
锥形瓶中,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加入煮沸过的蒸馏水
,待样品完全溶解后,加入煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇
和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色),立即用
呈无色),立即用 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为 )。平行测定三次,消耗标准溶液的平均体积为
)。平行测定三次,消耗标准溶液的平均体积为 。
。
对于上述实验,下列说法正确的是
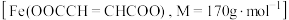 是一种治疗贫血的药物。其制备及纯度测定实验如下:
是一种治疗贫血的药物。其制备及纯度测定实验如下:I.制备
步骤1:将
 富马酸
富马酸 固体置于
固体置于 烧杯中,加水
烧杯中,加水 ,在加热搅拌下加入
,在加热搅拌下加入 溶液
溶液 ,使其
,使其 为
为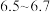 。
。步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通
 并加热一段时间后,维持温度100℃,缓慢滴加
并加热一段时间后,维持温度100℃,缓慢滴加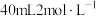 的
的 溶液,搅拌充分反应
溶液,搅拌充分反应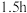 ;
;
 。
。Ⅱ.纯度测定
取
 样品置于
样品置于 锥形瓶中,加入煮沸过的
锥形瓶中,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加入煮沸过的蒸馏水
,待样品完全溶解后,加入煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇
和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色),立即用
呈无色),立即用 标准溶液滴定至终点(反应的离子方程式为
标准溶液滴定至终点(反应的离子方程式为 )。平行测定三次,消耗标准溶液的平均体积为
)。平行测定三次,消耗标准溶液的平均体积为 。
。对于上述实验,下列说法正确的是
A.“步骤1”中发生反应的离子反应为 |
| B.为提高冷凝效果,仪器A可改用直形冷凝管 |
| C.锥形瓶溶液由红色变为无色即达到滴定终点 |
D.富马酸亚铁产品的纯度为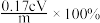 |
更新时间:2024-05-20 22:49:17
|
相似题推荐
单选题
|
困难
(0.15)
名校
【推荐1】25℃时,用浓度均为0.1mol·L-1的NaOH 溶液和盐酸分别滴定体积均为20mL,浓度均为0.1mol·L-1的HA溶液与BOH溶液。滴定过程中溶液的pH随滴加溶液的体积变化关系如图所示。下列说法中正确的是
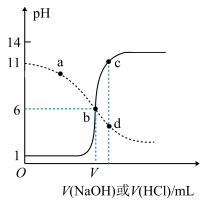

| A.HA为弱酸,BOH为强碱 |
| B.a点时,溶液中粒子浓度存在关系:c(B+)>c(Cl-)>c(OH-)>c(BOH) |
| C.b点时两种溶液中水的电离程度相同,且V=20 |
| D.c、d两点溶液混合后微粒之间存在关系:c(H+)= c(OH-)+c(BOH) |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】常温下,在含MnCl2和HCN的混合溶液中滴加NaOH溶液,得到的浊液中pX[pX=-lgc(Mn2+)或 ]与由的关系如图所示。已知,100.3=2。下列叙述正确的是
]与由的关系如图所示。已知,100.3=2。下列叙述正确的是
 ]与由的关系如图所示。已知,100.3=2。下列叙述正确的是
]与由的关系如图所示。已知,100.3=2。下列叙述正确的是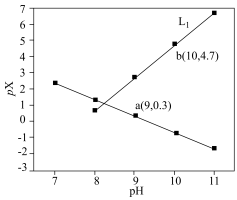
A.L1代表 与pH的关系 与pH的关系 |
B.常温下,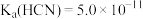 |
| C.Ksp[Mn(OH)2]的数量级为10-13 |
D.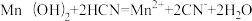 平衡常数 平衡常数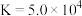 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
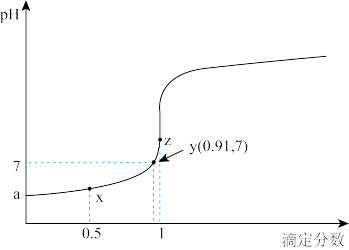
【推荐3】以0.10mol/L的氢氧化钠溶液滴定同浓度某一元酸HA的滴定曲线如图所示(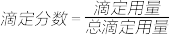 )。下列表述错误的是
)。下列表述错误的是
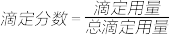 )。下列表述错误的是
)。下列表述错误的是
| A.z点后存在某点,溶液中的水的电离程度和y点的相同 |
| B.a约为3.5 |
C.z点处,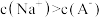 |
D.x点处的溶液中离子满足: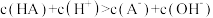 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐1】氯化亚砜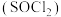 是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用
是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用 和
和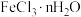 制备无水
制备无水 。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。
。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。
①称取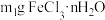 于试管中,加入足量
于试管中,加入足量 ,充分反应后固体质量为
,充分反应后固体质量为 。反应后的固体加入稀硫酸溶解,并分成两等份。
。反应后的固体加入稀硫酸溶解,并分成两等份。
②向其中一份溶液中滴加试剂X,验证实验过程中发生了副反应。
③向另一份溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,用新配制的
酸化后,用新配制的 标准溶液滴定
标准溶液滴定 ,达终点时消耗标准溶液
,达终点时消耗标准溶液 (滴定过程中
(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。
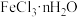 中n值计算正确的是
中n值计算正确的是
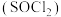 是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用
是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用 和
和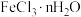 制备无水
制备无水 。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。
。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。①称取
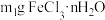 于试管中,加入足量
于试管中,加入足量 ,充分反应后固体质量为
,充分反应后固体质量为 。反应后的固体加入稀硫酸溶解,并分成两等份。
。反应后的固体加入稀硫酸溶解,并分成两等份。②向其中一份溶液中滴加试剂X,验证实验过程中发生了副反应。
③向另一份溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,用新配制的
酸化后,用新配制的 标准溶液滴定
标准溶液滴定 ,达终点时消耗标准溶液
,达终点时消耗标准溶液 (滴定过程中
(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。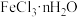 中n值计算正确的是
中n值计算正确的是A.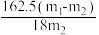 | B.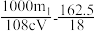 | C.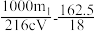 | D. |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】 某化学兴趣小组模拟酒驾的检测方法,设计如下实验:
①配制500mLc1mol/LK2Cr2O7标准溶液并加入少许稀硫酸酸化;
②量取VmL酒精溶液置于锥形瓶中;
③加入c1mol/LK2Cr2O7标准溶液V1mL,充分反应后,再加入过量的KI溶液和指示剂;
①用c2mol/LNa2S2O3溶液滴定反应后的溶液,达到滴定终点时,重复三次,平均消耗Na2S2O3溶液的体积为V2mL。
已知有关反应为:16H++2 +3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++
+3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++ +6I-=2Cr3++3I2+7H2O、I2+2
+6I-=2Cr3++3I2+7H2O、I2+2 =2I-+
=2I-+ 。
。
对上述实验,下列说法正确的是
①配制500mLc1mol/LK2Cr2O7标准溶液并加入少许稀硫酸酸化;
②量取VmL酒精溶液置于锥形瓶中;
③加入c1mol/LK2Cr2O7标准溶液V1mL,充分反应后,再加入过量的KI溶液和指示剂;
①用c2mol/LNa2S2O3溶液滴定反应后的溶液,达到滴定终点时,重复三次,平均消耗Na2S2O3溶液的体积为V2mL。
已知有关反应为:16H++2
 +3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++
+3CH3CH2OH=4Cr3++3CH3COOH+11H2O、14H++ +6I-=2Cr3++3I2+7H2O、I2+2
+6I-=2Cr3++3I2+7H2O、I2+2 =2I-+
=2I-+ 。
。对上述实验,下列说法正确的是
| A.若实验前锥形瓶中存在少量水,将导致测定结果偏小 |
| B.若因酒精挥发造成消耗Na2S2O3溶液的体积偏大,将导致测定结果偏大 |
| C.步骤③中加入K2Cr2O7溶液时,不慎有少量液体外洒,将导致测定结果偏大 |
| D.步骤④中,滴定终点时,若俯视读数,将导致测定结果偏小 |
您最近一年使用:0次




