 四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。| 阴离子 | 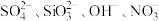 |
| 阳离子 | 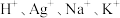 |
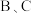 溶液混合均产生白色沉淀,
溶液混合均产生白色沉淀, 的焰色反应呈黄色。
的焰色反应呈黄色。回答下列问题:
(1)写出C的化学式:
 的电子式:
的电子式:(2)写出A溶液与
 溶液反应的离子方程式:
溶液反应的离子方程式:(3)A中阴离子的检验操作
(4)请选出适合存放
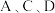 溶液的试剂瓶的序号:(每空1分)
溶液的试剂瓶的序号:(每空1分)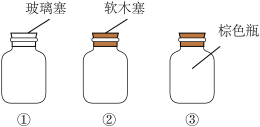
溶液 | A | C |
|
试剂瓶序号 |
相似题推荐
 、
、 、
、 取该溶液进行以下实验:
取该溶液进行以下实验:(1)用pH试纸检验,表明溶液呈强酸性,可以排除
(2)取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则产生白色沉淀的离子方程式为
(3)取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成,写出相应离子方程式:
(4)根据上述实验事实能确定溶液中肯定存在的离子是
 、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:(1)下列离子中,能大量存在于该废水中的是_______
 填标号
填标号
A. | B. | C. | D. |
 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、 用离子符号表示
用离子符号表示 。
。(3)某化学社团小组成员欲除去废水样品中的
 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:
 试剂
试剂 为
为 写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、 “分离操作”的名称是
“分离操作”的名称是 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为I.向该溶液中加入足量稀盐酸,在标准状况下放出气体;
II.向I中所得的滤液中滴加足量BaCl2溶液产生白色沉淀;
试回答下列问题:
(1)肯定存在的离子有
(2)可能存在的离子是
(3)检验溶液中肯定存在的阳离子的方法:
(1)以下说法正确的是___________。
A. 和 和 都是酸性氧化物 都是酸性氧化物 |
| B.汉白玉属于硅酸盐材料 |
C. 和 和 都能与水反应生成对应的酸 都能与水反应生成对应的酸 |
D. 和 和 都能将碳单质还原成CO 都能将碳单质还原成CO |
(3)玻璃是一种硅酸盐材料,请写出
 与碳酸钠高温条件下反应的化学方程式
与碳酸钠高温条件下反应的化学方程式(1)粘土[主要成分Al2Si2O5(OH)4] 是制备陶瓷的原料,请以氧化物形式表示粘土的组成
(2)现用四氯化硅和氮气在氢气中加强热发生反应,可制得高纯度氮化硅,反应的化学方程式为
(3)雕花玻璃是用氢氟酸对玻璃进行刻蚀,这一过程中发生反应的化学方程式为
(4)明矾可用于净水,请说明原因
(5)下图,若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在, B是白色胶状沉淀。

①实验室中常用A与某种溶液反应制备B,请写出该反应的离子方程式
②A与C也可以反应生成B,请写出反应的离子方程式
(1)在该反应中,还原剂是
(2)烟花爆竹的成分中含有黑火药。点燃后,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀引起爆炸。反应中每消耗0.1molS,释放的气体体积为
(3)除了黑火药,烟花爆竹中常加入一些金属元素,燃烧时会产生五彩缤纷的火焰。下表为一些金属元素的焰色:
| 金属元素 | 钠 | 钾 | 钙 | 锶 | 钡 | 铜 |
| 火焰颜色 | 黄 | 紫 | 砖红 | 洋红 | 黄绿 | 绿色 |
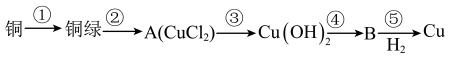
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是
(3)A、B在无色火焰上灼烧时,其焰色为
(4)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出CuCl2在水溶液中的电离方程式:
商品 | 食盐 | 碱面 | 84消毒液 | 发酵粉 |
主要成分 | ① NaCl | ② Na2CO3 | ③ NaClO | ④ NaHCO3 ⑤KAl(SO4)2·12H2O |
商品 | 料酒 | 白醋 | 洁厕灵 | \ |
主要成分 | ⑥C2H5OH | ⑦CH3COOH | ⑧HCl |
回答下列问题:
(1)以上主要成分中属于弱电解质的有
(2)当碱面不慎洒落在天然气火焰上,观察到的现象是
(3)KAl(SO4)2·12H2O的电离方程式为
(4)Na2CO3溶液中混有少量NaHCO3,可加适量的NaOH溶液除杂,离子反应方程式为
Na2CO3固体中若含有少量NaHCO3,可采取的除杂方法为
(5)NaHCO3溶液与白醋反应的离子方程式为
(6)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:



