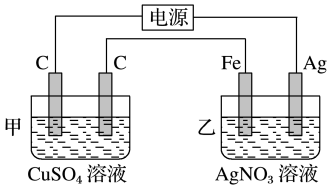
金属阳极钝化是一种电化学防护方法。将Fe 作阳极置于一定浓度的H2SO4 溶液中,一定条件下,Fe钝化形成致密Fe3O4氧化膜,试写出该过程中阳极的电极反应_______ 。
更新时间:2024-05-11 14:39:45
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】阅读短文,回答问题。
合成氨工业结束了人类依靠天然氮肥的历史,解决了人类的粮食问题。
近一百年来,工业上一直采用在高温、高压、催化剂的条件下将氮气和氢气转化为氨气,这样的条件每年需要消耗全世界1%~2%的能源供应,科学家一直致力于探索在温和条件下合成氨。
中科大研究团队研制了“钉单原子催化剂”合成氨,应用该催化剂通过电化学反应在室温下即可合成氨。原理如图1所示。

阴极表面电极反应的微观过程如图2所示。

该项研究工作开辟了单原子催化剂在电化学合成氨反应中的新途径,使得温和条件下合成氨成为可能。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)合成氨工业对解决人类的粮食问题发挥了重要作用。___________
(2)传统方法合成氨的化学方程式为N2+3H2 2NH3。
2NH3。___________
(3)传统合成氨的方法需消耗大量能源。___________
(4)“钉单原子催化剂”合成氨体现了我国科学家在科研领域的创新。___________
(5)图1中,水在阳极生成氧气。___________
(6)图2中,步骤②所示反应的方程式为有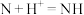 。
。___________
合成氨工业结束了人类依靠天然氮肥的历史,解决了人类的粮食问题。
近一百年来,工业上一直采用在高温、高压、催化剂的条件下将氮气和氢气转化为氨气,这样的条件每年需要消耗全世界1%~2%的能源供应,科学家一直致力于探索在温和条件下合成氨。
中科大研究团队研制了“钉单原子催化剂”合成氨,应用该催化剂通过电化学反应在室温下即可合成氨。原理如图1所示。

阴极表面电极反应的微观过程如图2所示。

该项研究工作开辟了单原子催化剂在电化学合成氨反应中的新途径,使得温和条件下合成氨成为可能。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)合成氨工业对解决人类的粮食问题发挥了重要作用。
(2)传统方法合成氨的化学方程式为N2+3H2
 2NH3。
2NH3。(3)传统合成氨的方法需消耗大量能源。
(4)“钉单原子催化剂”合成氨体现了我国科学家在科研领域的创新。
(5)图1中,水在阳极生成氧气。
(6)图2中,步骤②所示反应的方程式为有
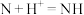 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。

①H+向___ (填“左”或“右”)移动。
②a电极为电解池的___ (填“阴”或“阳”)极,写出该电极的电极反应式:___ 。
(2)利用甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含Cr2O )时实验室利用如图装置模拟该法:
)时实验室利用如图装置模拟该法:

①M电极发生反应的电极反应式为___ 。
②已知电解池溶液里将Cr2O 转化为Cr3+,该反应的离子方程式为
转化为Cr3+,该反应的离子方程式为___ 。
③当N电极消耗标况下2.24L气体时,通过质子交换膜的离子数目为___ 。
(1)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。

①H+向
②a电极为电解池的
(2)利用甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含Cr2O
 )时实验室利用如图装置模拟该法:
)时实验室利用如图装置模拟该法:
①M电极发生反应的电极反应式为
②已知电解池溶液里将Cr2O
 转化为Cr3+,该反应的离子方程式为
转化为Cr3+,该反应的离子方程式为③当N电极消耗标况下2.24L气体时,通过质子交换膜的离子数目为
您最近一年使用:0次
【推荐1】Ⅰ.某研究小组利用如图1所示装置探究金属Fe的腐蚀与防护条件{已知Fe2+遇K3[Fe(CN)6]溶液生成蓝色沉淀}。反应一段时间后,分别向①区和②区的Cu电极附近滴加酚酞试液,向①区和②区的Fe电极附近滴加K3[Fe(CN)6]溶液。

(1)①区在Cu电极附近,②区Fe电极附近可观察到的现象分别是_______ 、_______ ,④区Zn电极的电极反应式为_______ 。
(2)上述①③两个实验表明,活泼性不同的两种金属作电极构成原电池时,一般是相对不活泼的金属被保护,根据此原理采取的金属防护方法称为_______ 。
Ⅱ.某研究小组又利用图2装置制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH- Fe
Fe +3H2↑。装置通电后,铁电极附近生成紫红色Fe
+3H2↑。装置通电后,铁电极附近生成紫红色Fe ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。

已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
(3)电解过程中须将阴极产生的气体及时排出,其原因是_______ 。
(4)c(Na2FeO4)随初始c(NaOH)的变化如图3所示。
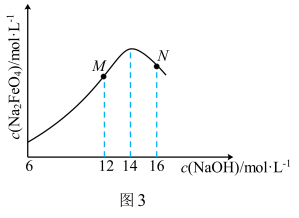
M、N两点的c(Na2FeO4)均低于最高值的原因是_______ 。

(1)①区在Cu电极附近,②区Fe电极附近可观察到的现象分别是
(2)上述①③两个实验表明,活泼性不同的两种金属作电极构成原电池时,一般是相对不活泼的金属被保护,根据此原理采取的金属防护方法称为
Ⅱ.某研究小组又利用图2装置制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-
 Fe
Fe +3H2↑。装置通电后,铁电极附近生成紫红色Fe
+3H2↑。装置通电后,铁电极附近生成紫红色Fe ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。
已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
(3)电解过程中须将阴极产生的气体及时排出,其原因是
(4)c(Na2FeO4)随初始c(NaOH)的变化如图3所示。

M、N两点的c(Na2FeO4)均低于最高值的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】为了延长锅炉的使用寿命,常在其内壁焊上锌片。请简要说明这种做法所依据的原理_______________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】为了防止铁被腐蚀,常在铁皮表面镀上一层较耐腐蚀的金属,如镀锌铁和镀锡铁,若罐头欲装蕃茄酱,该罐头的材料应选用上述的_______ 铁。各取一小块镀锌铁皮和镀锡铁皮,用小刀在上面刻划,露出里面的铁,然后在刻痕上滴一滴氯化钠溶液,再滴一滴K3[Fe(CN)6]溶液(K3[Fe(CN)6]溶液遇到Fe2+会出现蓝色沉淀),静置数分钟后先出现蓝色沉淀现象的哪一块铁片?_______ ;在铁片上发生的电极反应式为_______ ;在另一种金属上发生的电极反应式为_______ 。
您最近一年使用:0次