一种营养强化剂的结构简式如图所示。X、Y、Z、W的原子序数依次增大,Y和W位于第二周期,R位于元素周期表第四周期ds区,其基态原子无未成对电子。下列说法正确的是
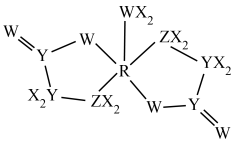
A.电负性: |
| B.基态R原子核外电子中有30个自旋方向相同 |
C.最简单氢化物的键角: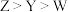 |
| D.从结构推测该物质水溶性较好 |
更新时间:2024-05-13 17:25:54
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于核外电子的描述中,正确的是( )
| A.电子云图中一个小黑点表示一个电子 |
| B.电子式中元素符号周围的小黑点数表示核外电子总数 |
| C.s电子在s电子云的球形空间内做规则运动 |
| D.核外电子的能量大小主要是由电子层和电子亚层决定 |
您最近一年使用:0次
【推荐2】离子液体是一种只由离子组成的液体,在低温下也能以液态稳定存在,是一种很有研究价值的溶剂。研究显示最常见的离子液体主要由如图所示的正离子和负离子组成,下列说法正确的是
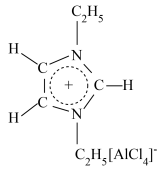

A. 电子式为 电子式为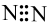 |
B.基态铝原子最外层结构的轨道表示式: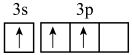 |
C.酸性: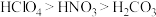 |
| D.基态氯原子有9种不同运动状态的电子 |
您最近一年使用:0次
【推荐1】短周期主族元素X、Y、Z、W、Q原子序数依次增大,其中Q是元素周期表中电负性最大的元素,由这五种元素组成的某药物结构如图所示。下列有关说法正确的是

A.电负性: |
B.第一电离能: |
| C.该分子中所有原子都满足8电子稳定结构 |
D.基态Z原子电子轨道表示式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列性质的比较中,能用周期律解释的是
| A.第一电离能:N>O | B.沸点:NH3>PH3 |
| C.酸性:CH3COOH<CCl3COOH | D.酸性:HNO3>H2SO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知通常分子中所含的键能越大,分子越稳定。参考下表中化学键的键能数据,判断下列分子中,受热时最不稳定的是( )
化学键 | H—H | H—Cl | H—Br | H—I |
键能kJ·mol-1 | 436.0 | 431.8 | 366 | 298.7 |
| A.氢气 | B.氯化氢 |
| C.溴化氢 | D.碘化氢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
①下列量子数可以存在:3, 0,-1,-1/2
②共价化合物一定含共价键,一定不含离子键
③水的非直线结构是由共价键的饱和性决定的
④由非金属元素组成的化合物一定是共价化合物
⑤分子中不一定存在共价键
⑥烯烃比烷烃的化学性质活泼是由于烷烃中的σ键比烯烃中的σ键稳定
①下列量子数可以存在:3, 0,-1,-1/2
②共价化合物一定含共价键,一定不含离子键
③水的非直线结构是由共价键的饱和性决定的
④由非金属元素组成的化合物一定是共价化合物
⑤分子中不一定存在共价键
⑥烯烃比烷烃的化学性质活泼是由于烷烃中的σ键比烯烃中的σ键稳定
| A.②⑤ | B.④⑥ | C.②③④ | D.①③⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铁、氮气、丙酮(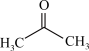 )和乙醇可参与制备铁氮化合物(FexNy),以下说法不正确的是
)和乙醇可参与制备铁氮化合物(FexNy),以下说法不正确的是
 )和乙醇可参与制备铁氮化合物(FexNy),以下说法不正确的是
)和乙醇可参与制备铁氮化合物(FexNy),以下说法不正确的是| A.丙酮中碳原子采用sp2和sp3杂化 |
| B.Fe元素位于元素周期表的第VIIIB族 |
| C.1个N2分子中有1个σ键和2个π键 |
| D.乙醇的沸点高于丙烷,是因为乙醇分子间存在氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知结构为正四面体形的离子E和直线形离子G反应,生成三角锥形分子L和V形分子M(组成E、G、L、M粒子的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是( )
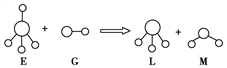

| A.四中粒子中都只含有极性键 |
| B.L、M都是极性分子 |
| C.L易溶于水,是因为与水形成分子间氢键 |
| D.E、L、M的中心原子都采取sp2杂化 |
您最近一年使用:0次



