链状葡萄糖分子中的醛基可与分子内羟基发生加成反应形成两种六元环状结构。常温下,各种葡萄糖结构及其所占百分含量如下图所示。已知各种葡萄糖结构中链状结构的熵最大,两种环状结构的熵相近。下列说法正确的是

A. |
B.三种结构中,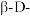 吡喃葡萄糖的焓最小 吡喃葡萄糖的焓最小 |
| C.葡萄糖由链状转化为环状结构是醛基和6号碳原子上羟基作用的结果 |
D.18g葡萄糖完全燃烧生成 和 和 放热akJ,故葡萄糖的燃烧热为10akJ/mol 放热akJ,故葡萄糖的燃烧热为10akJ/mol |
更新时间:2024-05-19 08:41:45
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程如图所示(图中只画出了 HAP的部分结构,用18O标记羟基磷灰石中的羟基氧原子)。下列说法正确的是


| A.反应物的键能之和大于生成物的键能之和 |
| B.HAP改变了该反应的历程和焓变,加快了反应速率 |
| C.经过该催化氧化过程后18O仍然在HAP中 |
| D.反应过程中,碳原子由sp2杂化变为sp杂化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】根据下图所得判断正确的是( )
已知:I2(g)=I2(s) ΔH=-62.4kJ/mol


已知:I2(g)=I2(s) ΔH=-62.4kJ/mol
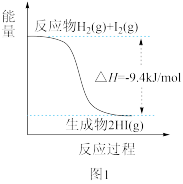
| A.图1反应为吸热反应 |
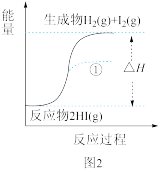
B.图2反应的热化学方程式为2HI(g) H2(g)+I2(g) ΔH=+9.4kJ/mol H2(g)+I2(g) ΔH=+9.4kJ/mol |
| C.图2中若I2的状态为固态,则能量变化曲线可能为① |
| D.断裂1molH2(g)和1molI2(g)中化学键需要的能量大于断裂2molHI(g)中化学键需要的能量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】根据下列图示所得出的结论正确的是
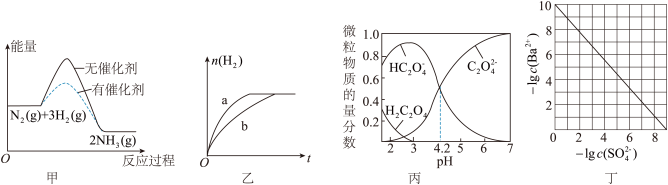

A.图甲表示.N2(g)+3H2(g) 2NH3(g)反应过程的能量变化关系,说明催化剂可以改变该反应的焓变 2NH3(g)反应过程的能量变化关系,说明催化剂可以改变该反应的焓变 |
| B.图乙表示等量的钠块分别与足量的水和乙醇反应产生氢气的物质的量随时间的变化关系,则曲线b表示水与钠的反应 |
| C.图丙表示25℃时水溶液中H2C2O4、HC2O4-、C2O42-的物质的量分数随pH的分布,说明H2C2O4的Ka1=1×10-4.2 |
| D.图丁表示25℃时BaSO4达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42-)的关系曲线,说明Ksp(BaSO4)=1×10-10 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知:①2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1
②H2S(g)=H2(g)+S(g) ΔH=+20.1 kJ·mol-1下列判断正确的是
②H2S(g)=H2(g)+S(g) ΔH=+20.1 kJ·mol-1下列判断正确的是
| A.氢气的燃烧热:ΔH=-241.8 kJ·mol-1 |
| B.②中若生成固态硫,ΔH将增大 |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.相同条件下,充分燃烧1 mol H2(g)与1 mol S(g)的混合物比充分燃烧1 mol H2S(g)放热多20.1 kJ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知101kPa、25℃下,1 mol可燃物完全燃烧生成稳定的 化合物时所放出的热量,叫做该物质的燃烧热。已知葡萄糖[C6H12O6(s)]的燃烧热为2804 kJ·mol-1。图中能正确表示反应:6CO2(g)+6H2O(g)=C6H12O6(s)+6O2(g)的能量变化曲线的是
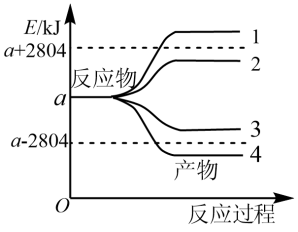
| A.曲线1 | B.曲线2 | C.曲线3 | D.曲线4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列关于各图的叙述正确的是
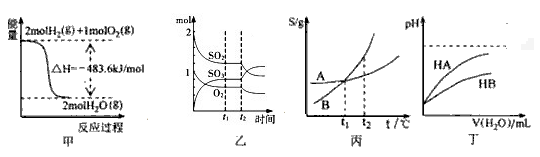

| A.图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ•mol-1 |
B.图乙表示一定条件下进行的反应2SO2+O2 2SO3各成分的物质的量变化,t2时刻改变的条件一定是缩小容器体积 2SO3各成分的物质的量变化,t2时刻改变的条件一定是缩小容器体积 |
| C.图丙表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数ω(B)>ω(A) |
| D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知2P(s)+3Cl2(g)=2PCl3(g)△H=﹣612kJ•mol﹣1.
PCl5(g)=PCl3(g)+Cl2(g)△H=+93kJ•mol﹣1.
则P(s)+ Cl2(g)=PCl5(g) 的△H是( )
Cl2(g)=PCl5(g) 的△H是( )
PCl5(g)=PCl3(g)+Cl2(g)△H=+93kJ•mol﹣1.
则P(s)+
 Cl2(g)=PCl5(g) 的△H是( )
Cl2(g)=PCl5(g) 的△H是( )| A.﹣705kJ•mol﹣1 | B.﹣399kJ•mol﹣1 |
| C.﹣203kJ mol﹣1 | D.﹣213kJ•mol﹣1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在298K和100kPa压力下,已知金刚石和石墨的熵、燃烧热和密度分别为:
此条件下,对于反应C(石墨)→C(金刚石),下列说法正确的是
物质 | S/(J·K−1·mol−1) | ∆H/(kJ·mol−1) | ρ/(kg·m−3) |
C(金刚石) | 2.4 | −395.40 | 3513 |
C(石墨) | 5.7 | −393.51 | 2260 |
| A.该反应的∆H<0,∆S<0 |
| B.由公式∆G=∆H−T∆S可知,该反应∆G=985.29kJ·mol−1 |
| C.金刚石比石墨稳定 |
| D.超高压条件下,石墨有可能变为金刚石 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 在葡萄糖溶液中滴入少量酸性 溶液,观察 溶液,观察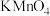 溶液是否褪色 溶液是否褪色 | 葡萄糖中是否含有醛基 |
| B | 室温下,用pH计分别测定浓度均为0.1mol· 的NaClO和 的NaClO和 溶液的pH 溶液的pH | 比较 和 和 的大小 的大小 |
| C | 将镀层破损的镀锌铁片放入酸化的3%NaCl溶液中一段时间后,取溶液于试管中,滴加KSCN溶液,观察现象 | 已破损的镀层锌是否仍对铁有保护作用 |
| D | 取两支试管,分别加入2mL0.5mol· 的 的 溶液,将其中一支试管先加热,然后置于冷水中,与另一支管对比 溶液,将其中一支试管先加热,然后置于冷水中,与另一支管对比 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】设 为阿伏加德罗常数的值,下列叙述中错误的是
为阿伏加德罗常数的值,下列叙述中错误的是
 为阿伏加德罗常数的值,下列叙述中错误的是
为阿伏加德罗常数的值,下列叙述中错误的是A.1mol葡萄糖分子含有的羟基数目为 |
B.30g乙酸与尿素 组成的混合物中含有氢原子总数为 组成的混合物中含有氢原子总数为 |
C.常温常压下,100g46%的乙醇溶液中,含H—O键的数目为 |
D.标准状况下甲烷和氧气的混合气体共22.4L,完全燃烧后的物质的分子总数一定为 |
您最近一年使用:0次

 O2(g)+H2(g)
O2(g)+H2(g)
 C6H12O6(葡萄糖)
C6H12O6(葡萄糖) 2CH3CH2OH+2CO2↑
2CH3CH2OH+2CO2↑

