短周期元素X、Y、Z、W、Q原子序数依次增大。W简单离子在同周期离子中半径最小;基态X、Z、Q原子均有两个单电子,Q与Z同主族。下列说法不正确 的是
A.第一电离能: |
B.电负性: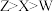 |
| C.Z与Q形成的化合物可能是非极性分子 |
| D.Z的氢化物沸点不可能低于X的氢化物沸点 |
2024·浙江金华·三模 查看更多[3]
更新时间:2024-06-02 12:26:40
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】叶蜡石的化学式为X2 [Y4 Z10](ZW)2,短周期元素W、Z、X、Y的原子序数依次增大,X与Y为同一周期相邻元素,Y的最外层电子数为次外层的一半,X的离子与ZW-含有相同的电子数。下列说法错误的是
| A.X的最高价氧化物可作耐火材料 |
| B.常温常压下,Z和W形成的常见化合物均为液体 |
| C.原子半径:X > Y > Z > W |
| D.可用NaOH溶液分离X单质和Y单质的混合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲~辛八种元素在周期表中的相对位置如图所示。乙是原子半径最大的短周期主族元素,且与己的原子序数相差3,丁与辛同周期。下列判断正确的是
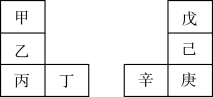
| A.氢化物的沸点:戊<己 |
| B.最高价氧化物对应水化物的碱性:丁<辛<庚 |
| C.己与庚的原子序数相差18 |
| D.乙的单质与水、O2都能剧烈反应,含乙元素的产物都既含离子键,又含极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】X、Y、Z、W是4种短周期主族元素,在周期表中的相对位置如表,已知四种元素的原子最外层电子数之和为18,则以下说法中正确的是( )

| A.Y的最高正化合价与最低负化合价的代数和为2 |
| B.X、Y、Z、W四种原子中,X的原子半径最小 |
| C.Y的氢化物的沸点一定高于X的氢化物的沸点 |
| D.X、Y、W三种元素氧化物对应的水化物的酸性依次增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据表1信息,判断以下叙述正确的是( )
表1部分短周期元素的原子半径及主要化合价
表1部分短周期元素的原子半径及主要化合价
| 元素代号 | X | Y | Z | M | N |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A.氢化物的稳定性为H2N>H2M |
| B.X、Y的金属性X<Y |
| C.Y的最高价氧化物的水化物能溶于稀氨水 |
| D.X2+与M2-具有相同的电子层结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】 、
、 、
、 均为短周期主族元素,它们原子的最外层电子数之和为10。
均为短周期主族元素,它们原子的最外层电子数之和为10。 与
与 同族,
同族, 最外层电子数等于
最外层电子数等于 次外层电子数,且
次外层电子数,且 原子半径大于
原子半径大于 。下列叙述正确的是( )。
。下列叙述正确的是( )。
 、
、 、
、 均为短周期主族元素,它们原子的最外层电子数之和为10。
均为短周期主族元素,它们原子的最外层电子数之和为10。 与
与 同族,
同族, 最外层电子数等于
最外层电子数等于 次外层电子数,且
次外层电子数,且 原子半径大于
原子半径大于 。下列叙述正确的是( )。
。下列叙述正确的是( )。A. 和 和 的氧化物中均含离子键 的氧化物中均含离子键 |
B.热稳定性: 的简单氢化物大于 的简单氢化物大于 的简单氢化物 的简单氢化物 |
C. 与 与 可形成离子化合物 可形成离子化合物 |
D. 的单质与 的单质与 的单质均能溶于浓硝酸 的单质均能溶于浓硝酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】三种前四周期主族元素X、Y、Z形成的一种化合物具有高效的储氢性能,其氢含量高达7.84%,释氢时的原理为Z(YX4)2=ZX2+2Y+3X2。下列说法错误的是
| A.化合物Z(YX4)2中的Y不满足8电子稳定结构 |
| B.化合物Z(YX4)2中含有离子键、共价键、配位键 |
| C.同周期中第一电离能小于Y的元素只有1种 |
D.YX 阴离子为正四面体结构 阴离子为正四面体结构 |
您最近一年使用:0次
【推荐2】X、Y、Z、W是原子序数递增的短周期元素,X元素基态原子最外电子层上s、p电子数相等;Y的最高价氧化物对应的水化物与最低价氢化物可以生成一种盐;Z元素基态原子价层电子排布为 ;W元素基态原子的M层有1个未成对的p电子。下列说法
;W元素基态原子的M层有1个未成对的p电子。下列说法一定 正确的是
 ;W元素基态原子的M层有1个未成对的p电子。下列说法
;W元素基态原子的M层有1个未成对的p电子。下列说法A.电负性: | B.电离能: |
C.最高正价: | D.最高价氧化物对应水化物的酸性: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述中,错误的是
A. 的熔沸点比 的熔沸点比 高,与分子间的范德华力有关系 高,与分子间的范德华力有关系 |
B. 易溶于 易溶于 ,可用相似相溶规律解释 ,可用相似相溶规律解释 |
C. 分子中 分子中 键与 键与 键个数比为4∶1 键个数比为4∶1 |
D. 为V形极性分子,微粒间的作用力为范德华力 为V形极性分子,微粒间的作用力为范德华力 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】LDFCB是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成,结构如图,Y的最外层电子数等于X的核外电子总数,下列说法正确的是
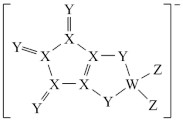

| A.同周期元素第一电离能小于Y的有5种 |
| B.简单氢化物的沸点:X<Y |
| C.W、Z形成的化合物分子是含有极性键的极性分子 |
| D.四种元素形成的简单氢化物中X的最稳定 |
您最近一年使用:0次

 的键角相等
的键角相等

