据海通证券发布的最新研究报告表明,受尼龙66的拉动,目前我国己二酸供给缺口较大,且预计2024—2026年仍将整体处于紧缺状态.实验室模拟高锰酸钾氧化环己醇(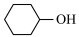 )制备己二酸
)制备己二酸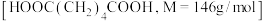 的实验过程如下:
的实验过程如下:
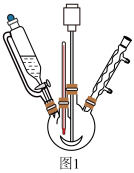
②用电热套加热升温到40℃,移走电热套,缓慢滴加环己醇,控制温度50℃左右,使之充分反应;
③趁热抽滤,用热水洗涤滤渣
 2~3次,合并滤液;
2~3次,合并滤液;④向滤液中加入4mL浓盐酸酸化,加热浓缩,冷却析出晶体,抽滤,得到己二酸粗品4.599g.回答下列问题:
(1)已知:
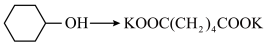 会放出热量,补全该反应的化学方程式
会放出热量,补全该反应的化学方程式(2)经反复实验对比研究,该实验条件下环己醇滴速控制在20s/滴时最佳,理由是
(3)实验中判断反应进行完全的方法是用玻璃棒蘸取1滴反应混合物,点到滤纸上,若滤纸上
(4)步骤④中抽滤时采用如下装置(图2).抽滤时先打开水龙头,抽气管,用倾析法将混合物转移至布氏漏斗中.抽滤完毕,接下来的操作是
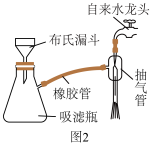
(5)步骤④中加入浓盐酸酸化的目的是
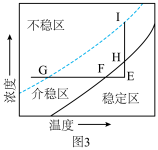
(6)图3是己二酸的浓度与温度关系曲线图.介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸溶液处于
更新时间:2024-05-28 13:08:37
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】邻硝基苯甲醛是一种重要的精细化学品,实验室可通过图1装置(夹持仪器已略去),以邻硝基苯甲醇为原料,利用两相反应体系(图2)实现邻硝基苯甲醛的选择性氧化合成.已知部分物质的性质如下表所示。

实验步骤如下:
I.向三颈瓶中依次加入 邻硝基苯甲醇,
邻硝基苯甲醇, 二氯甲烷(沸点
二氯甲烷(沸点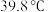 )和磁子,搅拌使固体全部溶解。再依次加入
)和磁子,搅拌使固体全部溶解。再依次加入 水溶液(做催化剂)和
水溶液(做催化剂)和 饱和
饱和 溶液。在
溶液。在 和剧烈搅拌条件下,滴加
和剧烈搅拌条件下,滴加 足量
足量 水溶液后,继续反应
水溶液后,继续反应 。
。
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用 二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在 二氯甲烷中,加入
二氯甲烷中,加入 饱和
饱和 溶液,充分作用后,分离得到水层,水层在冰浴中用
溶液,充分作用后,分离得到水层,水层在冰浴中用 氢氧化钠溶液调节到
氢氧化钠溶液调节到 ,浅黄色固体析出完全.抽滤、干燥至恒重,得
,浅黄色固体析出完全.抽滤、干燥至恒重,得 产品。
产品。
(1)控制反应温度为 的方法是
的方法是__________ ;滴加 溶液时,需要先将漏斗上端玻璃塞打开,目的是
溶液时,需要先将漏斗上端玻璃塞打开,目的是_______________ 。
(2)合成产品的化学方程式为________________ 。
(3)相比于单相反应体系,利用两相反应体系可以大幅减少副产物的量,原因是______________ ;该副产物主要成分是_______________ 。
(4)步骤Ⅱ中除去并回收二氯甲烷的实验方法是_________________ 。
(5)若用一定浓度盐酸代替“步骤Ⅲ”中的 氢氧化钠溶液调节
氢氧化钠溶液调节 ,
,_________________ (填“能”或“不能”)析出大量产品,原因是___________________ 。
(6)本实验产率为________________ (计算结果保留3位有效数字)。
| 物质 | 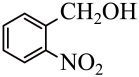 |  |  |
| 溶解性 | 微溶于水,易溶于 | 难溶于水,易溶于 | 易溶水,难溶于 |
熔点/ | 70 | 43 | — |
沸点/ | 270 | 153 | — |
| 性质 | 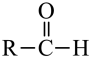   (易溶于水) (易溶于水) | ||

实验步骤如下:
I.向三颈瓶中依次加入
 邻硝基苯甲醇,
邻硝基苯甲醇, 二氯甲烷(沸点
二氯甲烷(沸点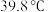 )和磁子,搅拌使固体全部溶解。再依次加入
)和磁子,搅拌使固体全部溶解。再依次加入 水溶液(做催化剂)和
水溶液(做催化剂)和 饱和
饱和 溶液。在
溶液。在 和剧烈搅拌条件下,滴加
和剧烈搅拌条件下,滴加 足量
足量 水溶液后,继续反应
水溶液后,继续反应 。
。Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用
 二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。Ⅲ.将粗品溶解在
 二氯甲烷中,加入
二氯甲烷中,加入 饱和
饱和 溶液,充分作用后,分离得到水层,水层在冰浴中用
溶液,充分作用后,分离得到水层,水层在冰浴中用 氢氧化钠溶液调节到
氢氧化钠溶液调节到 ,浅黄色固体析出完全.抽滤、干燥至恒重,得
,浅黄色固体析出完全.抽滤、干燥至恒重,得 产品。
产品。(1)控制反应温度为
 的方法是
的方法是 溶液时,需要先将漏斗上端玻璃塞打开,目的是
溶液时,需要先将漏斗上端玻璃塞打开,目的是(2)合成产品的化学方程式为
(3)相比于单相反应体系,利用两相反应体系可以大幅减少副产物的量,原因是
(4)步骤Ⅱ中除去并回收二氯甲烷的实验方法是
(5)若用一定浓度盐酸代替“步骤Ⅲ”中的
 氢氧化钠溶液调节
氢氧化钠溶液调节 ,
,(6)本实验产率为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
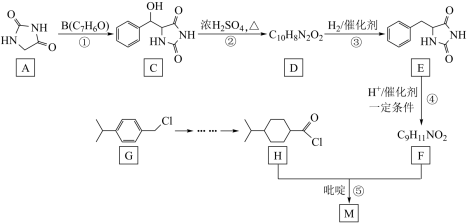
【推荐2】一种重要的降血糖药物M( )的合成路线如下(略去部分反应条件):
)的合成路线如下(略去部分反应条件):
已知: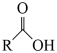
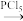

回答下列问题:
(1)A的分子式为________ 。
(2)反应③的反应类型为______ 。
(3)下列关于上述涉及的有机物的说法不正确的是_____ (填标号)。
a.化合物E能使酸性高锰酸钾溶液褪色
b.化合物F既能与盐酸反应,又能与NaOH溶液反应
c.M中含氧官能团的名称为酯基、酮基
(4)写出F+H→M的化学方程式:_______ 。
(5)物质I与G互为同分异构体,满足下列条件的I的结构有______ 种,写出1H-NMR谱中峰面积比为9:2:2的结构简式:_______ 。
①一定条件下水解后的产物能与FeCl3溶液发生显色反应
②苯环上只有两个取代基
(6)请设计以G为原料合成H的合成路线流程图(无机试剂任选):______ 。
 )的合成路线如下(略去部分反应条件):
)的合成路线如下(略去部分反应条件):
已知:

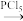

回答下列问题:
(1)A的分子式为
(2)反应③的反应类型为
(3)下列关于上述涉及的有机物的说法不正确的是
a.化合物E能使酸性高锰酸钾溶液褪色
b.化合物F既能与盐酸反应,又能与NaOH溶液反应
c.M中含氧官能团的名称为酯基、酮基
(4)写出F+H→M的化学方程式:
(5)物质I与G互为同分异构体,满足下列条件的I的结构有
①一定条件下水解后的产物能与FeCl3溶液发生显色反应
②苯环上只有两个取代基
(6)请设计以G为原料合成H的合成路线流程图(无机试剂任选):
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】1,6—己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6—己二酸,反应原理为:



 ;
;
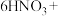

 。
。

相关物质的物理性质见表:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入 固体和18mL浓
固体和18mL浓 (略过量),向恒压滴液漏斗中加入6mL环己醇;
(略过量),向恒压滴液漏斗中加入6mL环己醇;
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃,移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇,调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕;
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止,然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品;
Ⅳ.1,6-己二酸粗产品的提纯。
(1)仪器A的名称为___________ ,其作用是___________ 。
(2)B中发生反应的化学反应方程式为___________ (其中一种产物为亚硝酸盐)。
(3)滴加环己醇的过程中,可用冷水浴冷却维持50~60℃,防止温度过高,说明该反应的
___________ 0(填“>”或“<”)。
(4)步骤Ⅲ中需“迅速将”三颈烧瓶中混合液倒入烧杯中的原因是___________ ,将步骤Ⅲ补充完整:___________ 。
(5)步骤Ⅳ提纯粗产品的方法的名称为___________ 。
(6)最终得到1,6—己二酸产品4.810g,则1,6—己二酸的产率为___________ 。(保留三位有效数字)



 ;
;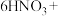

 。
。
相关物质的物理性质见表:
| 试剂 | 相对分子质量 | 密度/( ) ) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6—己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
 | 117 | 2.326 | 210(分解) | - | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入
 固体和18mL浓
固体和18mL浓 (略过量),向恒压滴液漏斗中加入6mL环己醇;
(略过量),向恒压滴液漏斗中加入6mL环己醇;Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃,移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇,调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕;
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止,然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品;
Ⅳ.1,6-己二酸粗产品的提纯。
(1)仪器A的名称为
(2)B中发生反应的化学反应方程式为
(3)滴加环己醇的过程中,可用冷水浴冷却维持50~60℃,防止温度过高,说明该反应的

(4)步骤Ⅲ中需“迅速将”三颈烧瓶中混合液倒入烧杯中的原因是
(5)步骤Ⅳ提纯粗产品的方法的名称为
(6)最终得到1,6—己二酸产品4.810g,则1,6—己二酸的产率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】氯亚铂酸钾是合成绝大部分二价铂化合物的原料,广泛应用于电镀、医药中间体、催化剂前驱体等的制备。
已知:
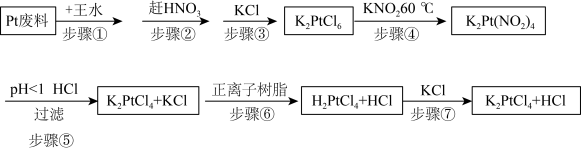
利用Pt废料制备氯亚铂酸钾,流程如下:
(2)关于实验步骤说法错误的是___________。
(3)步骤④发生时有红棕色气体生成,写出发生的化学反应方程式,并标出电子转移的方向和数目___________ 。
(4)步骤⑦得到的溶液中含 和HCl,为了进一步得到晶体
和HCl,为了进一步得到晶体 ,需进一步蒸发浓缩(温度75℃附近)、冷却结晶、过滤、用乙醇洗涤、干燥得氯亚铂酸钾(
,需进一步蒸发浓缩(温度75℃附近)、冷却结晶、过滤、用乙醇洗涤、干燥得氯亚铂酸钾( )成品。
)成品。
①蒸发浓缩需要控制温度75℃附近的原因___________ 。
②洗涤操作中,用乙醇洗涤相比于用蒸馏水洗涤的优势是___________ 。
A.减小固体的溶解损失
B.除去固体表面吸附的杂质
C.乙醇挥发带走水分,使固体快速干燥
③实验室进行以上步骤不需要用到的仪器是___________ 。___________ 。
已知:
| 氯亚铂酸钾(K2PtCl4) | 水溶性可溶 10 g/L(20℃)、不溶于乙醇、受热分解。 |
| 氯铂酸钾(K2PtCl6) | 溶于热水、微溶于冷水、几乎不溶于乙醇、乙醚。 |
| 氯铂酸(H2PtCl6) | 110℃时部分分解,150℃开始生成金属铂。 |
| 亚硝酸钾(KNO2) | 有一定还原性,还原性:KNO2弱于K2C2O4。 |
| 亚硝酸(HNO2) | 弱酸、不稳定、易分解。 |
| A.步骤①中王水可以用浓硫酸代替 |
| B.步骤②利用硝酸的易挥发性,适合加强热 |
| C.步骤③加入KCl能促进K2PtCl6晶体析出 |
| D.步骤④用还原剂K2C2O4代替更好 |
(2)关于实验步骤说法错误的是___________。
| A.步骤⑤利用酸性条件下亚硝酸的不稳定性 |
B.步骤⑥用正离子树脂交换是指 和 和 的交换 的交换 |
| C.步骤⑦是氧化还原反应 |
| D.最后得到的溶液中经蒸发能除去HCl |
(3)步骤④发生时有红棕色气体生成,写出发生的化学反应方程式,并标出电子转移的方向和数目
(4)步骤⑦得到的溶液中含
 和HCl,为了进一步得到晶体
和HCl,为了进一步得到晶体 ,需进一步蒸发浓缩(温度75℃附近)、冷却结晶、过滤、用乙醇洗涤、干燥得氯亚铂酸钾(
,需进一步蒸发浓缩(温度75℃附近)、冷却结晶、过滤、用乙醇洗涤、干燥得氯亚铂酸钾( )成品。
)成品。①蒸发浓缩需要控制温度75℃附近的原因
②洗涤操作中,用乙醇洗涤相比于用蒸馏水洗涤的优势是
A.减小固体的溶解损失
B.除去固体表面吸附的杂质
C.乙醇挥发带走水分,使固体快速干燥
③实验室进行以上步骤不需要用到的仪器是
A.  B.
B.  C.
C.  D.
D.
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
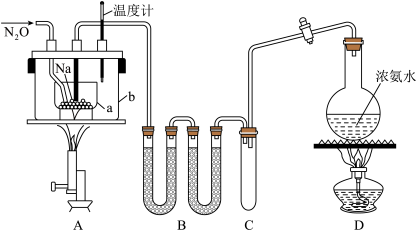
【推荐2】叠氮化钠(NaN3)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为_____________ ;装置C的主要作用是______________________ 。
(2)步骤①中先加热通氨气的目的是_____________________________________ ;步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为_______________________________ 。步骤③中最适宜的加热方式为 ___________ (填“水浴加热”,“油浴加热”)。
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)___________ 。
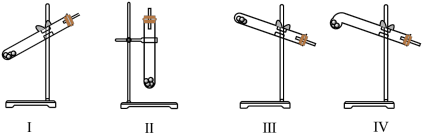
(4)生成NaN3的化学方程式为_____________________________________ 。
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是__________________ 。
(6)步骤④中用乙醚洗涤的主要目的是_______________________________ 。
(7)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500 g试样配成500.00 mL溶液。②取50.00 mL溶液置于锥形瓶中,加入50.00 mL 0.1010 mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8 mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑;Ce4++Fe2+=Ce3++Fe3+;试样中NaN3的质量分数为_______________ 。
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为
(2)步骤①中先加热通氨气的目的是
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)

(4)生成NaN3的化学方程式为
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是
(6)步骤④中用乙醚洗涤的主要目的是
(7)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500 g试样配成500.00 mL溶液。②取50.00 mL溶液置于锥形瓶中,加入50.00 mL 0.1010 mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8 mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑;Ce4++Fe2+=Ce3++Fe3+;试样中NaN3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】钽是一种过渡金属,钽酸锂(LiTaO3)可用于制作滤波器。一种制备钽酸锂的流程如下:回答下列问题:

(1)LiTaO3中钽的化合价为___ 。
(2)同体A呈红色,其主要成分是___ (写化学式),常见用途有___ (填一种即可)。
(3)操作2的名称是___ ,用来检验溶液B中阴离子的常用试剂是___ 。
(4)HTaO3是___ (填字母)。
a.难溶的强酸 b.可溶的弱酸 c.可溶的强酸 d.难溶的弱酸
(5)烧渣与NaOH溶液转化成溶液A的过程中,发生反应的离子方程式为___ 。
(6)上述废料中含Ta2O5的质量分数为44.2%,杂质不含Ta元素。现有100kg该废料,按上述流程最多可制备___ kgLiTaO3。

(1)LiTaO3中钽的化合价为
(2)同体A呈红色,其主要成分是
(3)操作2的名称是
(4)HTaO3是
a.难溶的强酸 b.可溶的弱酸 c.可溶的强酸 d.难溶的弱酸
(5)烧渣与NaOH溶液转化成溶液A的过程中,发生反应的离子方程式为
(6)上述废料中含Ta2O5的质量分数为44.2%,杂质不含Ta元素。现有100kg该废料,按上述流程最多可制备
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发黏、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生在SCl2。____________ ,装置F中试剂的作用是____________ 。
②装置连接顺序:A→________ →________ →________ →E→D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是____________ 。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和____________ 。
(2)少量S2Cl2泄漏时应喷水减慢其挥发(或扩散),并产生酸性悬浊液,但不要对泄漏物或泄漏点直接喷水,其原因是____________ 。
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。____________ (填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为____________ (用含V、m的式子表示)。
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解 ②S2Cl2+Cl2 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生在SCl2。
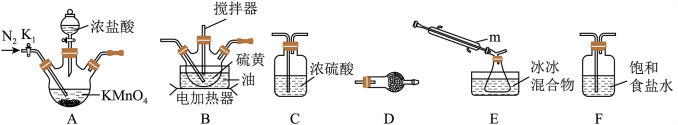
②装置连接顺序:A→
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
④为了提高S2Cl2的纯度,实验的关键是控制好温度和
(2)少量S2Cl2泄漏时应喷水减慢其挥发(或扩散),并产生酸性悬浊液,但不要对泄漏物或泄漏点直接喷水,其原因是
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。
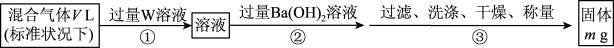
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】水杨酸乙酯常用于配制香料,某小组用水杨酸( )和乙醇合成水杨酸乙酯的原理及实验步骤如下:
)和乙醇合成水杨酸乙酯的原理及实验步骤如下:



Ⅰ.如图,在圆底烧瓶中依次加入 水杨酸、
水杨酸、 乙醇、
乙醇、 环己烷、
环己烷、 浓硫酸,混匀后加入沸石,油水分离器中加水至p处,接通冷凝水,加热三颈烧瓶,在90℃下冷凝回流
浓硫酸,混匀后加入沸石,油水分离器中加水至p处,接通冷凝水,加热三颈烧瓶,在90℃下冷凝回流 ,过程中有机物会回流至三颈烧瓶中,不定期打开油水分离器放出部分水,使水层液面保持在p处附近,直至反应结束,再蒸出多余的环己烷和乙醇。
,过程中有机物会回流至三颈烧瓶中,不定期打开油水分离器放出部分水,使水层液面保持在p处附近,直至反应结束,再蒸出多余的环己烷和乙醇。

Ⅱ.将烧瓶中的残留物转移至分液漏斗,依次用少量水、5% 溶液和水洗涤;分出的产物加入少量无水
溶液和水洗涤;分出的产物加入少量无水 固体,过滤得到粗酯。
固体,过滤得到粗酯。
Ⅲ.将粗酯进行蒸馏,收集233℃~235℃的馏分,得水杨酸乙酯 。
。
已知:环己烷-乙醇-水会形成共沸物(沸点62.6℃)被蒸馏出来。
常用物理常数:
回答下列问题:
(1)步骤Ⅰ的加热方式为_______ ,冷凝水方向为_______ (填“a进b出”或“b进a出”)。
(2)步骤Ⅰ加入环己烷对合成水杨酸乙酯的作用是_______ 。
(3)步骤Ⅰ利用油水分离器判断反应结束的标志是_______ 。
(4)步骤Ⅱ加入 溶液洗去的物质是
溶液洗去的物质是_______ ,无水 的作用是
的作用是_______ 。
(5)步骤Ⅲ进行蒸馏时选用空气冷凝管,如下图,不用直型冷凝管的原因为_______ 。

(6)本实验的产率为_______ 。
 )和乙醇合成水杨酸乙酯的原理及实验步骤如下:
)和乙醇合成水杨酸乙酯的原理及实验步骤如下:



Ⅰ.如图,在圆底烧瓶中依次加入
 水杨酸、
水杨酸、 乙醇、
乙醇、 环己烷、
环己烷、 浓硫酸,混匀后加入沸石,油水分离器中加水至p处,接通冷凝水,加热三颈烧瓶,在90℃下冷凝回流
浓硫酸,混匀后加入沸石,油水分离器中加水至p处,接通冷凝水,加热三颈烧瓶,在90℃下冷凝回流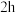 ,过程中有机物会回流至三颈烧瓶中,不定期打开油水分离器放出部分水,使水层液面保持在p处附近,直至反应结束,再蒸出多余的环己烷和乙醇。
,过程中有机物会回流至三颈烧瓶中,不定期打开油水分离器放出部分水,使水层液面保持在p处附近,直至反应结束,再蒸出多余的环己烷和乙醇。
Ⅱ.将烧瓶中的残留物转移至分液漏斗,依次用少量水、5%
 溶液和水洗涤;分出的产物加入少量无水
溶液和水洗涤;分出的产物加入少量无水 固体,过滤得到粗酯。
固体,过滤得到粗酯。Ⅲ.将粗酯进行蒸馏,收集233℃~235℃的馏分,得水杨酸乙酯
 。
。已知:环己烷-乙醇-水会形成共沸物(沸点62.6℃)被蒸馏出来。
常用物理常数:
| 名称 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸乙酯 | 无色液体 | 1.14 | 1.3 | 234 |
| 水杨酸 | 白色晶体 | 1.44 | 158 | 210 |
| 乙醇 | 无色液体 | 0.789 | 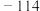 | 78.3 |
(1)步骤Ⅰ的加热方式为
(2)步骤Ⅰ加入环己烷对合成水杨酸乙酯的作用是
(3)步骤Ⅰ利用油水分离器判断反应结束的标志是
(4)步骤Ⅱ加入
 溶液洗去的物质是
溶液洗去的物质是 的作用是
的作用是(5)步骤Ⅲ进行蒸馏时选用空气冷凝管,如下图,不用直型冷凝管的原因为

(6)本实验的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】
(1)装置中有刻度的甲管可以用______________ 代替 (填仪器名称),按图连接好装置后,检查装置气密性的方法是______________________________
(2)某实验小组用镁粉、盐酸、醋酸设计实验来证明:在同温同压下,当上述两种酸的物质的量相同时,与镁粉反应生成氢气的体积相同而反应速率不同。装置如右图所示,
有关实验数据记录于下表:
请回答下列问题:
①每次实验至少需要用电子天平(能称准1 mg) 称取镁粉___________________ g;
②冷却到25℃后,在读取气体体积时,首先应如何操作:__________________________ ;
③分析实验数据,t(a1)远远大于t(b1)的原因是__________________________ 。
(3)用图示装置,某同学设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为mg的镀锌铁皮与6mol·L—1 NaOH溶液反应。回答下列问题:(已知锌的密度为ρ g/cm3)
① 写出Zn镀层与NaOH溶液反应的离子方程式________________________________
②为提高测定的准确性,需将锥形瓶上的单孔橡胶塞换为双孔橡胶塞,另一孔插入______ (填仪器名称)
实验时先向锥形瓶中加入镀锌铁皮样品,塞上双孔塞,再加入NaOH溶液;
③ 已知实验前后甲管中液面读数差为V mL(实验条件的气体摩尔体积为Vmmol·L—1)。则镀锌铁皮的锌镀层厚度为_________________________ cm。(写出数学表达式)

(1)装置中有刻度的甲管可以用
(2)某实验小组用镁粉、盐酸、醋酸设计实验来证明:在同温同压下,当上述两种酸的物质的量相同时,与镁粉反应生成氢气的体积相同而反应速率不同。装置如右图所示,
有关实验数据记录于下表:
| 酸溶液 | 酸溶液 | 气体体积/mL | 反应时间 | |
| (实验A) | (实验B) | (25℃、101 kPa) | 实验A | 实验B |
| CH3COOH 0.1 mol/L 40.00mL | HCl溶液 0.1 mol/L 40.00mL | 5 | t(a1)=155 s | t(b1)=7 s |
| 10 | t(a2)=310 s | t(b2)=16 s | ||
| 15 | t(a3)=465 s | t(b3)=30 s | ||
| 20 | t(a4)=665 s | t(b4)=54 s | ||
| …… | …… | …… | ||
请回答下列问题:
①每次实验至少需要用电子天平(能称准1 mg) 称取镁粉
②冷却到25℃后,在读取气体体积时,首先应如何操作:
③分析实验数据,t(a1)远远大于t(b1)的原因是
(3)用图示装置,某同学设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为mg的镀锌铁皮与6mol·L—1 NaOH溶液反应。回答下列问题:(已知锌的密度为ρ g/cm3)
① 写出Zn镀层与NaOH溶液反应的离子方程式
②为提高测定的准确性,需将锥形瓶上的单孔橡胶塞换为双孔橡胶塞,另一孔插入
实验时先向锥形瓶中加入镀锌铁皮样品,塞上双孔塞,再加入NaOH溶液;
③ 已知实验前后甲管中液面读数差为V mL(实验条件的气体摩尔体积为Vmmol·L—1)。则镀锌铁皮的锌镀层厚度为
您最近一年使用:0次

 2SCl2
2SCl2 

