W、X、Y、Z均为短周期元素,它们可以形成离子化合物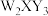 ,W和Y两种元素可以生成
,W和Y两种元素可以生成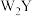 和
和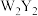 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
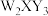 ,W和Y两种元素可以生成
,W和Y两种元素可以生成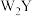 和
和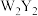 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是A.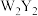 与Z的最高价氧化物反应,生成的产物中存在极性键、非极性键和离子键 与Z的最高价氧化物反应,生成的产物中存在极性键、非极性键和离子键 |
| B.同周期元素中,X的最高价氧化物的水化物酸性最强 |
| C.简单氢化物的稳定性Y大于Z |
D.W、X、Y的原子半径由大到小的顺序是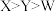 |
更新时间:2024-05-21 22:06:05
|
相似题推荐
多选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知34Se、35Br位于同一周期,根据元素在周期表中的位置,下列说法正确的是( )
| A.离子还原性:Se2->Br- | B.气态氢化物的稳定性:H2S>H2Se |
| C.原子半径:Cl>Br>Se | D.酸性:H2SeO4>HBrO4>HClO4 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.010 mol·L-1的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是
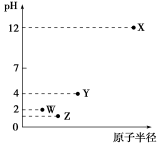

| A.简单离子半径:X>Y>Z>W |
| B.Y元素存在同素异形体 |
| C.气态氢化物的稳定性:W>Z>Y |
| D.X和Y的最高价氧化物对应的水化物恰好中和时,溶液呈中性 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】如表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号,其中J为0族元素。下列说法正确的是
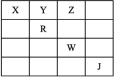

A.R原子的核外电子的轨道表示式为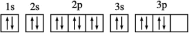 |
| B.Y2−与Na+的半径大小关系为Y2->Na+ |
| C.X的第一电离能小于Y的第一电离能 |
| D.表中电负性最大的元素为Z |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大,X和W位于同一主族,Y的最外层电子数等于Z和W的最外层电子数之和,Y可与Z形成淡黄色化合物Z2Y2。下列说法正确的是
| A.简单离子半径:Z>X>Y |
| B.简单氢化物的沸点:Y>X>W |
| C.元素X的含氧酸均为强酸 |
| D.X与W元素能存在于同一离子化合物中 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】X、Y、Z、W、R属于短周期主族元素,X的原子半径在短周期主族元素中最大,Y元素位于元素周期表的第二周期,Y元素原子的最外层电子数为m,次外层电子数为n,Z元素原子的L层电子数为m+n,M层电子数为m−n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2∶1。下列叙述正确的是
| A.WY2、RY2都属于共价化合物 |
| B.Y的简单气态氢化物比R的简单气态氢化物稳定 |
| C.X与Y形成的两种化合物中阳、阴离子的个数比均为1∶2 |
| D.Z、W、R最高价氧化物对应水化物的酸性由强到弱的顺序是R>Z>W |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】A、B、C为三种短周期元素,A、B在同周期, A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中正确的是
| A.原子序数:A>B>C | B.原子半径:A>B>C |
| C.离子半径:A2->C->B2+ | D.原子核外最外层电子数:A>C>B |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】下列有关H2S和H2O2性质的解释合理的是
| 选项 | 性质 | 解释 |
| A | 常温下,H2O2呈液态,H2S呈气态 | H2O2分子间存在氢键,而H2S分子间不存在氢键 |
| B | 双氧水中存在[H3O2]+ | H2O2中氧有孤电子对,H+有空轨道,能形成配位键 |
| C | H2O2能氧化H2S | H2O2中氧的化合价只能降低 |
| D | H2S溶液中存在S2- | H2S是离子化合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】下列说法中正确的是
| A.完全由非金属元素组成的化合物不一定是共价化合物 |
| B.构成分子晶体的粒子一定含有共价键 |
| C.含有离子键的晶体一定是离子晶体 |
| D.含有共价键的化合物一定是共价化合物 |
您最近一年使用:0次


 溶液,再滴加少量氯水
溶液,再滴加少量氯水

 溶液中加入少量氯水,再加
溶液中加入少量氯水,再加 ,振荡
,振荡
 表示其简单离子
表示其简单离子

