“摩尔盐”[ (NH4)2Fe(SO4)2·6H2O ] 是分析化学中的重要试剂。查阅文献得知:“摩尔盐”隔绝空气加热至500℃时可完全分解,但产物复杂。某学习小组欲探究其分解产物。
Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想__________ 不成立(填序号)。
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置。
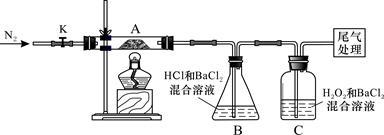
请回答下列问题:
(1)B装置的容器名称是__________ 。
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是______ 。
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀。C中发生反应的离子方程式为_________________________ 。
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是_______________ 。
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中,_________________ 。
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是_______ 。
Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置。

请回答下列问题:
(1)B装置的容器名称是
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀。C中发生反应的离子方程式为
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中,
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是
更新时间:2016-12-09 07:54:25
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】苯乙酮(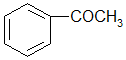 )广泛用于皂用香精和烟草香精中,可由苯和乙酸酐制备。
)广泛用于皂用香精和烟草香精中,可由苯和乙酸酐制备。
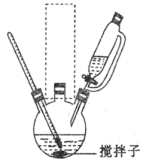
已知:
步骤I:向三颈烧瓶中加入39 g苯和44.5 g无水氯化铝,在搅拌下滴加25.5 g乙酸酐(C4H6O3),在70~80℃下加热45min,发生反应: +(CH3CO)2O
+(CH3CO)2O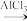
 +CH3COOH。
+CH3COOH。
步骤II:冷却后将反应物倒入100g冰水中,有白色胶状沉淀生成,采用合适的方法处理,水层用苯萃取,合并苯层溶液,再依次用30 mL 5% NaOH溶液和30 mL水洗涤,分离出的苯层用无水硫酸镁干燥。
步骤III:常压蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(1)AlCl3在反应中作___________ ,步骤I中的加热方式为___________ 。
(2)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________ (填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL
(3)图示实验装置虚线框内缺少一种仪器,该仪器名称为___________ 。
(4)步骤II中生成的白色胶状沉淀的化学式为___________ ,该物质易堵塞滤纸,处理白色胶状沉淀的方法为___________ 。
(5)步骤II中用NaOH溶液洗涤的目的是___________ 。
(6)步骤III中收集苯乙酮的温度应为___________ 。
(7)实验中收集到24.0 mL苯乙酮,则苯乙酮的产率为___________ 。
 )广泛用于皂用香精和烟草香精中,可由苯和乙酸酐制备。
)广泛用于皂用香精和烟草香精中,可由苯和乙酸酐制备。
已知:
| 名称 | 熔点/℃ | 沸点/℃ | 密度/(g·mL-1 ) | 溶解性 |
| 苯 | 5.5 | 80.1 | 0.88 | 不溶于水,易溶于有机溶剂 |
| 苯乙酮 | 19.6 | 203 | 1.03 | 微溶于水,易溶于有机溶剂 |
| 乙酸酐 | -73 | 139 | 1.08 | 有吸湿性,易溶于有机溶剂 |
| 乙酸 | 16.6 | 118 | 1.05 | 易溶于水,易溶于有机溶剂 |
 +(CH3CO)2O
+(CH3CO)2O
 +CH3COOH。
+CH3COOH。步骤II:冷却后将反应物倒入100g冰水中,有白色胶状沉淀生成,采用合适的方法处理,水层用苯萃取,合并苯层溶液,再依次用30 mL 5% NaOH溶液和30 mL水洗涤,分离出的苯层用无水硫酸镁干燥。
步骤III:常压蒸馏回收苯,再收集产品苯乙酮。
请回答下列问题:
(1)AlCl3在反应中作
(2)根据上述实验药品的用量,三颈烧瓶的最适宜规格为
A.100 mL B.250 mL C.500 mL D.1000 mL
(3)图示实验装置虚线框内缺少一种仪器,该仪器名称为
(4)步骤II中生成的白色胶状沉淀的化学式为
(5)步骤II中用NaOH溶液洗涤的目的是
(6)步骤III中收集苯乙酮的温度应为
(7)实验中收集到24.0 mL苯乙酮,则苯乙酮的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】三氯乙醛是无色易挥发油状液体,有刺激性气味,易溶于乙醇、乙醚和氯仿,能与水化合生成三氯乙醛水合物,易被 氧化生成
氧化生成 。可用于制造滴滴涕、敌百虫、敌敌畏等杀虫剂、三氯乙醛脲除草剂。医药上用于生产氯霉素、合霉素等。实验室设计如下图所示装置,测定
。可用于制造滴滴涕、敌百虫、敌敌畏等杀虫剂、三氯乙醛脲除草剂。医药上用于生产氯霉素、合霉素等。实验室设计如下图所示装置,测定 样品的质量分数,并用制得的
样品的质量分数,并用制得的 在
在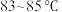 下乙醇制备少量三氯乙醛。
下乙醇制备少量三氯乙醛。_______ ,A中发生反应的化学方程式为_______ 。
(2)装置D、G内所盛试剂的作用为_______ ,导气管a的作用是_______ 。
(3)标准状况下,测定 样品的质量分数时,若实验前后集气管中液面读数分别为
样品的质量分数时,若实验前后集气管中液面读数分别为 、
、 ,则
,则 样品的质量分数的表达式为
样品的质量分数的表达式为_______ (无需化简)。
(4)该实验装置中三通阀的孔路位置如下所示,测定 样品的质量分数时调节为
样品的质量分数时调节为_______ ,制备少量三氯乙醛时三通阀的孔路调节为_______ ,并将水准管向_______ (填“上”或“下”)移动,使 进入右侧装置。
进入右侧装置。_______ ,仪器b中冷凝水下进上出的目的是_______ ,由于实验过程中可能会生成 等杂质,从F中分离出
等杂质,从F中分离出 ,需要进行蒸馏操作,蒸馏时不能选用仪器b的原因是
,需要进行蒸馏操作,蒸馏时不能选用仪器b的原因是_______ 。
(6)装置H的作用是吸收过量的 ,其离子方程式为
,其离子方程式为_______ ,下列装置中能代替装置H的是_______ (错选、漏选均不得分)。
 氧化生成
氧化生成 。可用于制造滴滴涕、敌百虫、敌敌畏等杀虫剂、三氯乙醛脲除草剂。医药上用于生产氯霉素、合霉素等。实验室设计如下图所示装置,测定
。可用于制造滴滴涕、敌百虫、敌敌畏等杀虫剂、三氯乙醛脲除草剂。医药上用于生产氯霉素、合霉素等。实验室设计如下图所示装置,测定 样品的质量分数,并用制得的
样品的质量分数,并用制得的 在
在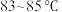 下乙醇制备少量三氯乙醛。
下乙醇制备少量三氯乙醛。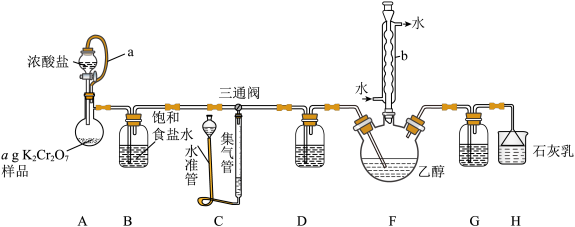
(2)装置D、G内所盛试剂的作用为
(3)标准状况下,测定
 样品的质量分数时,若实验前后集气管中液面读数分别为
样品的质量分数时,若实验前后集气管中液面读数分别为 、
、 ,则
,则 样品的质量分数的表达式为
样品的质量分数的表达式为(4)该实验装置中三通阀的孔路位置如下所示,测定
 样品的质量分数时调节为
样品的质量分数时调节为 进入右侧装置。
进入右侧装置。A. B.
B. C.
C. D.
D.
 等杂质,从F中分离出
等杂质,从F中分离出 ,需要进行蒸馏操作,蒸馏时不能选用仪器b的原因是
,需要进行蒸馏操作,蒸馏时不能选用仪器b的原因是(6)装置H的作用是吸收过量的
 ,其离子方程式为
,其离子方程式为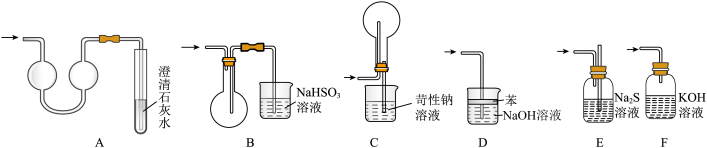
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】亚硝酸钙是白色粉末,易潮解,易溶于水,微溶于乙醇、乙醚。实验室用NO和CaO2 (淡黄色固体)制备无水亚硝酸钙的装置(夹持装置略)如图所示。
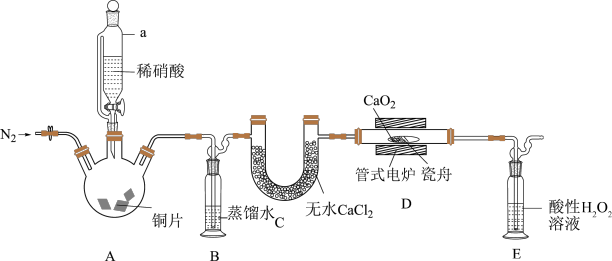
回答下列问题:
(1)实验开始先通N2,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a与普通分液漏斗相比,其优点是___________ 。
(2)装置E中,酸性H2O2溶液可将剩余的NO氧化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(3)CaO2完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②打开止水夹,向装置中通入一段时间N2;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……。则操作②的目的是___________ 。
(4)上述装置存在一处缺陷,会导致亚硝酸钙产率降低,改进的方法是___________ 。
(5)测定所得亚硝酸钙中硝酸钙的含量。
实验原理: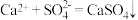 ;
;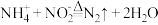
实验步骤: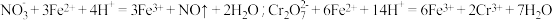
I.准确称取ag所得亚硝酸钙,置于150mL烧杯中,加入100mL蒸馏水和bg足量的硫酸钠,搅拌均匀,将溶液与沉淀全部移入250mL容量瓶,加蒸馏水稀释至刻度,摇匀,过滤;(忽略固体对溶液体积的影响)
Ⅱ.取25.00mL滤液于500mL锥形瓶中,加入足量NH4Cl饱和溶液,煮沸5min;
Ⅲ.冷却后用少量蒸馏水洗涤锥形瓶内壁,再加入25.00mLc₁mol·L-1硫酸亚铁铵[(NH4)2SO4·FeSO4]溶液、在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1:1);
Ⅳ.加4滴指示剂,迅速用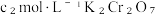 标准液滴定至终点,消耗K2Cr2O7标准液VmL。
标准液滴定至终点,消耗K2Cr2O7标准液VmL。
则所得亚硝酸钙中硝酸钙的质量分数为___________ ;已知在酸性条件下, 可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是
可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是___________ (填标号)。
a.步骤l中,称量时样品发生了潮解
b.步骤Ⅱ中,煮沸时间过短
c.步骤Ⅲ中量取的硫酸亚铁铵溶液的实际体积小于25.00mL
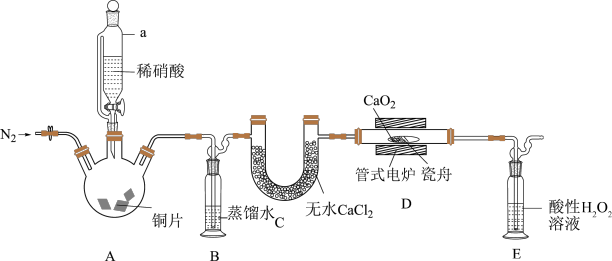
回答下列问题:
(1)实验开始先通N2,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a与普通分液漏斗相比,其优点是
(2)装置E中,酸性H2O2溶液可将剩余的NO氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为(3)CaO2完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②打开止水夹,向装置中通入一段时间N2;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……。则操作②的目的是
(4)上述装置存在一处缺陷,会导致亚硝酸钙产率降低,改进的方法是
(5)测定所得亚硝酸钙中硝酸钙的含量。
实验原理:
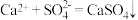 ;
;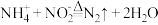
实验步骤:
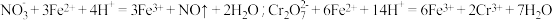
I.准确称取ag所得亚硝酸钙,置于150mL烧杯中,加入100mL蒸馏水和bg足量的硫酸钠,搅拌均匀,将溶液与沉淀全部移入250mL容量瓶,加蒸馏水稀释至刻度,摇匀,过滤;(忽略固体对溶液体积的影响)
Ⅱ.取25.00mL滤液于500mL锥形瓶中,加入足量NH4Cl饱和溶液,煮沸5min;
Ⅲ.冷却后用少量蒸馏水洗涤锥形瓶内壁,再加入25.00mLc₁mol·L-1硫酸亚铁铵[(NH4)2SO4·FeSO4]溶液、在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1:1);
Ⅳ.加4滴指示剂,迅速用
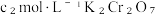 标准液滴定至终点,消耗K2Cr2O7标准液VmL。
标准液滴定至终点,消耗K2Cr2O7标准液VmL。则所得亚硝酸钙中硝酸钙的质量分数为
 可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是
可氧化Fe2+,下列情况会导致硝酸钙的质量分数测量值偏小的是a.步骤l中,称量时样品发生了潮解
b.步骤Ⅱ中,煮沸时间过短
c.步骤Ⅲ中量取的硫酸亚铁铵溶液的实际体积小于25.00mL
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】化学小组探究FeCl3溶液与Na2S溶液的反应产物,利用如图所示的装置进行如下实验: 。
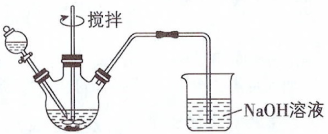
I.向三颈瓶中加入5mL pH=2的FeCl3溶液,滴加一定量pH=12的Na2S溶液,搅拌,能闻到臭鸡蛋气味,产生沉淀A。
II.向三颈瓶中加入5mL pH=12的Na2S溶液,逐滴滴加1~3滴pH=2的FeCl3溶液,搅拌,产生沉淀B。
已知:①FeS2为黑色固体,且不溶于水和盐酸;
②Ksp(Fe2S3)=1.0×10-88,Ksp(FeS2)=6.3×10-31,Ksp[Fe(OH)3]=4.0×10-38,Ksp(FeS)=3.7×10-19
回答下列问题:
(1)有同学预测硫化钠溶液和氯化铁溶液混合后会发生双水解反应,写出该反应的离子方程式:___________
(2) NaOH溶液的作用是___________ ,小组同学猜测,沉淀A、B可能为硫化物或它们的混合物。他们设计如下实验进行探究:
实验一、探究A的成分
取沉淀A于小烧杯中,进行如图所示的实验:
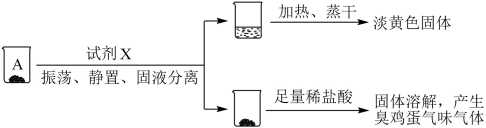
(3)试剂X的化学式是___________ ,由此推断A的成分是___________ (填化学式)。
实验二、探究B的成分
取沉淀B于小烧杯中,进行如图所示的实验:

(4) 向试管a中加入试剂Y,观察到明显现象,证明溶液中存在Fe2+。 试剂Y是___________ ,明显现象是___________ ,由此推断B的成分是___________ (填化学式)。
(5)分析I中实验没有得到Fe(OH)3的原因是___________

I.向三颈瓶中加入5mL pH=2的FeCl3溶液,滴加一定量pH=12的Na2S溶液,搅拌,能闻到臭鸡蛋气味,产生沉淀A。
II.向三颈瓶中加入5mL pH=12的Na2S溶液,逐滴滴加1~3滴pH=2的FeCl3溶液,搅拌,产生沉淀B。
已知:①FeS2为黑色固体,且不溶于水和盐酸;
②Ksp(Fe2S3)=1.0×10-88,Ksp(FeS2)=6.3×10-31,Ksp[Fe(OH)3]=4.0×10-38,Ksp(FeS)=3.7×10-19
回答下列问题:
(1)有同学预测硫化钠溶液和氯化铁溶液混合后会发生双水解反应,写出该反应的离子方程式:
(2) NaOH溶液的作用是
实验一、探究A的成分
取沉淀A于小烧杯中,进行如图所示的实验:

(3)试剂X的化学式是
实验二、探究B的成分
取沉淀B于小烧杯中,进行如图所示的实验:

(4) 向试管a中加入试剂Y,观察到明显现象,证明溶液中存在Fe2+。 试剂Y是
(5)分析I中实验没有得到Fe(OH)3的原因是
您最近一年使用:0次
【推荐2】治理氮氧化物(NOx)的污染是化学研究的重要课题之一。NO能被灼烧的铁粉还原为N2,同时生成同时生成FeO,利用下列装置模拟该反应。

已知:①浓硝酸可氧化NO;②NaOH溶液能与NO2反应,不与NO反应。
(1)上述装置接口的连接顺序为a→__________ (按气流方向,用小写字母表示)。
(2)装置D的作用是___________________ 。
(3)装置E中反应的化学方程式为___________________ 。
(4)打开分液漏斗活塞,烧瓶中观察到的实验现象有_____________________ 。
(5)实验室常用NaOH溶液吸收多余的氮氧化物(NOx):NO+NO2+2NaOH=2NaNO2+H2O。设计实验验证产物NaNO2既有氧化性又有还原性。
限选试剂:稀硫酸、KI-淀粉溶液、双氧水、酸性高锰酸钾溶液
(6)最终得到的亚硝酸钠(NaNO2)外观与食盐非常相似,毒性较强。
已知①Ksp(AgNO2) =2.0×10-8,Ksp(AgCl) =1.8×10-10;
② Ka(HNO2) =5.1×10-4。
若鉴别NaNO2和NaCl两种固体,实验方法是__________________________ (试剂自选)。

已知:①浓硝酸可氧化NO;②NaOH溶液能与NO2反应,不与NO反应。
(1)上述装置接口的连接顺序为a→
(2)装置D的作用是
(3)装置E中反应的化学方程式为
(4)打开分液漏斗活塞,烧瓶中观察到的实验现象有
(5)实验室常用NaOH溶液吸收多余的氮氧化物(NOx):NO+NO2+2NaOH=2NaNO2+H2O。设计实验验证产物NaNO2既有氧化性又有还原性。
限选试剂:稀硫酸、KI-淀粉溶液、双氧水、酸性高锰酸钾溶液
实验步骤 | 实验操作 | 现象 | 实验结论 |
1 | NaNO2具有氧化性 | ||
2 | NaNO2具有还原性 |
已知①Ksp(AgNO2) =2.0×10-8,Ksp(AgCl) =1.8×10-10;
② Ka(HNO2) =5.1×10-4。
若鉴别NaNO2和NaCl两种固体,实验方法是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】I.硫铁矿(主要成分为FeS2杂质为Al2O3、SiO2)是重要的矿产资源,以硫铁矿为原料制备绿矾(FeSO4•7H2O)的工艺流程如图:
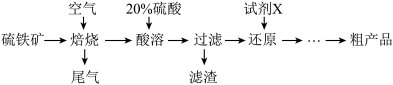
(1)硫铁矿中S元素的价态为______ ,滤渣的成分为______ 。
(2)还原步骤中,加入的试剂X的化学式为______ 。
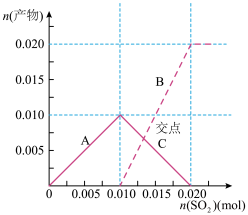
(3)实验室中可用NaOH溶液回收将SO2气体通入到0.100mol•L-1200mLNaOH溶液中,溶液中含硫元素的离子的物质的量与SO2的通入量的关系如图:实线A是______ 的变化曲线,虚线B是______ 的变化曲线(填离子符号)交点C处发生反应的离子方程式为_______ 。
II.硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物和两种非金属氧化物。

组装好仪器(已省略夹持仪器),在一定温度下按上述图示装置进行实验。
(4)组装好实验装置后,要进行的下一步操作是______ ;实验开始时通入氮气的目的是______ 。
(5)B中实验现象证明分解产物中含有______ (写化学式)。依据实验2硬质玻璃管中加热冷却后的固体性质确定分解产物有______ (写化学式)。
(6)某同学欲通过下列实验验证分解产物中含有的另一种非金属氧化物。
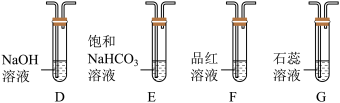
①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→______
②能证明生成了另一种非金属氧化物的现象是______ 。该现象体现了该物质的______ 性。写出该条件下硫酸亚铁受热分解的化学方程式______ 。

(1)硫铁矿中S元素的价态为
(2)还原步骤中,加入的试剂X的化学式为
(3)实验室中可用NaOH溶液回收将SO2气体通入到0.100mol•L-1200mLNaOH溶液中,溶液中含硫元素的离子的物质的量与SO2的通入量的关系如图:实线A是

II.硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物和两种非金属氧化物。

组装好仪器(已省略夹持仪器),在一定温度下按上述图示装置进行实验。
| 序号 | 操作步骤 | 实验现象 |
| 1 | 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | B中产生大量白色沉淀 |
| 2 | A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到红棕色固体物质 |
(5)B中实验现象证明分解产物中含有
(6)某同学欲通过下列实验验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→
②能证明生成了另一种非金属氧化物的现象是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢 )放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是___________________________ 。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用_______ (选填序号)。
a.KSCN溶液和氯水 b.H2O2 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的物质的量为____________ 。分析上述实验中SO2物质的量的结果,丙同学认为气体Y中还可能含有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。

(3)装置B中试剂的作用是____________ 。
(4)认为气体Y中还含有CO2的理由是___________________ (用化学方程式表示)。
(5)为确认CO2的存在,需在装置中添加M于__________ (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是___________________________ 。
(1)将已去除表面氧化物的铁钉(
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用
a.KSCN溶液和氯水 b.H2O2 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的物质的量为

(3)装置B中试剂的作用是
(4)认为气体Y中还含有CO2的理由是
(5)为确认CO2的存在,需在装置中添加M于
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】下图所示装置是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。

(1)若烧瓶中盛装Zn片,分液漏斗中盛装稀H2SO4,则:
①当制备H2、验证H2的还原性并检验H2的氧化产物,仪器连接顺序为:A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是__________ 、__________ (写化学式);D装置的作用是______________ 。
②上述实验中为了使H2产生的速率不至于过快,在不改变现有药品的条件下,可采取的方法有______________ 、______________ 。(要求:写出的两种方法原理不同)
(2)若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3。能产生大量NH3的原因是:
a________________ ;b______________ ;c_____________ 。
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→____ →_____ →_____ (填正确序号的字母)此时在其中的一个装置中可能会出现大量红棕色气体,该装置是_________ (用字母表示);用化学方程式解释红棕色气体产生的原因:_____________ 、_____________ 。

(1)若烧瓶中盛装Zn片,分液漏斗中盛装稀H2SO4,则:
①当制备H2、验证H2的还原性并检验H2的氧化产物,仪器连接顺序为:A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是
②上述实验中为了使H2产生的速率不至于过快,在不改变现有药品的条件下,可采取的方法有
(2)若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3。能产生大量NH3的原因是:
a
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】H2O2是一种绿色试剂,在化学工业中用于生产过氧乙酸、亚氯酸钠等的原料,医药工业用作杀菌剂、消毒剂。某化学小组为探究H2O2的性质做了如下实验:
(1) 下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据。
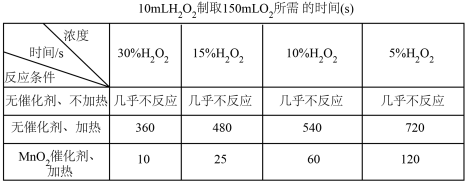
研究小组在设计方案时,考虑了浓度、____ 、____ 因素对过氧化氢分解速率的影响。
(2) 另一研究小组拟在同浓度 Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响。限选试剂与仪器:30% H2O2、0.1 mol·L-1FeCl3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器。设计实验装置,完成图1方框内的装置示意图(要求所测得的数据能直接体现反应速率大小)。________
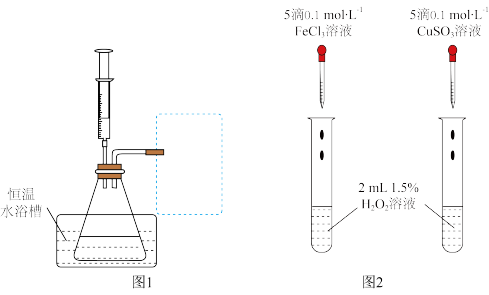
(3) 对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和 Cu2+对H2O2分解的催化效果,研究小组的同学设计了如图2所示的实验。请回答相关问题:
①可通过观察________ ,比较得出结论。
②有同学提出将0.1 mol·L-1FeCl3溶液改为0.05 mol·L-1Fe2(SO4)3更为合理,其理由是___ 。
(4) 已知 FeCl3溶液中主要含有H2O、Fe3+和 Cl-三种微粒,甲同学又做了两种猜想。
猜想 1:真正催化分解H2O2的是FeCl3溶液中的 Fe3+。
猜想 2:真正催化分解H2O2的是____ 。
完成表格验证猜想:
(1) 下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据。

研究小组在设计方案时,考虑了浓度、
(2) 另一研究小组拟在同浓度 Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响。限选试剂与仪器:30% H2O2、0.1 mol·L-1FeCl3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器。设计实验装置,完成图1方框内的装置示意图(要求所测得的数据能直接体现反应速率大小)。

(3) 对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和 Cu2+对H2O2分解的催化效果,研究小组的同学设计了如图2所示的实验。请回答相关问题:
①可通过观察
②有同学提出将0.1 mol·L-1FeCl3溶液改为0.05 mol·L-1Fe2(SO4)3更为合理,其理由是
(4) 已知 FeCl3溶液中主要含有H2O、Fe3+和 Cl-三种微粒,甲同学又做了两种猜想。
猜想 1:真正催化分解H2O2的是FeCl3溶液中的 Fe3+。
猜想 2:真正催化分解H2O2的是
完成表格验证猜想:
| 所需试剂 | 操作及现象 | 结论 |
| Cl-对H2O2分解无催化作用 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】氢化铝钠( )是有机合成中重要的还原剂。实验室以无水四氢呋喃为溶剂,
)是有机合成中重要的还原剂。实验室以无水四氢呋喃为溶剂, 和NaH为反应物,在无水无氧条件下制备
和NaH为反应物,在无水无氧条件下制备 。
。
已知:①二苯甲酮(沸点305℃)作指示剂,在有水体系中无色,在无水体系中呈蓝色。
② 易溶于四氢呋喃(沸点66℃),难溶于甲苯(沸点110.6℃)。
易溶于四氢呋喃(沸点66℃),难溶于甲苯(沸点110.6℃)。
回答下列问题:
(1)制备无水四氢呋喃(装置如图1,夹持及加热装置略)________ 。实验开始,用 排尽装置内的空气;打开活塞K,接通冷凝水并加热装置C至80℃,当观察到
排尽装置内的空气;打开活塞K,接通冷凝水并加热装置C至80℃,当观察到________ ,关闭活塞K,在装置B中收集无水四氢呋喃。
(2)制备 (装置如图2,搅拌、加热和夹持装置略)
(装置如图2,搅拌、加热和夹持装置略) 作催化剂,再加入50mL含4.80gNaH的四氢呋喃悬浊液;接通冷凝水,控温80℃,边搅拌边缓慢滴加50mL含
作催化剂,再加入50mL含4.80gNaH的四氢呋喃悬浊液;接通冷凝水,控温80℃,边搅拌边缓慢滴加50mL含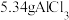 的四氢呋喃溶液,有白色固体析出;静置沉降,取上层清液,经一系列操作得到产品。
的四氢呋喃溶液,有白色固体析出;静置沉降,取上层清液,经一系列操作得到产品。
①制备 的化学方程式为
的化学方程式为________ 。
②图2装置存在的一处缺陷是________ 。
③由上层清液获得 的系列操作:加入甲苯,减压蒸馏→操作a,得粗产品→…→得较纯净的产品。减压蒸馏的馏出物为
的系列操作:加入甲苯,减压蒸馏→操作a,得粗产品→…→得较纯净的产品。减压蒸馏的馏出物为________ ;操作a为________ 。
(3)测定 的产率
的产率
将所得产品用足量无水乙醇、盐酸处理(杂质不反应),加热沸腾分离出 ,冷却后配成100mL溶液。量取5.00mL待测溶液、
,冷却后配成100mL溶液。量取5.00mL待测溶液、 溶液于锥形瓶,调节pH并加热煮沸2min。冷却后用
溶液于锥形瓶,调节pH并加热煮沸2min。冷却后用 醋酸锌标准溶液滴定剩余的EDTA,达终点时消耗标准溶液16.40mL。已知EDTA与
醋酸锌标准溶液滴定剩余的EDTA,达终点时消耗标准溶液16.40mL。已知EDTA与 、
、 均按1:1反应,则
均按1:1反应,则 的产率为
的产率为________ 。若量取EDTA溶液时滴定管尖嘴部分有气泡,放出溶液后气泡消失,则测定结果将________ (填“偏大”、“偏小”或“不变”)。
 )是有机合成中重要的还原剂。实验室以无水四氢呋喃为溶剂,
)是有机合成中重要的还原剂。实验室以无水四氢呋喃为溶剂, 和NaH为反应物,在无水无氧条件下制备
和NaH为反应物,在无水无氧条件下制备 。
。已知:①二苯甲酮(沸点305℃)作指示剂,在有水体系中无色,在无水体系中呈蓝色。
②
 易溶于四氢呋喃(沸点66℃),难溶于甲苯(沸点110.6℃)。
易溶于四氢呋喃(沸点66℃),难溶于甲苯(沸点110.6℃)。回答下列问题:
(1)制备无水四氢呋喃(装置如图1,夹持及加热装置略)
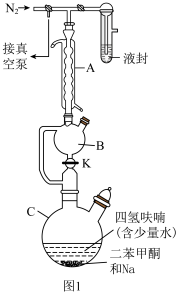
 排尽装置内的空气;打开活塞K,接通冷凝水并加热装置C至80℃,当观察到
排尽装置内的空气;打开活塞K,接通冷凝水并加热装置C至80℃,当观察到(2)制备
 (装置如图2,搅拌、加热和夹持装置略)
(装置如图2,搅拌、加热和夹持装置略)
 作催化剂,再加入50mL含4.80gNaH的四氢呋喃悬浊液;接通冷凝水,控温80℃,边搅拌边缓慢滴加50mL含
作催化剂,再加入50mL含4.80gNaH的四氢呋喃悬浊液;接通冷凝水,控温80℃,边搅拌边缓慢滴加50mL含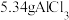 的四氢呋喃溶液,有白色固体析出;静置沉降,取上层清液,经一系列操作得到产品。
的四氢呋喃溶液,有白色固体析出;静置沉降,取上层清液,经一系列操作得到产品。①制备
 的化学方程式为
的化学方程式为②图2装置存在的一处缺陷是
③由上层清液获得
 的系列操作:加入甲苯,减压蒸馏→操作a,得粗产品→…→得较纯净的产品。减压蒸馏的馏出物为
的系列操作:加入甲苯,减压蒸馏→操作a,得粗产品→…→得较纯净的产品。减压蒸馏的馏出物为(3)测定
 的产率
的产率将所得产品用足量无水乙醇、盐酸处理(杂质不反应),加热沸腾分离出
 ,冷却后配成100mL溶液。量取5.00mL待测溶液、
,冷却后配成100mL溶液。量取5.00mL待测溶液、 溶液于锥形瓶,调节pH并加热煮沸2min。冷却后用
溶液于锥形瓶,调节pH并加热煮沸2min。冷却后用 醋酸锌标准溶液滴定剩余的EDTA,达终点时消耗标准溶液16.40mL。已知EDTA与
醋酸锌标准溶液滴定剩余的EDTA,达终点时消耗标准溶液16.40mL。已知EDTA与 、
、 均按1:1反应,则
均按1:1反应,则 的产率为
的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】实验室用工业铬酸钠(Na2CrO4)为原料制备氯化铬晶体(CrCl3•6H2O)的主要步骤如下:

Ⅰ.将1mol工业铬酸钠、1mol甲醇、400mL水依次加入三颈烧瓶中。
Ⅱ.升温至120℃时,打开仪器a活塞缓慢滴加足量盐酸,保持温度在100℃反应3h,反应生成CO2。
Ⅲ.待反应液冷却后,用NaOH(aq)调节pH,得到Cr(OH)3沉淀。
Ⅳ.将过滤后所得固体完全溶解于过量的盐酸中,蒸发浓缩、冷却结晶、过滤、多次洗涤沉淀,低温干燥,得到CrCl3•6H2O。
(1)仪器a的名称是______ ;仪器b的冷凝水从______ 进水(选填“A:上口”或“B:下口”)。
(2)写出步骤Ⅱ的离子方程式:______ 。
(3)已知常温下Ksp[Cr(OH)3]≈1×10-32,步骤Ⅲ中,为使Cr3+沉淀完全,调节溶液pH的最小值是_____ (保留两位有效数字)。
测定产品中CrCl3•6H2O(M=266.5g•mol-1)纯度。称取产品0.2665g,加水溶解并定容于250mL容量瓶中,移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸腾后加入稍过量的Na2O2,充分加热煮沸,适当稀释,加稀酸酸化,使Cr3+完全转化为Cr2O ,再加入足量KI,加塞,摇匀,于暗处静置5min后,加入指示剂,用0.0100mol•L-1Na2S2O3(aq)滴定至终点,平行测定三次,平均消耗Na2S2O3(aq)21.00mL。
,再加入足量KI,加塞,摇匀,于暗处静置5min后,加入指示剂,用0.0100mol•L-1Na2S2O3(aq)滴定至终点,平行测定三次,平均消耗Na2S2O3(aq)21.00mL。
已知:Cr2O +6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
(4)加入稍过量的Na2O2后,充分加热煮沸的目的是______ 。若缺少此操作测定结果会_____ (选填“A:偏大”或“B:偏小”)。加稀酸酸化,使用的是______ (选填“A:硫酸”或“B:盐酸”)。滴定使用的指示剂是______ 。
(5)产品中CrCl3•6H2O的质量分数为_____ (保留两位有效数字)。
(6)CrCl3•6H2O有三种结构,分别呈紫罗兰色、暗绿色和亮绿色。在三种化合物中,Cr3+的配位数均为6,等物质的量的三种化合物分别与足量AgNO3(aq)充分反应,生成的AgCl沉淀的物质的量之比为3:2:1,则呈亮绿色的配合物内界离子的化学式为______ 。
(7)CrCl3、CrF3的熔点分别是83℃和1100℃,两者熔点差异大的原因是______ 。
已知:
I2(Cr)>I2(Mn)的原因是______ 。

Ⅰ.将1mol工业铬酸钠、1mol甲醇、400mL水依次加入三颈烧瓶中。
Ⅱ.升温至120℃时,打开仪器a活塞缓慢滴加足量盐酸,保持温度在100℃反应3h,反应生成CO2。
Ⅲ.待反应液冷却后,用NaOH(aq)调节pH,得到Cr(OH)3沉淀。
Ⅳ.将过滤后所得固体完全溶解于过量的盐酸中,蒸发浓缩、冷却结晶、过滤、多次洗涤沉淀,低温干燥,得到CrCl3•6H2O。
(1)仪器a的名称是
(2)写出步骤Ⅱ的离子方程式:
(3)已知常温下Ksp[Cr(OH)3]≈1×10-32,步骤Ⅲ中,为使Cr3+沉淀完全,调节溶液pH的最小值是
测定产品中CrCl3•6H2O(M=266.5g•mol-1)纯度。称取产品0.2665g,加水溶解并定容于250mL容量瓶中,移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸腾后加入稍过量的Na2O2,充分加热煮沸,适当稀释,加稀酸酸化,使Cr3+完全转化为Cr2O
 ,再加入足量KI,加塞,摇匀,于暗处静置5min后,加入指示剂,用0.0100mol•L-1Na2S2O3(aq)滴定至终点,平行测定三次,平均消耗Na2S2O3(aq)21.00mL。
,再加入足量KI,加塞,摇匀,于暗处静置5min后,加入指示剂,用0.0100mol•L-1Na2S2O3(aq)滴定至终点,平行测定三次,平均消耗Na2S2O3(aq)21.00mL。已知:Cr2O
 +6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。(4)加入稍过量的Na2O2后,充分加热煮沸的目的是
(5)产品中CrCl3•6H2O的质量分数为
(6)CrCl3•6H2O有三种结构,分别呈紫罗兰色、暗绿色和亮绿色。在三种化合物中,Cr3+的配位数均为6,等物质的量的三种化合物分别与足量AgNO3(aq)充分反应,生成的AgCl沉淀的物质的量之比为3:2:1,则呈亮绿色的配合物内界离子的化学式为
(7)CrCl3、CrF3的熔点分别是83℃和1100℃,两者熔点差异大的原因是
已知:
| 元素 | 第二电离能I2/kJ•mol-1 |
| Cr | 1590.6 |
| Mn | 1509.0 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】氯化亚砜(SOCl2)具有较强的巯基和羟基取代能力,广泛应用于有机合成中。工业上可以利用SO3与SCl2反应制得,装置如下图所示(夹持及加热装置已略去):

物质的相关性质如下表:
已知:H2SO4(浓) SO3+H2O;SCl2与SOCl2互溶。
SO3+H2O;SCl2与SOCl2互溶。
实验步骤如下:
①通入干燥的氮气(能够抑制三氧化硫气体逸出),观察A中气泡控制N2的流速;
②将P2O5固体置于烧瓶B中,向B中分多次缓慢加入5.44mL浓硫酸(密度为1.84g· cm-3,质量分数为98%),再向C中加入足量SCl2;
③冷凝管接入冷凝水后将烧瓶B升温至225℃,三氧化硫液体缓慢流入锥形瓶C中;
④反应完成后取下锥形瓶C,……(操作),得到高纯SOCl2产物。
回答下列问题:
(1)仪器a的名称为_______ ,锥形瓶C中生成氯化亚砜的方程式为_______ 。
(2)该制备SOCl2装置存在的缺陷为_______ 。
(3)实验步骤④中的操作为_______ (填名称)。
(4)将得到的SOCl2溶于水生成两种酸,反应的离子方程式为_______ ,取所得溶液体积的十分之一用0.5mol·L-1标准碘溶液滴定,选用_______ 做指示剂,滴定终点消耗标准碘溶液的体积为13.00mL,则SOCl2的产率为_______ ,若滴定后,滴定管尖嘴处有气泡,则测定结果_______ (填“偏高”“偏低”或“不变”)。

物质的相关性质如下表:
| 物质 | SO3 | SCl2 | SOCl2 |
| 熔点/℃ | 16.8 | -78 | -105 |
| 沸点/℃ | 44.8 | 60 | 78.8 |
| 与水反应 | 均能与水剧烈反应 | ||
 SO3+H2O;SCl2与SOCl2互溶。
SO3+H2O;SCl2与SOCl2互溶。实验步骤如下:
①通入干燥的氮气(能够抑制三氧化硫气体逸出),观察A中气泡控制N2的流速;
②将P2O5固体置于烧瓶B中,向B中分多次缓慢加入5.44mL浓硫酸(密度为1.84g· cm-3,质量分数为98%),再向C中加入足量SCl2;
③冷凝管接入冷凝水后将烧瓶B升温至225℃,三氧化硫液体缓慢流入锥形瓶C中;
④反应完成后取下锥形瓶C,……(操作),得到高纯SOCl2产物。
回答下列问题:
(1)仪器a的名称为
(2)该制备SOCl2装置存在的缺陷为
(3)实验步骤④中的操作为
(4)将得到的SOCl2溶于水生成两种酸,反应的离子方程式为
您最近一年使用:0次



