现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4 = Na+ + H+ + SO42- 。
根据实验现象,回答下列问题:
(1)A为 ,C为 。
(2)写出下列反应的离子方程式
A + B ,A + D ,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为 ,反应后得到的溶液中含有的阴离子有 。
(4)上述没有明显变化的实验④、⑥,其中 发生了离子反应,离子方程式为 。请设计实验证明其发生了反应 。(试剂任选)
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A + B | 生成白色沉淀 |
| ② | A + C | 放出无色气体 |
| ③ | A + D | 放出无色气体 |
| ④ | B + C | 无明显变化 |
| ⑤ | B + D | 生成白色沉淀 |
| ⑥ | C + D | 无明显变化 |
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4 = Na+ + H+ + SO42- 。
根据实验现象,回答下列问题:
(1)A为 ,C为 。
(2)写出下列反应的离子方程式
A + B ,A + D ,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为 ,反应后得到的溶液中含有的阴离子有 。
(4)上述没有明显变化的实验④、⑥,其中 发生了离子反应,离子方程式为 。请设计实验证明其发生了反应 。(试剂任选)
更新时间:2016-12-09 00:57:16
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)根据下列实验现象或要求写离子方程式(描述现象的,需要写出所有涉及的离子方程式。)
(2)某无色溶液,其中有可能存在的离子如下Na+、Ag+、Ba2+、Al3+、AlO 、S2-、CO
、S2-、CO 、SO
、SO 、SO
、SO ,现取该溶液进行有关实验,实验结果如图所示:
,现取该溶液进行有关实验,实验结果如图所示:

①沉淀甲是___________ ,生成沉淀的离子方程式___________ ;
②沉淀乙是___________ ,由溶液甲生成沉淀乙的离子方程式___________ ;
③沉淀丙是___________ ,设计实验证明___________ ;
④综合上述信息,可以肯定存在的离子有___________ 。
| 实验现象 | 离子方程式 |
| ①澄清石灰水中通入CO2出现白色沉淀,继续通,沉淀溶解。 | |
| ②湿法制备高铁酸钾(K2FeO4)的过程为,在氢氧化铁固体中加入KClO和KOH的混合液。写出该过程的离子方程式并配平。 |
(2)某无色溶液,其中有可能存在的离子如下Na+、Ag+、Ba2+、Al3+、AlO
 、S2-、CO
、S2-、CO 、SO
、SO 、SO
、SO ,现取该溶液进行有关实验,实验结果如图所示:
,现取该溶液进行有关实验,实验结果如图所示:
①沉淀甲是
②沉淀乙是
③沉淀丙是
④综合上述信息,可以肯定存在的离子有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知水在25℃和100℃时的电离平衡曲线如图所示:

(1)25℃时水的电离平衡曲线应为_______ (填“A”或“B”)。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为_______ 。
(3)25℃时,等体积的pH=12的NaOH和氨水溶液与0.1mol/L的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积分别为Va、Vb,则Va_______ Vb(填大于、小于、等于)。
(4)t℃时,由水电离出H+的浓度为10-11mol/L,则该溶液中一定能大量共存的是_______。

(1)25℃时水的电离平衡曲线应为
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为
(3)25℃时,等体积的pH=12的NaOH和氨水溶液与0.1mol/L的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积分别为Va、Vb,则Va
(4)t℃时,由水电离出H+的浓度为10-11mol/L,则该溶液中一定能大量共存的是_______。
A.K+、Cu2+、SO 、S2- 、S2- | B.H+、Fe2+、SO 、NO 、NO |
C.Na+、SO 、NO 、NO 、Cl- 、Cl- | D.OH-、NH 、HCO 、HCO 、Na+ 、Na+ |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某无色透明溶液里加入铝粉可放出氢气,试分析下列离子: H+、Ba2+、Fe3+、OH-、SO 、Cl-、CO
、Cl-、CO 中可能有哪些离子存在于该溶液中:
中可能有哪些离子存在于该溶液中:
第一种情况:若溶液呈碱性,可能大量存在的离子是_______ 。
第二种情况:若溶液呈酸性,可能大量存在的离子是_______ 。
 、Cl-、CO
、Cl-、CO 中可能有哪些离子存在于该溶液中:
中可能有哪些离子存在于该溶液中:第一种情况:若溶液呈碱性,可能大量存在的离子是
第二种情况:若溶液呈酸性,可能大量存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
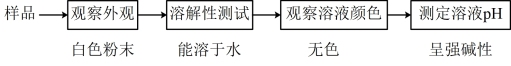
【推荐2】有一份样品,可能是下列物质中的一种或几种:CuSO4、BaSO4、FeCl3、KOH、NaCl、CaCO3。对该样品进行初步测试后,得出如图所示的结果。分析该白色粉末是什么物质。说一说你的理由_______ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A和B两支试管的溶液中共含有K+、Ag+、Mg2+、Cl﹣、OH﹣、NO3﹣六种离子,向试管A的溶液中滴入酚酞试液呈红色.请回答下列问题:
(1)试管A的溶液中所含上述离子共有____ 种.
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为_____ (填“A”或“B”).
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是_____ (填化学式).
(4)若向由试管A的溶液中阳离子组成的硫酸氢盐溶液中,滴入 Ba(OH)2溶液至溶液显中性,则发生反应的离子方程式为___________________________ .
(1)试管A的溶液中所含上述离子共有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若向由试管A的溶液中阳离子组成的硫酸氢盐溶液中,滴入 Ba(OH)2溶液至溶液显中性,则发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对一份稀溶液作初步分析发现,溶液无色、澄清,其中可能含有SO42-、Na+、CO32-、Cl﹣、Ca2+等离子中的若干种。然后又做了如下实验,以确认这些离子是否大量存在。
①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
②在实验①的溶液中再加入硝酸银溶液,结果又生成了不溶于稀硝酸的白色沉淀。
③用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色。
问:
(1)上述实验可以确定溶液中一定含有_____ ,一定没有_____ 。
(2)从以上操作中,不能判断是否存在的离子是_____ ,为了检验该离子是否存在,请你写出进一步检验的操作步骤和实验现象:_____ 。
(3)有同学认为实验③可以省略,你认为呢?_____ (填“可以”或“不可以”),并说明理由_____ 。
①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
②在实验①的溶液中再加入硝酸银溶液,结果又生成了不溶于稀硝酸的白色沉淀。
③用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色。
问:
(1)上述实验可以确定溶液中一定含有
(2)从以上操作中,不能判断是否存在的离子是
(3)有同学认为实验③可以省略,你认为呢?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】学校化学研究小组对某溶液进行检测分析,该无色溶液中可能含有H+、NH 、K+、Al3+、HCO
、K+、Al3+、HCO 、Cl﹣、Cu2+、SO
、Cl﹣、Cu2+、SO 等离子中的几种离子。
等离子中的几种离子。
①经实验检测可知溶液明显呈酸性。
②取该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生。
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解。
请回答:
(1)该溶液中一定不存在的离子有_____ (填离子符号,下同),一定存在的离子有_____
(2)写出②中发生反应的离子方程式:_____
(3)分别写出③中产生气体丙和沉淀乙溶解所发生反应的离子方程式_____
(4)该溶液中不能确定是否含有的离子是_____ ,可通过_____ 实验来进一步确定该离子。
 、K+、Al3+、HCO
、K+、Al3+、HCO 、Cl﹣、Cu2+、SO
、Cl﹣、Cu2+、SO 等离子中的几种离子。
等离子中的几种离子。①经实验检测可知溶液明显呈酸性。
②取该溶液于试管中滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到白色沉淀甲,向滤液中加入AgNO3溶液未见沉淀产生。
③另取少量该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当沉淀增加到一定量后开始产生气体丙,最后沉淀完全溶解。
请回答:
(1)该溶液中一定不存在的离子有
(2)写出②中发生反应的离子方程式:
(3)分别写出③中产生气体丙和沉淀乙溶解所发生反应的离子方程式
(4)该溶液中不能确定是否含有的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是______ 价。CrO2-是一种酸根离子,则Fe(CrO2)2属于________ (填“酸”“碱”“盐”或“氧化物”)。
(2)区分明胶的水溶液和K2SO4溶液的方法是_________ 。分离提纯明胶的水溶液和K2SO4溶液的混合物方法是______________ 。
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明SO42-能够透过半透膜:_____________________ 。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(2)区分明胶的水溶液和K2SO4溶液的方法是
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明SO42-能够透过半透膜:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题。
(1)向CuCl2溶液中滴加NaOH溶液,现象:_______ ,离子方程式:_______ 。
(2)向Ba(OH)2溶液中加入稀硫酸,现象:_______ ,离子方程式:_______ 。
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:
①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关反应的离子方程式为_______ 。
③通过以上叙述可知溶液中肯定不存在的离子是_______ ,可能存在的离子是_______ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向Ba(OH)2溶液中加入稀硫酸,现象:
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO
 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
③通过以上叙述可知溶液中肯定不存在的离子是
您最近一年使用:0次

 、
、 、OH−、Cl−。
、OH−、Cl−。 且有金属铝剩余时,一定存在的离子是
且有金属铝剩余时,一定存在的离子是 、Cl-、CO
、Cl-、CO 中的某一种。
中的某一种。

