25℃时,水的电离达到平衡:H2O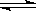 H++OH;ΔH>0,下列叙述正确的是
H++OH;ΔH>0,下列叙述正确的是
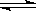 H++OH;ΔH>0,下列叙述正确的是
H++OH;ΔH>0,下列叙述正确的是| A.向水中加入稀氨水,平衡逆向移动,c(OH―)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量稀硫酸,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
更新时间:2016-12-09 09:02:23
|
【知识点】 水的电离
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,有下列四种溶液:
下列说法正确的是( )
| ① | ② | ③ | ④ |
| 0.1 mol·L-1NaOH溶液 | pH=11 NaOH溶液 | 0.1mol·L-1CH3COOH溶液 | pH=3 CH3COOH溶液 |
| A.由水电离出的c(H+):①>③ |
| B.③稀释到原来的100倍后,pH与④相同 |
| C.②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用0.10mo/LNaOH溶液滴定20.0mL0.10mo/LH2A溶液,溶液pH和温度随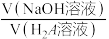 的变化曲线如图所示(忽略溶液混合时体积的变化)。下列说法正确的
的变化曲线如图所示(忽略溶液混合时体积的变化)。下列说法正确的

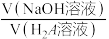 的变化曲线如图所示(忽略溶液混合时体积的变化)。下列说法正确的
的变化曲线如图所示(忽略溶液混合时体积的变化)。下列说法正确的
| A.25℃,H2A的电离常数Ka2=10-9.7 |
| B.从W至Z点,水的电离程度逐渐增大,Kw不变 |
C.当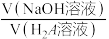 =1.5时,3c(Na+)=2c(H2A)+2c(HA-)+2c(A2-) =1.5时,3c(Na+)=2c(H2A)+2c(HA-)+2c(A2-) |
| D.在X点时,c(OH-)-c(H+)=0.05mol/L-c(HA-)-2c(A2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】甘油硼酸是一种一元有机弱酸,可简写为HM。常温下,向20 mL 0.2 mol·L-1HM溶液中逐滴加入浓度为0.2 mol·L-1的NaOH溶液,溶液中 、pH、中和率(中和率=
、pH、中和率(中和率= )的变化如图所示。
)的变化如图所示。

下列说法正确的是
 、pH、中和率(中和率=
、pH、中和率(中和率= )的变化如图所示。
)的变化如图所示。
下列说法正确的是
| A.HM的电离常数数量级为10-5 |
| B.a点时,c(HM)+c(M- )= 2c(Na+ ) |
| C.b点时,c(M- )>c(Na +)>c(H+ )>c(OH- ) |
| D.溶液中水的电离程度: c点<b点 |
您最近一年使用:0次



