某化学课外活动小组以海带为原料获得少量碘水,并以四氯化碳(沸点76.80C)为溶剂将碘从碘水中提取出来,具体过程如图所示。
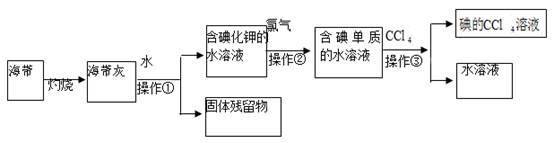
请回答下列问题:
(1)操作①的名称为________________ 、_________________ ;
(2)向含碘单质的水溶液中加入CCl4振荡、静置后,观察到的现象是______________________ ;
(3)操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是_______________________ 。
(4)从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶、牛角管外,还需要____________________ ,实验中温度计水银球所处位置为___________ 。

请回答下列问题:
(1)操作①的名称为
(2)向含碘单质的水溶液中加入CCl4振荡、静置后,观察到的现象是
(3)操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是
(4)从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶、牛角管外,还需要
更新时间:2015-12-03 11:24:53
|
相似题推荐
【推荐1】有机物M(只含C、H、O三种元素中的两种或三种)具有令人愉悦的牛奶香气,主要用于配制奶油、乳品、酸奶和草莓等型香精,是我国批准使用的香料产品,其沸点为 。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图所示,仪器a的名称是_______ ,图中虚线框内应选用右侧的_______ (填“仪器x”或“仪器y”)。

步骤二:确定M的实验式和分子式。
(2)利用李比希法测得4.4g有机物M完全燃烧后产生CO2 8.8g和H2O 3.6g。
①M的实验式为_______ 。
②已知M的密度是同温同压下二氧化碳密度的2倍,则M的相对分子质量为_______ ,分子式为_______ 。
步骤三:确定M的结构简式。
(3)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示。

M中官能团的名称为_______ ,M的结构简式为_______ (填键线式)。
(4)写出两种含有酯基的M的同分异构体的结构简式:_______ 。
 。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图所示,仪器a的名称是

步骤二:确定M的实验式和分子式。
(2)利用李比希法测得4.4g有机物M完全燃烧后产生CO2 8.8g和H2O 3.6g。
①M的实验式为
②已知M的密度是同温同压下二氧化碳密度的2倍,则M的相对分子质量为
步骤三:确定M的结构简式。
(3)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示。

M中官能团的名称为
(4)写出两种含有酯基的M的同分异构体的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)下列实验装置一般用于什么实验操作(填实验操作名称)
A______________ B______________ C____________
A.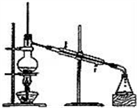 B.
B.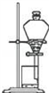 C.
C.
(2) 在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
①CO的质量为________ ②混合气体的平均摩尔质量为________
③CO2的体积为________ ④混合气体的密度为_____ (小数点后保留1位)
A
A.
 B.
B. C.
C.
(2) 在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4 g。
①CO的质量为
③CO2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.无机化合物可根据其组成和性质进行分类。

(1)如图所示的物质分类方法名称是_______ 。
(2)在 Ca、H、O、N 四种元素中任意选择三种元素组成合适的物质,将其化学式分别填在①、②后面的横线上①_______ ,②________ 。
(3)写出向澄清石灰水中通入少量④反应的离子方程式:_______ 。
(4)在盛有 FeCl3溶液的烧杯中,加入氢氧化钠溶液反应后,得到的分散系类别是_______ ;向 Fe(OH)3胶体中逐滴滴入过量的稀硫酸,可观察到的现象是_______ ;
II.选择合适的实验方法完成下列操作(填字母):
A.蒸馏 B.分液 C.升华 D.过滤 E.蒸发结晶 F.溶解、过滤 (洗涤、干燥)、蒸发结晶 G.溶解、蒸发浓缩、冷却结晶、过滤(洗涤、干燥)
(5)分离KCl和MnO2的混合物_______ 。
(6)除去KNO3固体中少量的KCl_______ 。
(7)从碘和氯化钠的混合物中提取碘_______ 。
(8)从NaCl水溶液中提取NaCl固体_______ 。
(9)从海水中得到淡水_______ 。
(10)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)_______ 。

(1)如图所示的物质分类方法名称是
(2)在 Ca、H、O、N 四种元素中任意选择三种元素组成合适的物质,将其化学式分别填在①、②后面的横线上①
(3)写出向澄清石灰水中通入少量④反应的离子方程式:
(4)在盛有 FeCl3溶液的烧杯中,加入氢氧化钠溶液反应后,得到的分散系类别是
II.选择合适的实验方法完成下列操作(填字母):
A.蒸馏 B.分液 C.升华 D.过滤 E.蒸发结晶 F.溶解、过滤 (洗涤、干燥)、蒸发结晶 G.溶解、蒸发浓缩、冷却结晶、过滤(洗涤、干燥)
(5)分离KCl和MnO2的混合物
(6)除去KNO3固体中少量的KCl
(7)从碘和氯化钠的混合物中提取碘
(8)从NaCl水溶液中提取NaCl固体
(9)从海水中得到淡水
(10)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)
您最近一年使用:0次
【推荐1】现有直馏汽油和裂化汽油各一瓶。已知:裂化汽油主要成分为烷烃、烯烃,直馏汽油主要成分为烷烃、环烷烃、芳香烃。
(1)请从下列试剂中选择最合理的试剂区别上述两种汽油。所选试剂是_______ (填字母)。
A.酸性 溶液 B.乙醇 C.溴水
溶液 B.乙醇 C.溴水
(2)加入所选试剂后,直馏汽油中观察到的现象是_______ ;裂化汽油中观察到的现象是_______ 。
(1)请从下列试剂中选择最合理的试剂区别上述两种汽油。所选试剂是
A.酸性
 溶液 B.乙醇 C.溴水
溶液 B.乙醇 C.溴水(2)加入所选试剂后,直馏汽油中观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】将代表下列各分离物质方法的字母,填在相应的位置上:
A.过滤法;B.降温结晶法;C.分液法;D.萃取法;E.蒸发法;F.蒸馏法
(1)提取碘水中的碘___ ;
(2)除去植物油中的水___ ;
(3)将溶液中的大量硝酸钾与少量氯化钠分离___ ;
(4)除去乙醇中溶解的微量食盐可采用___ 。
A.过滤法;B.降温结晶法;C.分液法;D.萃取法;E.蒸发法;F.蒸馏法
(1)提取碘水中的碘
(2)除去植物油中的水
(3)将溶液中的大量硝酸钾与少量氯化钠分离
(4)除去乙醇中溶解的微量食盐可采用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】教材中有两个关于混合物分离的实验,请回答下列有关问题
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示
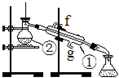
(1)写出下列仪器的名称:①___________ ②_____________
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是______________ ,将仪器补充完整后进行的实验操作的名称是______________ ;①的进水口是__________ (填“f”或“g”)
(3)仪器②中常加入碎瓷片,这样做的目的是___________________
实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液.
其实验操作中有如下两步:
①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔.
②静置分层后,旋开活塞,用烧杯接收下层液体
(4)下层流出的是_____________ 溶液,上层液体从_________________ 得到(填“上口”或“下口”)
(5)萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是( )
A.不与碘反应
B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同
D.可以选用CCl4、 酒精做萃取剂.
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示

(1)写出下列仪器的名称:①
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是
(3)仪器②中常加入碎瓷片,这样做的目的是
实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液.
其实验操作中有如下两步:
①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔.
②静置分层后,旋开活塞,用烧杯接收下层液体
(4)下层流出的是
(5)萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是
A.不与碘反应
B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同
D.可以选用CCl4、 酒精做萃取剂.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用所给的工艺流程生产单质碘:
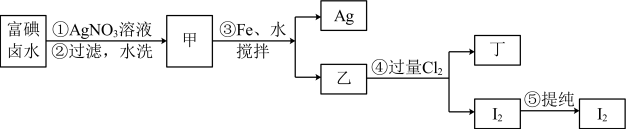
(1)碘位于元素周期表中的第___________ 周期第___________ 族。
(2)步骤③加Fe的目的是___________
(3)写出步骤④的化学方程式:___________ 。
(4)上述生产流程中,可以循环利用的副产物是,已知上述流程得到的该副产物含杂质,现需将其制成生产所需的试剂,先后还需加入___________ 、___________ 来进行处理。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)___________ 。
(6)第⑤步操作可供提纯I2的两种方法是和___________ 、___________ 。

(1)碘位于元素周期表中的第
(2)步骤③加Fe的目的是
(3)写出步骤④的化学方程式:
(4)上述生产流程中,可以循环利用的副产物是,已知上述流程得到的该副产物含杂质,现需将其制成生产所需的试剂,先后还需加入
(5)甲物质见光易变黑,其原因是(用化学方程式表示)
(6)第⑤步操作可供提纯I2的两种方法是和
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】海洋资源的利用具有广阔前景。
(1)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是____ 。
(2)如图是从海水中提取镁的简单流程。
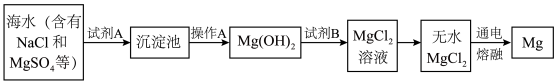
①工业上常用于沉淀Mg2+的试剂A是____ ,操作A的名称是____ 。
②由无水MgCl2制取Mg的化学方程式是____ 。
(3)海带灰中富含以I-形式存在的碘元素。从海带中提取I2的过程如图所示:

①灼烧海带时不需用到下列仪器中的____ (填字母序号)。
a.漏斗 b.酒精灯 c.坩埚 d.泥三角
②向滤液中加入稀硫酸和过氧化氢溶液进行反应,写出该反应的离子方程式____ 。
(1)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
(2)如图是从海水中提取镁的简单流程。

①工业上常用于沉淀Mg2+的试剂A是
②由无水MgCl2制取Mg的化学方程式是
(3)海带灰中富含以I-形式存在的碘元素。从海带中提取I2的过程如图所示:

①灼烧海带时不需用到下列仪器中的
a.漏斗 b.酒精灯 c.坩埚 d.泥三角
②向滤液中加入稀硫酸和过氧化氢溶液进行反应,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ. 过氧化物是一类非常重要的化合物,从人们制得第一种过氧化物距今已有200多年的历史了,在众多的过氧化物中过氧化氢迄今为止仍然得到广泛的应用。
(1)与H2O2具有相同的电子总数的双原子分子有_______________ (写两种);
(2)若从海水中提取碘,需将碘化物变成单质碘。写出在酸性条件下H2O2氧化I—离子的离子方程式__________________________________________ ;
(3)Na2O2、K2O2、CaO2和BaO2都能与酸作用生成H2O2,目前实验室制取H2O2可通过上述某种过氧化物与适量的稀H2SO4作用并过滤后获得,其中最适合的过氧化物是________________ (填化学式);
Ⅱ. 葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是____________ 。
(2)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水。为研究E的组成与结构,通过实验得到如下信息:
①有机物E的相对分子量为90。9.0g E完全燃烧时,生成CO2 0.3mol, H2O 5.4g。则有机物E的分子式为_________ 。
②实验证实其中含有羟基,羧基,甲基,则E的结构简式为______________ 。
③写出E与足量Na的化学方程式___________________ 。
(1)与H2O2具有相同的电子总数的双原子分子有
(2)若从海水中提取碘,需将碘化物变成单质碘。写出在酸性条件下H2O2氧化I—离子的离子方程式
(3)Na2O2、K2O2、CaO2和BaO2都能与酸作用生成H2O2,目前实验室制取H2O2可通过上述某种过氧化物与适量的稀H2SO4作用并过滤后获得,其中最适合的过氧化物是
Ⅱ. 葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是
(2)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水。为研究E的组成与结构,通过实验得到如下信息:
①有机物E的相对分子量为90。9.0g E完全燃烧时,生成CO2 0.3mol, H2O 5.4g。则有机物E的分子式为
②实验证实其中含有羟基,羧基,甲基,则E的结构简式为
③写出E与足量Na的化学方程式
您最近一年使用:0次



